Clear Sky Science · it
L'idrofobicità superficiale e la rigidità determinano la corona proteica su nanoparticelle somministrate per via orale nel trattamento della colite
Trasformare le pillole in terapie più intelligenti
Le persone affette da malattie infiammatorie intestinali come la colite spesso assumono potenti farmaci antinfiammatori, ma gran parte di ogni dose viene sprecata o provoca effetti collaterali in altre parti del corpo. Questo studio esplora un nuovo modo per far agire i farmaci orali come missili guidati: progettando minuscole particelle veicolanti il farmaco che reclutano le proteine intestinali dell’organismo come sistema di targeting naturale, aiutando i farmaci a concentrarsi sulle cellule immunitarie che guidano l’infiammazione intestinale.
Come l’intestino veste le nanoparticelle
Quando una nanoparticella entra nell’organismo, viene rapidamente ricoperta da uno strato sottile di proteine, formando quella che gli scienziati chiamano “corona proteica”. Nell’intestino malato questa corona appare molto diversa rispetto a quella dei tessuti sani perché la composizione proteica locale è cambiata. Gli autori hanno precedentemente scoperto che la colite genera una corona intestinale particolare che indirizza moderatamente le particelle verso cellule immunitarie chiamate macrofagi, che tanto alimentano quanto risolvono l’infiammazione. Qui, hanno cercato di modellare deliberatamente quella corona modificando due proprietà fondamentali delle particelle veicolanti il farmaco — la loro repellenza all’acqua (idrofobicità) e la loro rigidità — per trasformare un effetto modesto, indotto dalla malattia, in una strategia di targeting potente.
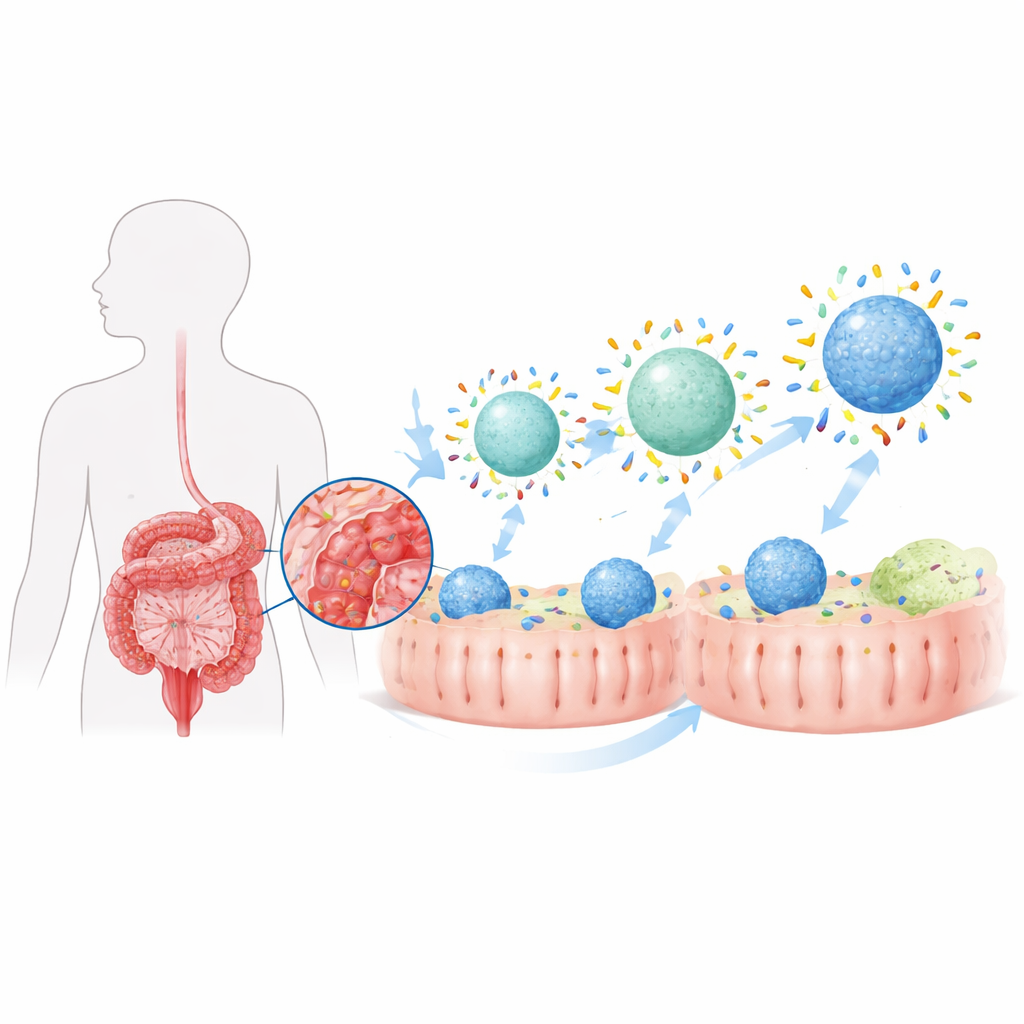
Rendere le particelle più attraenti per le proteine
Il team ha costruito nanoparticelle a base lipidica simili a minuscole bolle di grasso e ha regolato quanto le loro superfici fossero idrofile o idrofobe aggiungendo diverse quantità di un comune rivestimento polimerico. Le particelle con superfici più idrofobe hanno legato molte più proteine intestinali quando sono state esposte a fluidi di colite, sia negli animali sia nelle provette. Quando queste particelle “fobiche” sono state caricate con lo steroide budesonide e somministrate per via orale a ratti con colite, hanno consegnato molta più droga ai macrofagi del colon rispetto alle versioni più idrofile. Di conseguenza, gli animali trattati hanno recuperato più peso corporeo, hanno mostrato minore accorciamento e danno tissutale del colon e avevano livelli più bassi di molecole infiammatorie nell’intestino. Tuttavia, sebbene l’infiammazione sia migliorata, non è tornata completamente a uno stato sano, suggerendo che aumentare semplicemente la quantità totale di proteine nella corona non fosse sufficiente.
Indurire le particelle per scegliere partner migliori
Per spingere il concetto oltre, i ricercatori hanno mantenuto le superfici idrofobe ma hanno modificato la struttura interna per rendere le particelle morbide, intermedie o rigide riempiendo i loro nuclei con sfere di plastica di diverse dimensioni. Tutte e tre hanno comunque acquisito quantità totali simili di proteine intestinali, ma la composizione delle proteine è cambiata. Le particelle più rigide hanno formato corone particolarmente ricche di proteine in grado di agganciarsi a recettori sui macrofagi o di trasportare piccoli nutrienti che queste cellule assorbono. Una di queste proteine, S100A8, è abbondante negli intestini infiammati e può interagire con recettori specifici dei macrofagi. Bloccare S100A8 sulla corona ha ridotto nettamente l’assorbimento delle particelle rigide da parte dei macrofagi, rivelandola come un componente di targeting chiave selezionato dalla rigidità della particella.
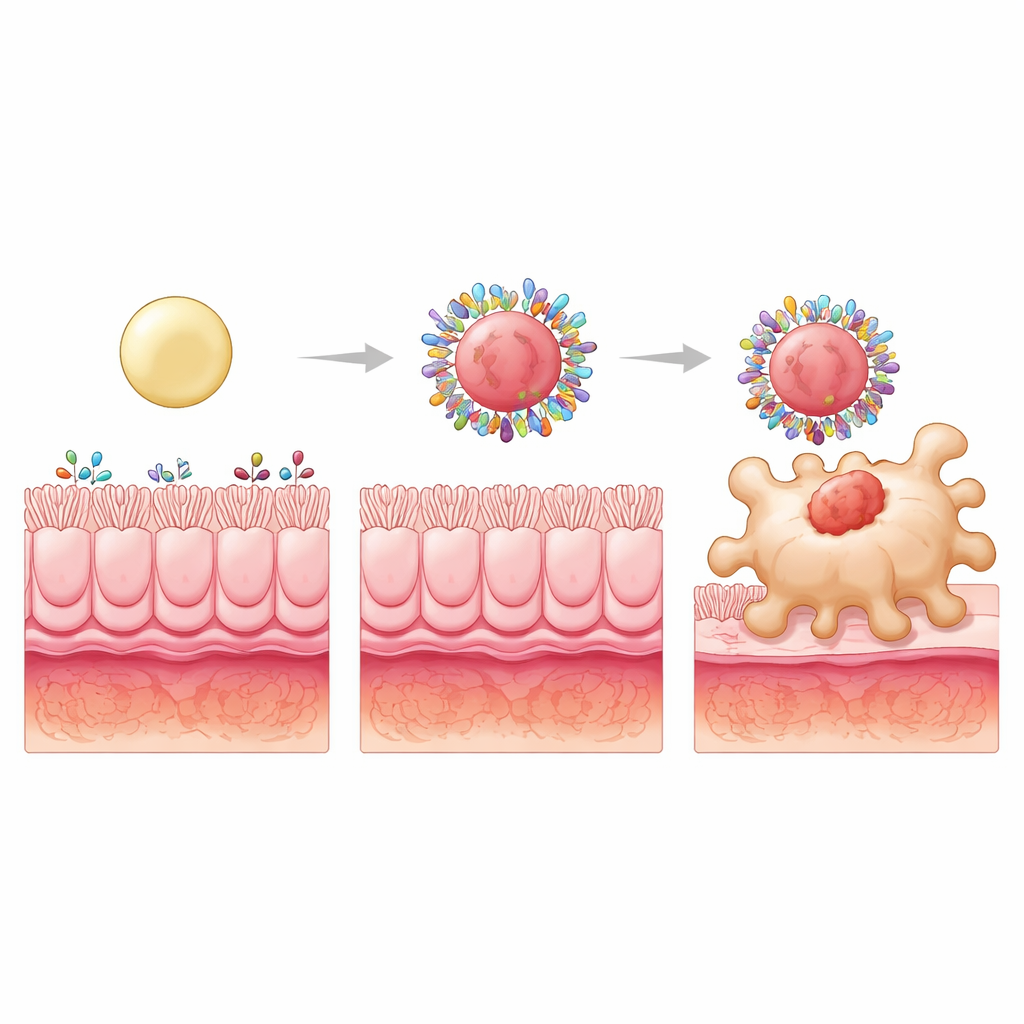
Da un targeting migliore a una guarigione migliore
Quando la budesonide è stata incapsulata in queste particelle ad alta idrofobicità e alta rigidità e somministrata per via orale a ratti con colite, i benefici sono stati notevoli. La formulazione rigida non solo ha ridotto il danno intestinale e lo stress ossidativo, ma ha anche normalizzato più segnali infiammatori a livelli osservati negli animali sani. Ha ripristinato un equilibrio più sano tra tipi di macrofagi “attaccanti” e “calmanti” e ha aumentato le cellule T regolatorie, che aiutano a contenere le risposte immunitarie. È importante sottolineare che questi miglioramenti dipendevano dall’ambiente proteico alterato dalla malattia nella colite; lo stesso design non mostrava un targeting speciale nei ratti sani, sottolineando che la corona è un alleato dinamico e specifico della patologia.
Perché questo è importante per le medicine future
Questo lavoro dimostra che possiamo indirizzare le proteine dell’organismo a comportarsi come etichette intelligenti e auto-rinnovanti sui vettori di farmaci orali semplicemente modulando le proprietà superficiali e meccaniche dei vettori. Incrementando prima la cattura proteica tramite superfici idrofobe e poi usando la rigidità per favorire proteine dirette ai macrofagi come S100A8, i ricercatori hanno creato nanoparticelle che cercano naturalmente le cellule immunitarie che guidano la colite e portano la terapia esattamente dove è più necessaria. La stessa logica progettuale — manipolare come le particelle si percepiscono e si comportano sulla superficie intestinale — potrebbe essere adattata a molti tipi di nanomedicine e patologie, offrendo una strada nuova e più sottile verso trattamenti mirati senza dover aggiungere molecole di targeting artificiali.
Citazione: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Parole chiave: somministrazione di farmaci con nanoparticelle, malattie infiammatorie intestinali, corona proteica, nanomedicina orale, miraggio dei macrofagi