Clear Sky Science · it
Un atlante d’interazioni su scala di genere tra gli ortologhi di NS4B identifica un ruolo conservato per l’UFMilazione nella replicazione degli ortoflavivirus
Perché questo studio sui virus è importante
Virus come dengue, Zika e West Nile si stanno diffondendo in nuove aree e possono causare sintomi che vanno dalla febbre alle infezioni cerebrali e alle malformazioni congenite. Eppure continuiamo a non disporre di terapie ampie e affidabili. Questo studio esplora come una collaborazione nascosta tra questi virus e un poco noto sistema di marcatura cellulare chiamato UFMilazione aiuti i patogeni a moltiplicarsi. Mappando questa relazione in molti virus correlati, gli autori individuano un punto debole condiviso che potrebbe essere sfruttato per sviluppare futuri farmaci antivirali.
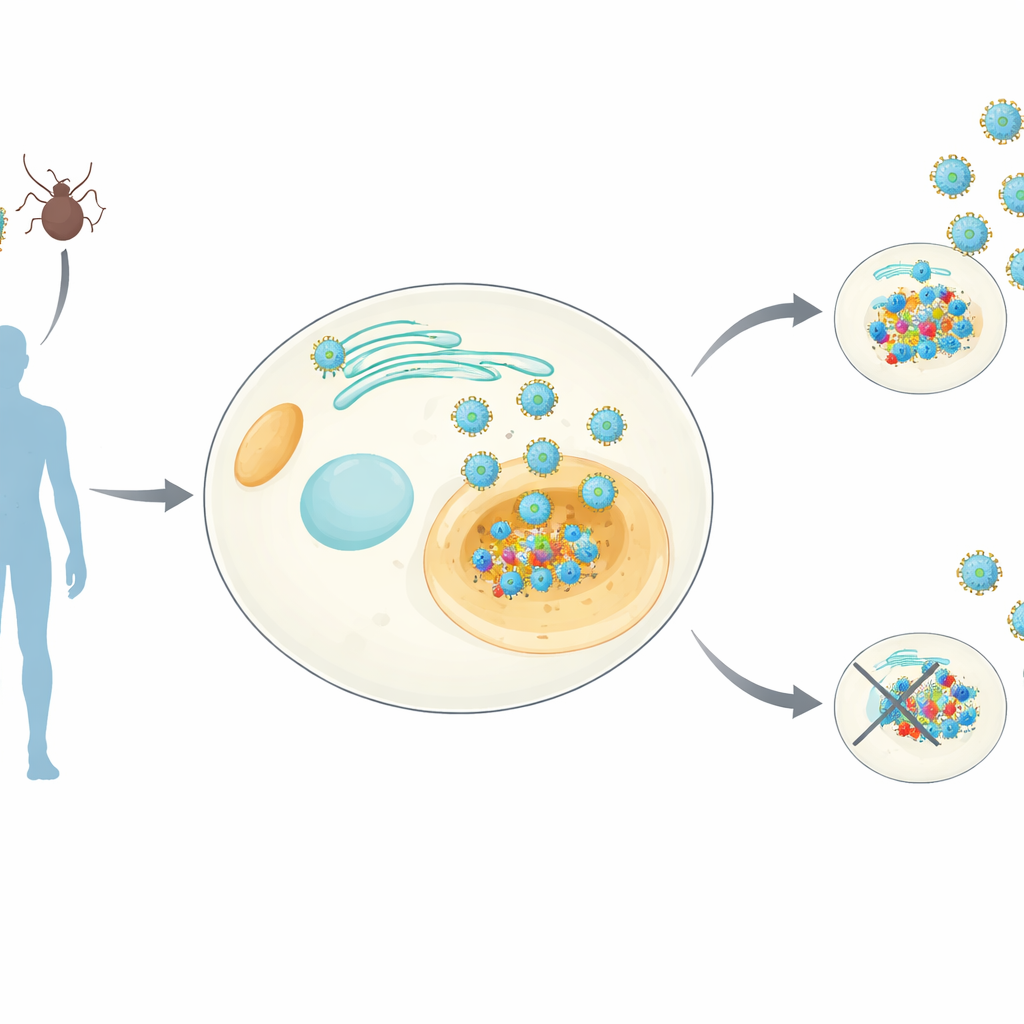
Seguire un importante insider virale
Gli ortoflavivirus – il gruppo che include dengue, Zika, febbre gialla e altri – possiedono tutti una piccola proteina chiamata NS4B che si inserisce nelle membrane all’interno delle nostre cellule. NS4B è nota per essere essenziale alla replicazione virale, ma le sue funzioni precise sono rimaste poco chiare. I ricercatori hanno creato linee cellulari umane che producono stabilmente NS4B proveniente da otto diversi ortoflavivirus. Hanno quindi usato tecniche sensibili di spettrometria di massa per isolare NS4B insieme alle proteine umane che vi si legano e, in parallelo, hanno misurato come l’espressione di NS4B alteri il profilo complessivo delle proteine nella cellula. Questo ha prodotto un “atlante delle interazioni” a livello di genere – che chiamano NS4Bome – mostrando bersagli ospiti sia comuni sia specifici per virus.
Trucchi condivisi e strategie su misura
L’atlante ha rivelato 538 proteine umane che interagiscono con NS4B e oltre 500 la cui abbondanza cambia quando NS4B è presente. Molte di queste sono concentrate in percorsi che gestiscono la produzione di energia nei mitocondri, la rimodellazione delle membrane interne e il traffico di proteine e lipidi neoformati. Alcune interazioni erano condivise dalla maggior parte dei virus, suggerendo stratagemmi evolutivamente conservati usati da tutti gli ortoflavivirus. Altre sono apparse solo in certe specie o ceppi, spiegando potenzialmente perché alcuni virus preferiscono zanzare rispetto a zecche, o causano malattia cerebrale invece di febbre emorragica. Questa visione sistematica trasforma un insieme intricato di studi precedenti sparsi in una mappa coerente di come questi virus riorientano la cellula.
Un alleato sorprendente: il sistema di UFMilazione
Tra i molti partner a cui NS4B si legava, uno è emerso in modo particolare: UBA5, l’enzima iniziale della via di UFMilazione. L’UFMilazione è un sistema cellulare che attacca un piccolo tag proteico, UFM1, a bersagli selezionati, influenzando processi come il controllo della qualità proteica e le risposte allo stress. Usando interferenza con RNA e knockout genetici basati su CRISPR, il gruppo ha mostrato che cellule prive di UBA5 o incapaci di eseguire l’UFMilazione presentavano una replicazione molto ridotta di Zika e di diversi virus correlati. Reintrodurre UBA5 normale ha ripristinato la crescita virale, mentre forme mutanti incapaci di guidare l’UFMilazione non l’hanno fatto, dimostrando che l’attività di marcatura è essa stessa cruciale per l’infezione.
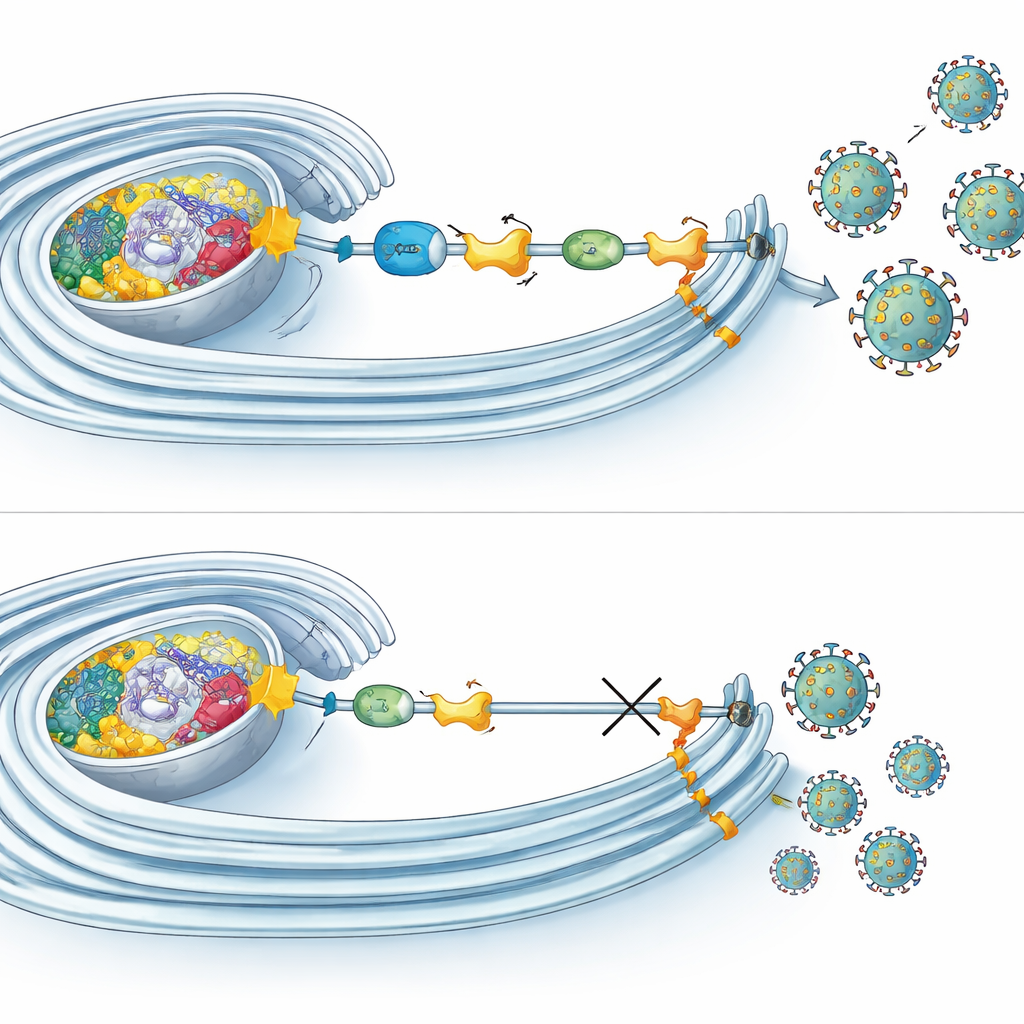
Come la marcatura sostiene le fabbriche virali
Microscopia ed esperimenti biochimici hanno rivelato che più componenti dell’UFMilazione si raggruppano proprio nei siti dove l’RNA virale viene copiato all’interno di membrane rimodellate. Lì si associano non solo con NS4B ma anche con altre proteine virali che costruiscono la macchina di replicazione. Interessante, bloccare l’UFMilazione non ha impedito l’ingresso virale, la produzione di RNA o la sintesi proteica. Piuttosto, ha compromesso soprattutto le fasi tardive del ciclo, come l’assemblaggio o il rilascio di particelle infettive. Allo stesso tempo, l’UFMilazione ha influenzato il modo in cui i mitocondri respirano: quando la via era disabilitata, le cellule mostravano un consumo di ossigeno ridotto e forme mitocondriali alterate. Al contrario, nelle fasi iniziali dell’infezione da Zika, la respirazione mitocondriale aumentava, suggerendo che i virus possano sfruttare l’UFMilazione per potenziare la produzione di energia della cellula proprio quando ne hanno più bisogno.
Testare un farmaco in cellule e piccoli pesci
Gli autori si sono poi concentrati su un composto a piccola molecola, DKM 2‑93, che blocca il sito attivo di UBA5. In cellule umane coltivate, questo inibitore ha ridotto la produzione di virus Zika di circa dieci volte a dosi che lasciavano le cellule sostanzialmente sane, mostrando attività in diversi tipi cellulari. Per verificare se questa strategia potesse funzionare in un organismo vivente, hanno usato un modello di zebrafish per l’infezione da Zika, che imita caratteristiche chiave della malattia nel cervello in sviluppo. Trattare embrioni infettati con DKM 2‑93 durante le prime fasi dello sviluppo cerebrale ha abbassato significativamente i livelli di RNA virale e ridotto la proporzione di pesci con malformazioni gravi, indicando un reale beneficio antivirale in vivo.
Cosa significa per i trattamenti futuri
Costruendo una mappa completa di come NS4B di molti ortoflavivirus interagisca con le proteine umane, questo studio mette in luce l’UFMilazione come una via aiutante conservata da cui questi virus dipendono per produrre particelle infettive. Poiché lo stesso sistema dell’ospite sembra sostenere dengue, Zika, West Nile e altri, farmaci che attenuino selettivamente l’UFMilazione potrebbero agire come antivirali ad ampio spettro, invece di mirare a un singolo virus alla volta. Sebbene siano necessari ulteriori studi per capire esattamente quali proteine vengano marcate e per garantirne la sicurezza, i risultati identificano un promettente bersaglio basato sull’ospite che un giorno potrebbe contribuire a frenare focolai di più malattie trasmesse da zanzare e zecche con un unico approccio terapeutico.
Citazione: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Parole chiave: virus Zika, dengue, interazioni ospite–virus, UFMilazione, antivirali ad ampio spettro