Clear Sky Science · it
Le snoRNA terminate da CPF-CF transitano attraverso il citoplasma tramite un meccanismo di sorveglianza mediato da proteine guardiane dell’mRNA
Come le minuscole RNA guida fanno una deviazione inaspettata
All'interno di ogni cellula, la sintesi delle proteine dipende da una precisa coreografia molecolare. Una parte chiave di questa danza è controllata dalle piccole RNA nucleolari, o snoRNA, che aiutano a sagomare i ribosomi della cellula—le macchine che costruiscono le proteine. Questo studio rivela che alcune di queste piccole guide escono inaspettatamente dal nucleo, visitano brevemente il citoplasma e poi ritornano, tutto a causa del modo in cui viene interrotta la loro produzione. Capire questo percorso di traffico nascosto fa luce su come le cellule tutelano la qualità degli RNA e proteggono l’informazione genetica.
Uno sguardo più attento agli aiutanti RNA della cellula
Le snoRNA sono brevi molecole di RNA che fungono da guide, indirizzando modifiche chimiche su altri RNA, in particolare quelli che costituiscono i ribosomi. Nelle cellule di lievito, la maggior parte delle snoRNA viene prodotta nel nucleo e si pensava rimanesse lì per tutta la vita, formando partnership stabili con proteine specifiche per creare gli snoRNP, i complessi operativi che modificano l'RNA ribosomiale. Tuttavia lavori precedenti avevano rilevato snoRNA in contatto con proteine normalmente coinvolte nell’esportazione degli mRNA fuori dal nucleo. Questa osservazione enigmatica ha sollevato una domanda: le snoRNA a volte viaggiano verso il citoplasma e, in tal caso, perché?
Scoprire le snoRNA in movimento
Rianalizzando dati di sequenziamento dell'RNA ottenuti da frazioni nucleari e citoplasmatiche accuratamente separate, gli autori hanno trovato che molte snoRNA sono effettivamente presenti nel citoplasma delle cellule di lievito normali, a livelli simili a quelli degli mRNA tipici. Quando hanno disattivato fattori chiave di esportazione, Mex67 e Xpo1, il pool citoplasmatico di snoRNA si è ridotto e nel nucleo si è accumulata una popolazione di precursori immaturi di snoRNA con estensioni 3′. La microscopia con sonde fluorescenti ha confermato questo spostamento: segnali che normalmente apparivano sia nel nucleolo sia debolmente nel citoplasma sono diventati fortemente nucleari quando l’esportazione è stata bloccata. Questi risultati mostrano che un sottoinsieme di snoRNA, spesso ancora portatore di sequenza extra alle estremità, viene attivamente trasportato fuori dal nucleo e non è semplicemente il risultato di perdite o contaminazioni del campione.
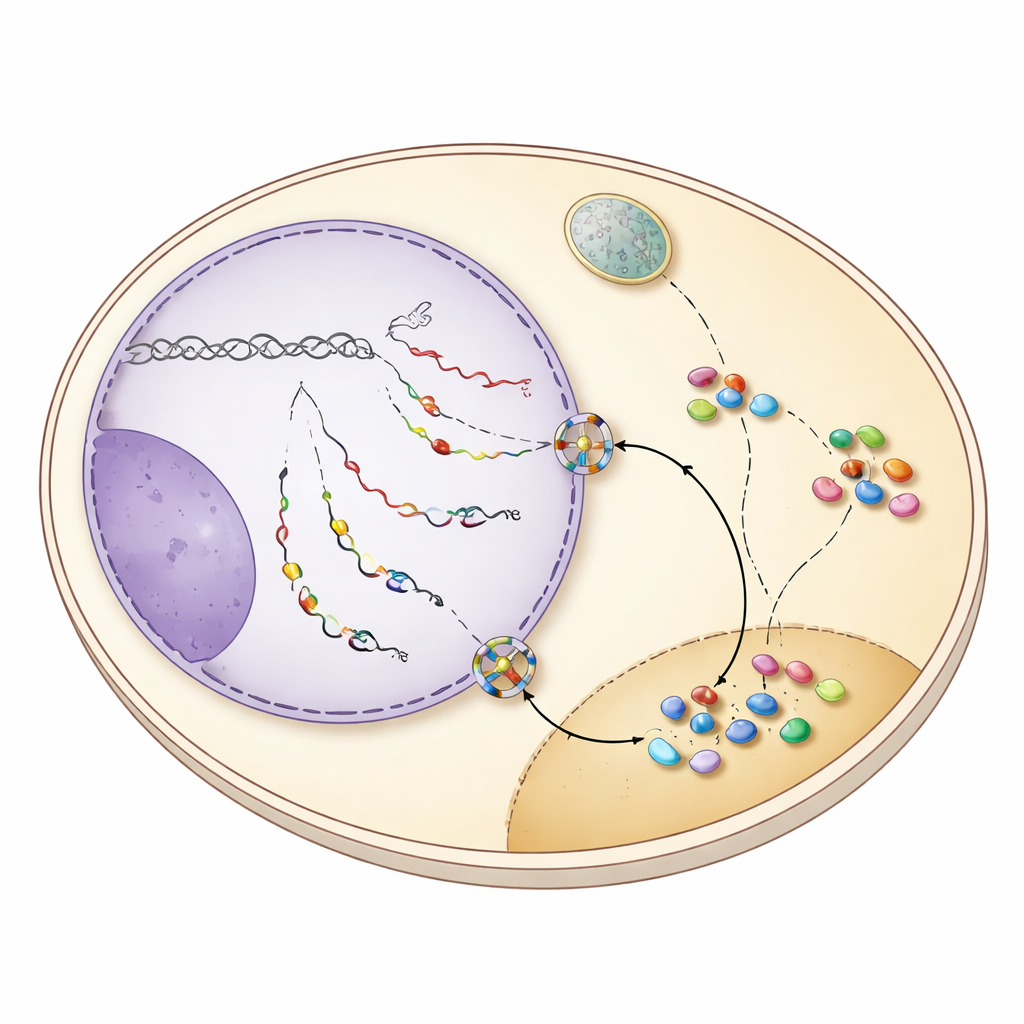
L'interruttore della proteina guardiana che manda le snoRNA fuori
La chiave di questo comportamento di shuttle risiede nel modo in cui viene terminata la trascrizione delle snoRNA. Nel lievito, la maggior parte delle snoRNA viene normalmente rilasciata dalla macchina trascrizionale da un sistema chiamato NNS, che le lascia con una coda corta prontamente rifilata nel nucleo. Molti geni di snoRNA, tuttavia, ospitano anche segnali di arresto di riserva riconosciuti da un secondo sistema, CPF‑CF, noto soprattutto per terminare gli mRNA e aggiungere lunghe code poli(A). Quando la terminazione NNS vacilla, i trascritti di snoRNA procedono fino a questi siti CPF‑CF a valle e ricevono una coda più lunga. Questa terminazione alterata recluta un insieme di proteine “guardiane”—tra cui Hrp1 e Nab2—che controllano il corretto processamento e contemporaneamente attirano il fattore di esportazione Mex67. Lo studio mostra che quando le snoRNA sono terminate da CPF‑CF, le proteine guardiane e Mex67 cooperano per inviare queste snoRNA codate attraverso i pori nucleari nel citoplasma.
Biglietti di andata e ritorno e controllo qualità
Una volta nel citoplasma, le snoRNA non vengono lasciate incustodite. Rimangono legate a un anello protettivo di proteine Lsm e al fattore Lhp1, che schermano l’estremità vulnerabile dell'RNA. Queste caratteristiche permettono a due recettori di importazione, Cse1 e Mtr10, di riconoscere le snoRNA in transito e riportarle nel nucleo. Quando gli autori hanno disattivato questi fattori di importazione o l’anello Lsm, precursori di snoRNA immaturi si sono accumulati nel citoplasma, confermando che questa macchina media il loro ritorno. Tornate nel nucleo, le code lunghe vengono rimosse dall’esosoma nucleare, le proteine core degli snoRNP si assemblano completamente e i complessi maturi si rilocalizzano al nucleolo. È importante notare che le snoRNA che avevano fatto questa deviazione risultavano pienamente funzionali: una snoRNA modello, snR13, ha continuato a eseguire le specifiche modifiche chimiche sull'RNA ribosomiale dopo essere stata terminata da CPF‑CF e inviata attraverso il citoplasma.
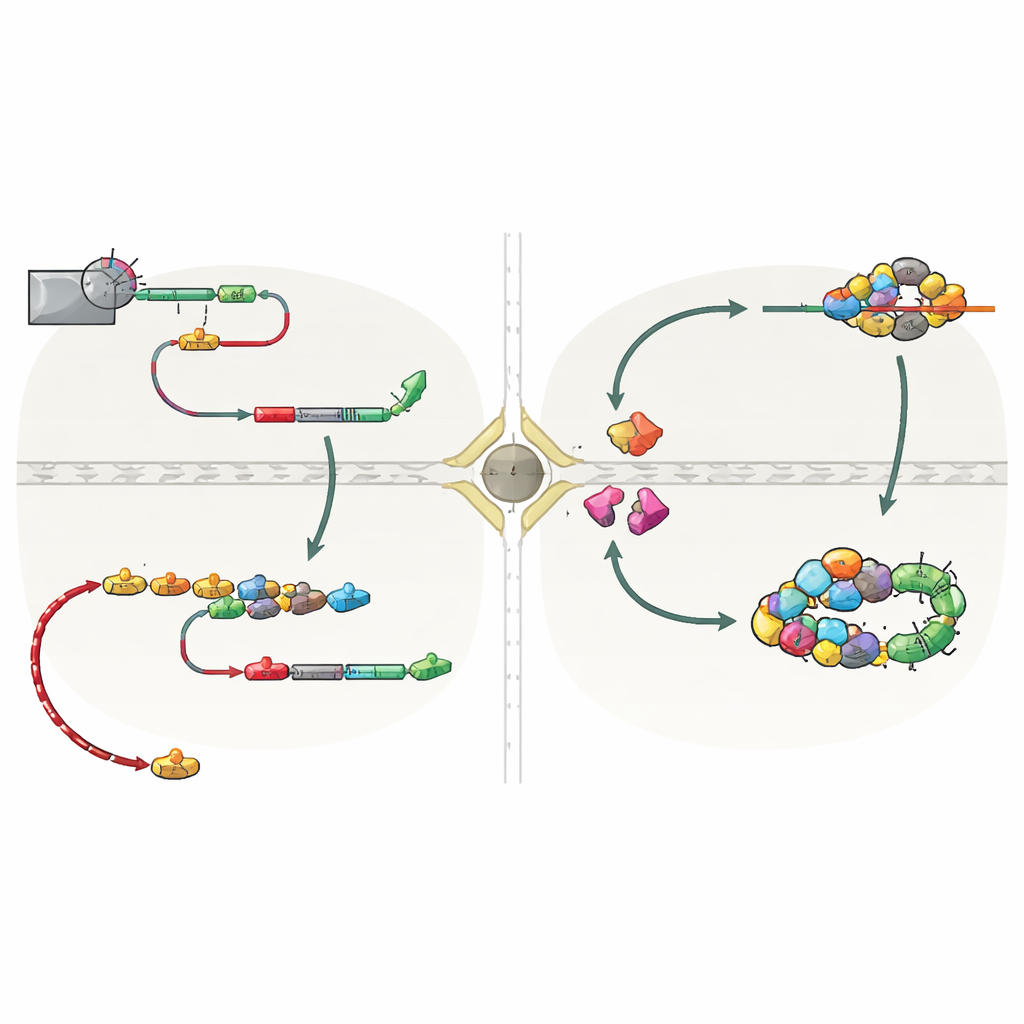
Perché questo percorso nascosto è importante
Questo lavoro rivela che il viaggio delle snoRNA non è un caso isolato, ma una via di riserva integrata controllata dal modo in cui termina la trascrizione. Quando il sistema NNS primario è indebolito—per esempio in particolari fasi del ciclo cellulare—i segnali CPF‑CF a valle salvano la produzione di snoRNA. Ciò evita lo spreco di RNA già sintetizzato e previene trascrizioni incontrollate che potrebbero interferire con geni vicini e danneggiare il DNA. Gli autori trovano anche indizi di una via di riserva analoga nelle cellule umane, dove snoRNA codificate singolarmente possono acquisire code poli(A) in siti correlati. In termini semplici, lo studio mostra che il “segnale di stop” scelto alla fine di un gene snoRNA decide se quell’RNA matura silenziosamente nel nucleo o esce brevemente e ritorna sotto la sorveglianza delle proteine guardiane. Questo meccanismo di sorveglianza guidato dalla terminazione della trascrizione aiuta a mantenere il panorama dell'RNA cellulare sia flessibile che sicuro.
Citazione: Yu, F., Zaccagnini, G., Duan, Y. et al. CPF-CF-terminated snoRNAs shuttle through the cytoplasm via an mRNA guard protein-mediated surveillance mechanism. Nat Commun 17, 2328 (2026). https://doi.org/10.1038/s41467-026-70373-8
Parole chiave: snoRNA, controllo della qualità dell'RNA, esportazione nucleare, terminazione della trascrizione, genetica della lievito