Clear Sky Science · it
Controllo della funzione dei lisosomi da parte della proteina GTPasi‑attivante TBC1D9B e del suo partner legante TMEM55B
Come i centri di riciclo cellulari mantengono l’equilibrio
All’interno di ciascuna delle nostre cellule sono presenti piccole sacche chiamate lisosomi che funzionano come centri di riciclo e hub di controllo per la crescita. Quando funzionano bene, le parti usurate vengono degradate e i loro componenti riutilizzati; quando falliscono, i rifiuti si accumulano e possono insorgere malattie, tra cui neurodegenerazione e cancro. Questo studio rivela come due proteine poco conosciute aiutino a commutare i lisosomi tra uno stato vagante, favorevole alla crescita, e una modalità aggregata, focalizzata sulla degradazione dei rifiuti, facendo luce su come le cellule si adattino a situazioni di abbondanza e carenza.
Spostare i centri di riciclo all’interno della cellula
I lisosomi non sono fissati in un punto. Viaggiano lungo piste interne, trascinati verso l’esterno da un insieme di motori molecolari e richiamati verso l’interno da un altro. La loro posizione nella cellula è importante: quando i nutrienti sono abbondanti, i lisosomi si distribuiscono verso le regioni periferiche della cellula e contribuiscono a sostenere i segnali di crescita; quando il cibo scarseggia, si ritirano al centro, diventano più acidi e intensificano la degradazione del materiale cellulare. Una piccola proteina simile a un interruttore chiamata ARL8 è nota per spingere i lisosomi verso l’esterno, ma fino ad ora nessuno aveva identificato un sistema frenante dedicato per ostacolarla. Gli autori hanno ipotizzato che un tale freno sarebbe cruciale per permettere alle cellule di passare rapidamente a una modalità di conservazione durante la fame.
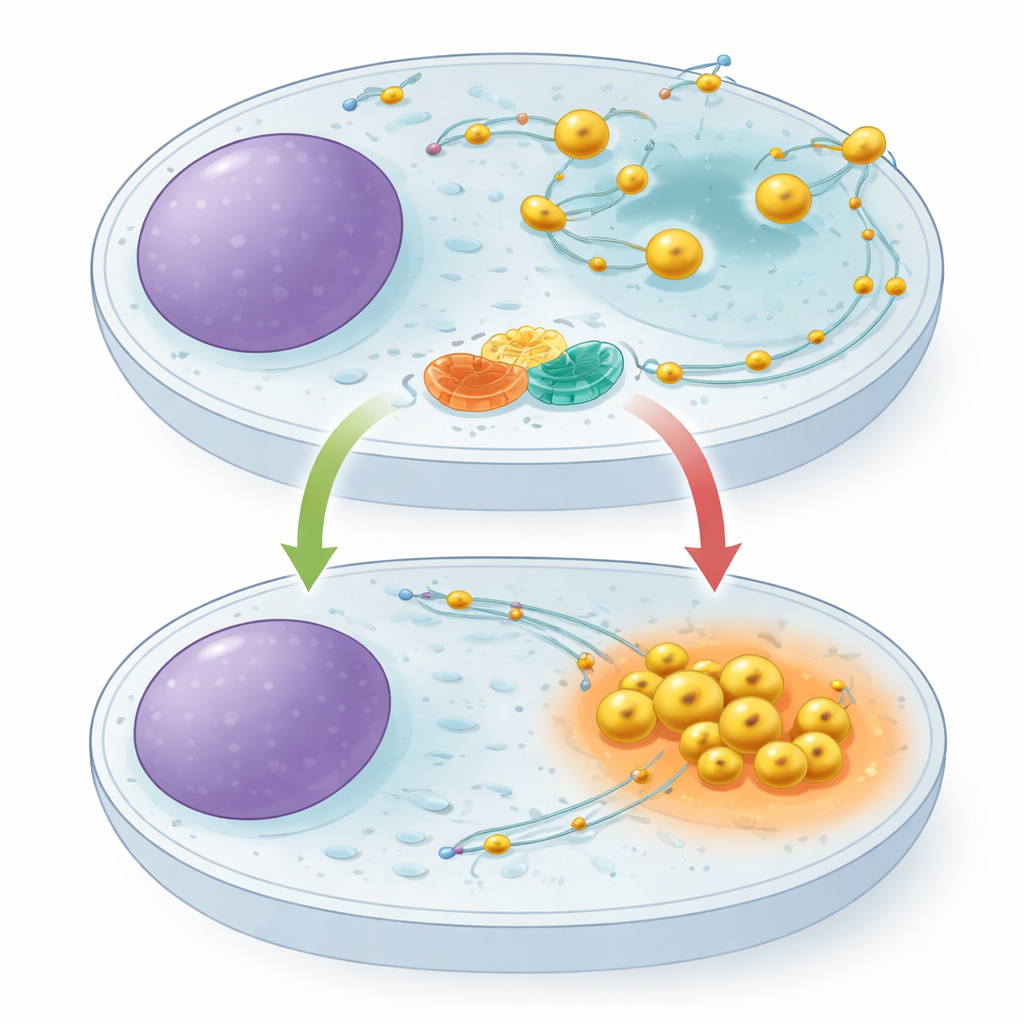
Una collaborazione molecolare sulla superficie del lisosoma
Usando tecniche di “pescaggio” proteico e spettrometria di massa, i ricercatori hanno scoperto che una proteina chiamata TBC1D9B si lega a una proteina di membrana lisosomiale denominata TMEM55B. TMEM55B attraversa l’involucro esterno del lisosoma, mentre TBC1D9B è per lo più solubile e può ancorarsi alla membrana. Il team ha dimostrato che queste due formano un complesso diretto: la TBC1D9B purificata si attacca alla porzione esposta di TMEM55B in provetta, e versioni marcate delle proteine si co‑precipitano da estratti cellulari. Una mappatura accurata dei segmenti proteici ha rivelato che diverse regioni di TBC1D9B contattano TMEM55B, posizionando TBC1D9B sulla superficie del lisosoma senza bloccare la parte della proteina responsabile della sua attività catalitica.
Quando il freno fallisce, i lisosomi vanno fuori controllo
Per capire cosa fa questa collaborazione, gli autori hanno usato l’editing CRISPR per rimuovere TMEM55B o TBC1D9B dalle cellule umane. In entrambi i casi, i lisosomi non si raggruppavano più vicino al nucleo ma si disperdevano verso il bordo cellulare e si muovevano più velocemente lungo le loro piste, imitando cellule in uno stato di alimentazione continua. Reintrodurre la TBC1D9B normale ripristinò il posizionamento corretto, mentre una versione priva di capacità catalitica no, indicando che la sua attività enzimatica è essenziale. Quando le cellule vennero private di nutrienti, le cellule di controllo richiamarono i lisosomi verso l’interno e aumentarono il loro potere digestivo, come dimostrato dall’aumento dell’attività di enzimi chiave e dalla maggiore degradazione di carichi di prova. Le cellule prive di TMEM55B o TBC1D9B non riuscirono a farlo: i loro lisosomi rimasero periferici e la loro risposta degradativa alla fame risultò attenuata. Anche l’autofagia, il processo con cui le cellule si “mangiano” componenti danneggiati, risultò compromessa, con una minore elaborazione di un marcatore dell’autofagia e accumulo della proteina adattatrice p62.
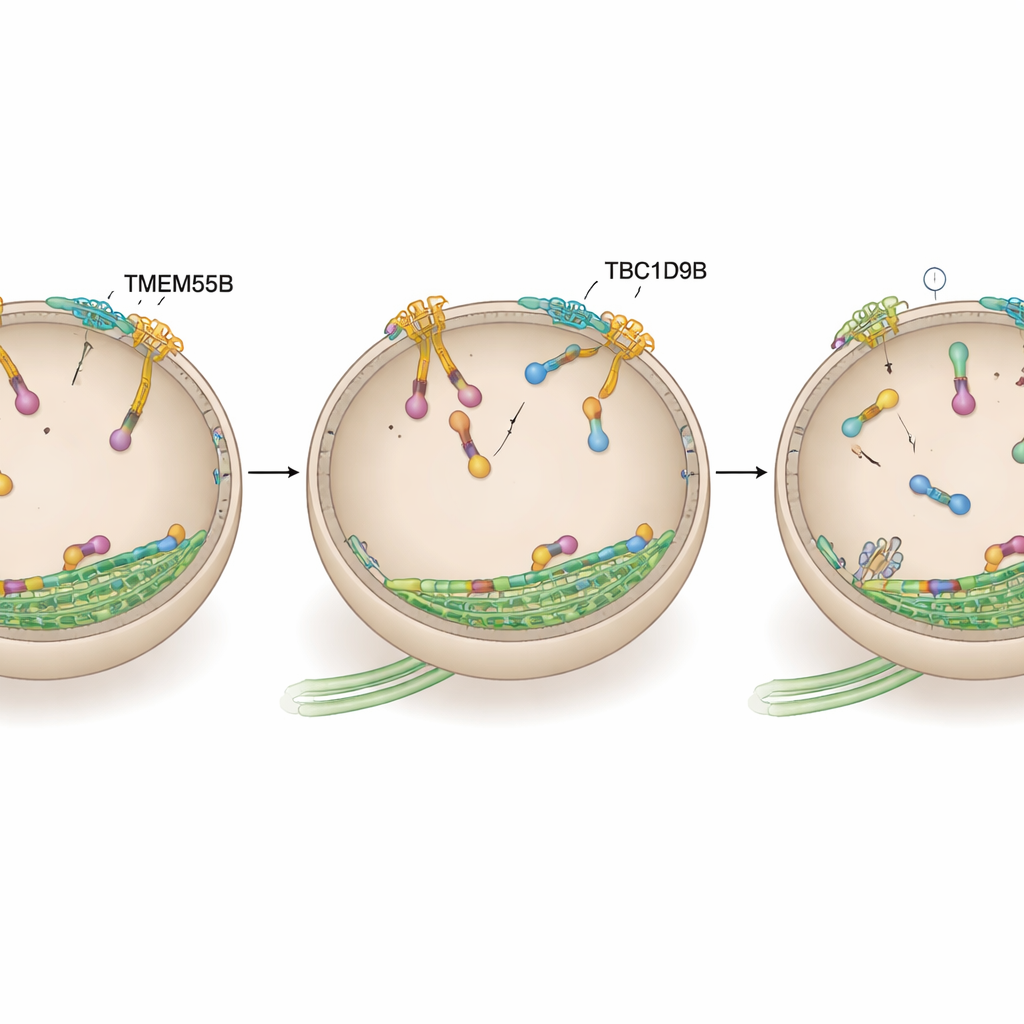
Spegnere il motore del lisosoma
Il gruppo ha quindi indagato se TBC1D9B eserciti i suoi effetti agendo direttamente su ARL8, l’interruttore che guida verso l’esterno. Utilizzando marcatura di prossimità in neuroni umani e test di legame in linee cellulari e con proteine purificate, hanno mostrato che TBC1D9B si lega selettivamente alla forma attiva, caricata di GTP, della variante ARL8B, ma non alla sua forma inattiva né all’affine ARL8A. Modellizzazioni strutturali hanno previsto che residui chiave di TBC1D9B contattino la tasca del GTP di ARL8B. In saggi biochimici, TBC1D9B accelerò l’idrolisi del GTP legato ad ARL8B, convertendo di fatto la proteina dallo stato “on” a quello “off”; una versione mutante di TBC1D9B priva di questi residui non fu più in grado di farlo. Coerentemente con ciò, le cellule prive di TMEM55B o TBC1D9B mostrarono un aumento di ARL8B sui lisosomi, mentre la sovraespressione di TBC1D9B richiamò i lisosomi verso il centro, similmente a una riduzione dell’attività di ARL8B.
Una nuova manopola di controllo per le pulizie cellulari
Infine, gli autori testarono se questo freno su ARL8B spiegasse i cambiamenti cellulari osservati in assenza di TBC1D9B. Quando ARL8B fu depletato, i lisosomi restarono raggruppati vicino al nucleo indipendentemente dalla presenza di TMEM55B o TBC1D9B, e i difetti nell’autofagia causati dalla perdita di TBC1D9B furono in gran parte compensati. Nel complesso, i dati supportano un modello in cui TMEM55B recluta TBC1D9B sui lisosomi, dove questa inattiva ARL8B e permette ai lisosomi di passare da uno stato disperso, di supporto alla crescita, a uno centralizzato, focalizzato sulla digestione. Per i non specialisti, ciò significa che lo studio ha scoperto una manopola importante che le cellule usano per decidere quando riciclare più aggressivamente, un processo con implicazioni per disturbi da accumulo di rifiuti nel cervello, il metabolismo e il cancro.
Citazione: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Parole chiave: lisosomi, autofagia, segnalazione cellulare, trasporto degli organelli, neurodegenerazione