Clear Sky Science · it
L’attivazione di NF-κB negli astrociti compromette la guarigione delle ferite dopo lesione cerebrale traumatica nei topi maschi
Perché le contusioni cerebrali non guariscono sempre in modo netto
Quando una persona subisce un colpo alla testa, la ferita visibile all’esterno è solo una parte della storia. In profondità nel cervello si attiva una complessa risposta di guarigione che può determinare se chi ha subito l’infortunio recupera bene o sviluppa problemi duraturi di memoria, umore o movimento. Questo studio sui topi maschi mette in luce come una via dello stress chiave all’interno delle cellule di supporto chiamate astrociti possa trasformare una risposta di riparazione normale in una che, paradossalmente, aggrava il danno dopo una lesione cerebrale traumatica.
I primi soccorritori nascosti del cervello
Gli astrociti sono cellule a forma di stella che circondano i neuroni e i vasi sanguigni, contribuendo a mantenere stabile l’ambiente interno del cervello. Dopo un trauma cranico cambiano rapidamente forma e comportamento, formando una barriera attorno all’area danneggiata e aiutando a ricostruire il tessuto. I ricercatori si sono concentrati su un interruttore molecolare all’interno di queste cellule chiamato NF-κB, noto per il suo ruolo nel controllo dell’infiammazione in molti tessuti. Hanno chiesto se, dopo una lesione a cranio chiuso simile alle comuni commozioni e contusioni umane, questo interruttore favorisca o ostacoli la capacità del cervello di guarire.
Un interruttore di stress che si accende dopo l’impatto
Analizzando l’attività genica nel tessuto cerebrale dei topi dopo il trauma, il gruppo ha riscontrato un’impennata di geni legati all’infiammazione e alla segnalazione NF-κB, soprattutto tra il terzo e il settimo giorno dopo il trauma, quando il danno secondario aumenta. Usando topi reporter, hanno mostrato che l’attivazione di NF-κB non era diffusa in tutto il cervello ma concentrata intorno al sito dell’impatto. Lì risultava particolarmente attiva nelle microglia (le sentinelle immunitarie del cervello) e negli astrociti che formano il confine della ferita. Tempistica e localizzazione suggerivano che NF-κB negli astrociti potesse essere un regolatore cruciale di come il cervello organizza la cicatrice e controlla la risposta immunitaria.
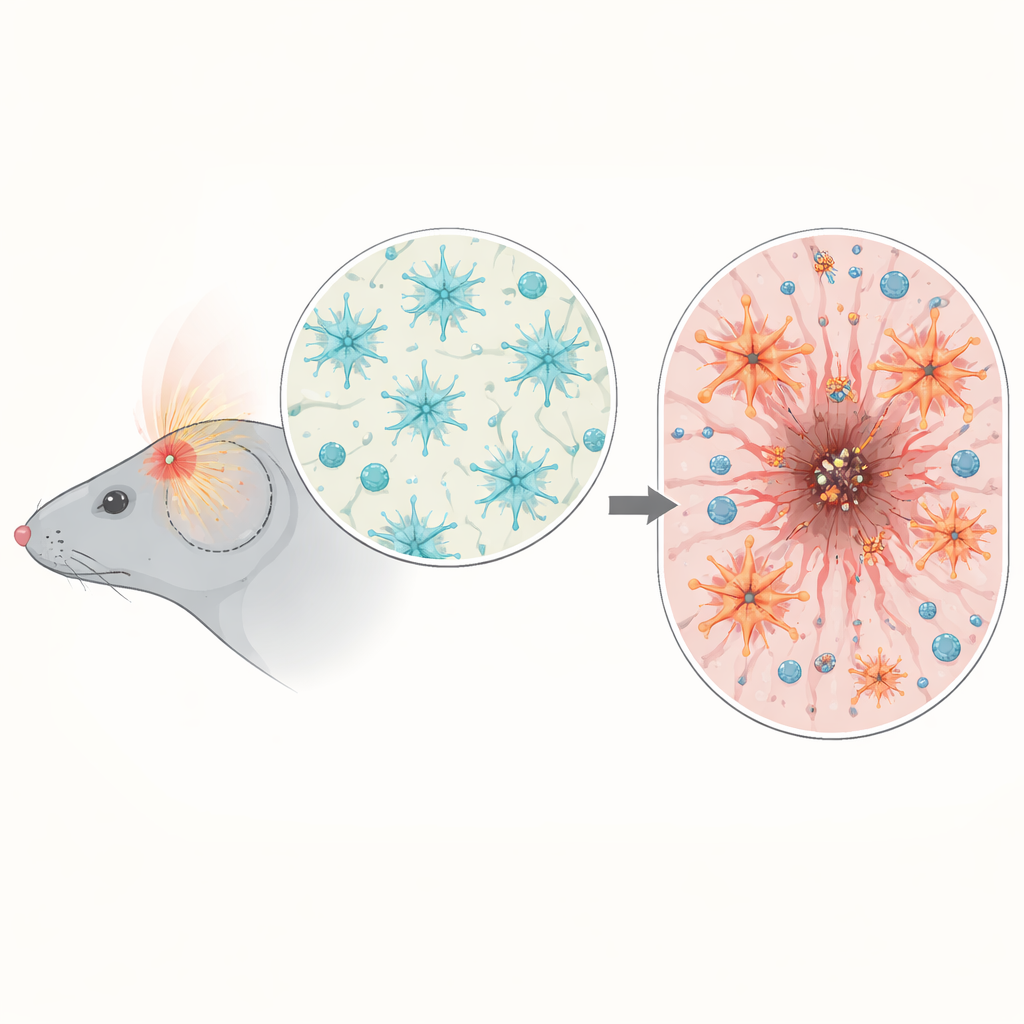
Attivare troppo gli astrociti
Per testare causa ed effetto, gli scienziati hanno ingegnerizzato topi in cui l’attività di NF-κB negli astrociti era o artificialmente aumentata o attenuata, ma solo dopo il completamento dello sviluppo cerebrale. Quando questi topi hanno subito un trauma cranico, quelli con NF-κB iperattivo negli astrociti hanno perso più peso, mostrato punteggi neurologici peggiori nelle prime fasi e presentato lesioni cerebrali più grandi e persistenti sia nelle sezioni di tessuto sia nelle risonanze magnetiche. Invece di formare una cicatrice pulita e ben definita che isola il nucleo danneggiato, i loro astrociti hanno prodotto un confine spesso e disorganizzato che non è riuscito a ridurre la ferita nel tempo. L’equilibrio normale delle proteine di matrice di supporto intorno alla lesione è risultato disturbato e una struttura barriera esterna chiave, nota come limitans gliale, si è formata in modo inadeguato, lasciando meno protetto il tessuto cerebrale circostante.
Quando i programmi di riparazione deragliano
Approfondendo i dettagli molecolari, il team ha isolato astrociti e cellule immunitarie vicine per un’analisi gene per gene. Negli animali sani, l’infortunio normalmente sopprime alcune funzioni di “manutenzione” degli astrociti mentre attiva geni che supportano la chiusura della ferita e la rigenerazione. Al contrario, gli astrociti con NF-κB cronicamente attivo apparivano già «danneggiati» anche prima del trauma e, dopo l’impatto, non riuscivano ad attivare pienamente i programmi riparativi benefici, come quelli associati a una trasformazione controllata che aiuta le cellule a costruire un confine efficace. Preferivano invece fortemente geni infiammatori, assumevano caratteristiche di uno stato astrocitario tossico legato all’invecchiamento e alle malattie neurodegenerative e mostravano segni di un profilo secretorio «simile alla senescenza» associato a ferite croniche non risolutive.
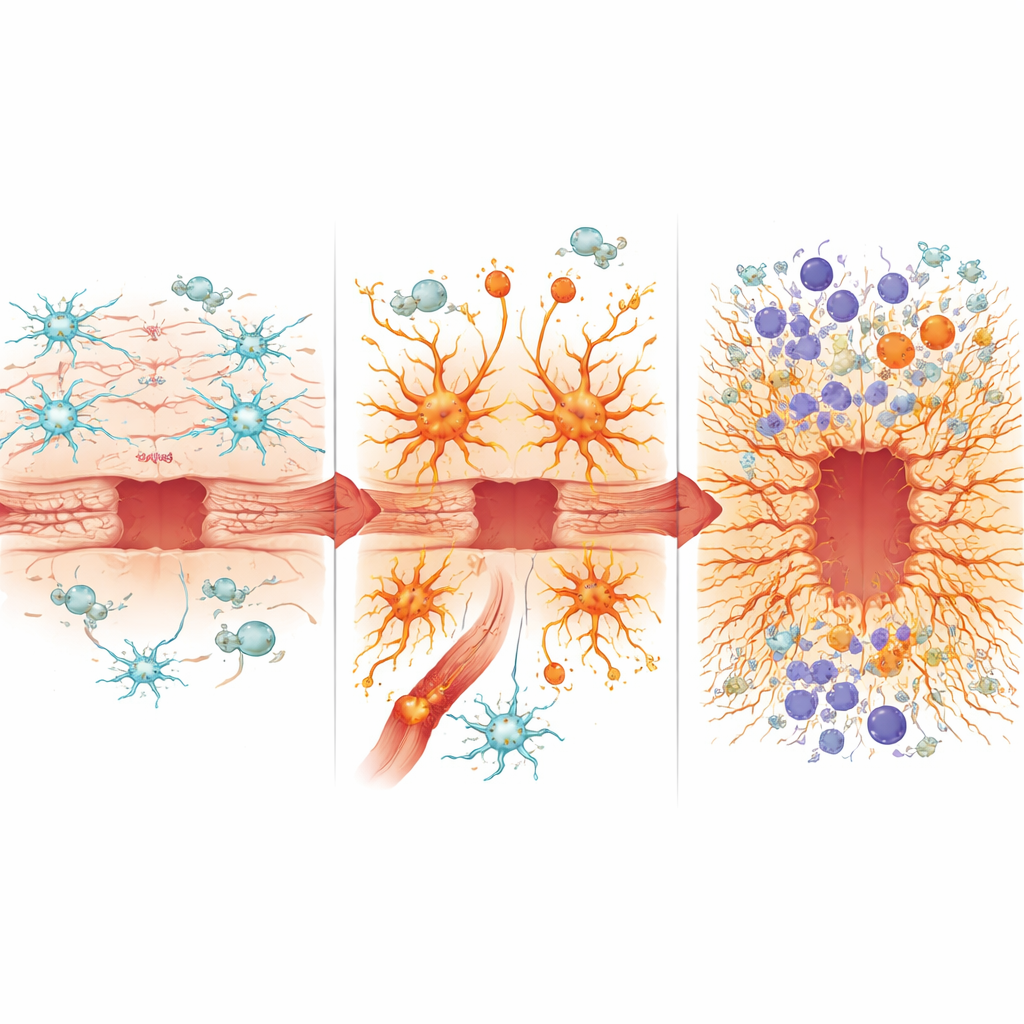
Alimentare l’incendio immunitario
Questi astrociti mal programmati hanno anche rimodellato il panorama immunitario cerebrale. La barriera emato-encefalica è diventata più permeabile, lasciando entrare più cellule immunitarie periferiche. I topi con NF-κB iperattivo negli astrociti hanno mostrato un’infiltrazione maggiore di cellule mieloidi infiammatorie e miscele alterate di neutrofili, monociti e cellule dendritiche, oltre a un aumento di linfociti T citotossici che possono danneggiare ulteriormente il tessuto. Le cellule immunitarie in questo contesto esprimevano segnali più forti guidati da vie dell’interferone e dell’inflammasoma, entrambe associate a infiammazione aggressiva e potenzialmente neurotossica. Allo stesso tempo, i livelli di diverse proteine protettive o pro-riparative, come l’osteopontina, risultavano ridotti, mentre altri fattori legati allo stress ossidativo, al sovraccarico di ferro e alla formazione di cicatrici, inclusi emossigenasi-1 e lipocalina-2, erano elevati. Il rapporto tra osteopontina e lipocalina-2 è emerso come un marcatore semplice che correla con una guarigione migliore o peggiore nelle diverse linee di topi.
Cosa significa per il recupero da un trauma cranico
Nel complesso, i risultati mostrano che quando la via di stress NF-κB negli astrociti è cronicamente sovraattivata, queste cellule passano dal sostenere una riparazione organizzata al favorire una cicatrizzazione caotica e un’infiammazione prolungata. Invece di costruire un confine netto che contenga il danno e permetta il rimodellamento tissutale, contribuiscono a creare un ambiente permeabile e infiammatorio che ingrandisce la lesione e compromette l’esito a lungo termine. Sebbene il lavoro sia stato condotto su topi maschi, indica NF-κB negli astrociti come un bersaglio promettente per terapie mirate a migliorare il recupero dopo lesione cerebrale traumatica e suggerisce che i livelli ematici di molecole come osteopontina e lipocalina-2 potrebbero un giorno aiutare i clinici a monitorare quanto bene sta guarendo il cervello del paziente.
Citazione: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Parole chiave: lesione cerebrale traumatica, astrociti, neuroinfiammazione, formazione della cicatrice cerebrale, NF-kappa B