Clear Sky Science · it
Un modello di organoidi cerebrali umani per l’encefalite da virus West Nile mostra immunocompetenza innata
Perché contano i piccoli cervelli coltivati in laboratorio
Il virus West Nile è un’infezione trasmessa dalle zanzare che può invadere il cervello e causare encefalite, un’infiammazione potenzialmente letale che uccide alcuni pazienti e lascia molti sopravvissuti con problemi di memoria e di movimento a lungo termine. Eppure i medici non dispongono ancora di un antivirale specifico né di un vaccino per gli esseri umani. Un motivo importante è che è stato difficile studiare cosa faccia il virus all’interno del cervello umano. In questo lavoro, i ricercatori utilizzano “organoidi cerebrali” — piccoli ammassi tridimensionali di cellule cerebrali umane cresciute a partire da cellule staminali — per costruire un modello di laboratorio realistico dell’encefalite da West Nile e osservare come le cellule cerebrali reagiscono.
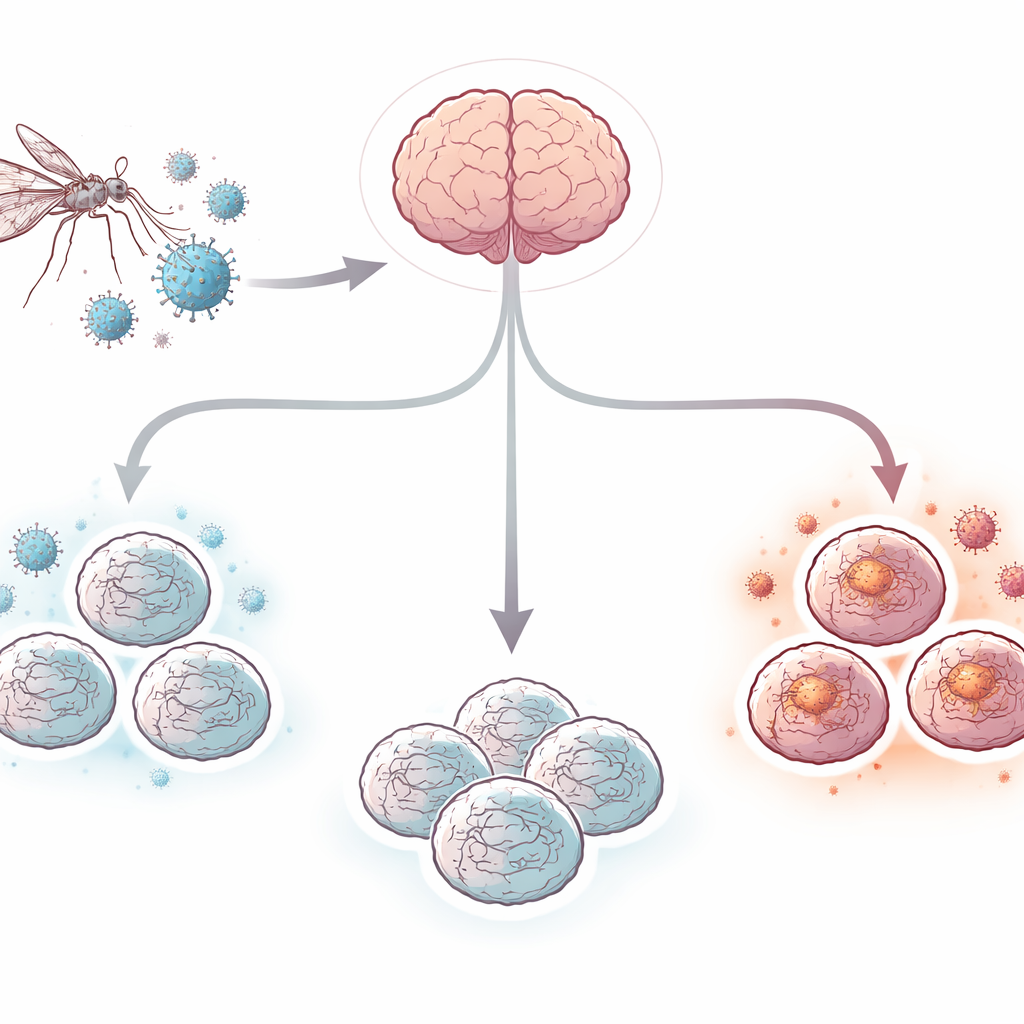
Costruire mini cervelli umani in una piastra
Il team ha iniziato con cellule staminali pluripotenti indotte umane, che possono essere indirizzate a diventare diversi tipi cellulari. Seguendo un protocollo a tappe, hanno coltivato queste cellule per circa 100 giorni fino a ottenere organoidi cerebrali delle dimensioni di un pisello che imitano caratteristiche chiave dello strato esterno del cervello umano. Questi mini‑cervelli contenevano reti di cellule nervose (neuroni), cellule di supporto chiamate astrociti e cellule immunitarie residenti chiamate microglia. Alcuni organoidi hanno inoltre formato strutture somiglianti al plesso coroideo, il tessuto che produce il liquido cerebrospinale e costituisce una barriera importante tra il sangue e il cervello. Questa mescolanza di tipi cellulari ha creato un ambiente più realistico rispetto alle tradizionali colture cellulari piatte.
Come si comporta il virus West Nile nei mini‑cervelli
Quando gli organoidi sono stati esposti a una bassa dose di virus West Nile, l’infezione si è instaurata con forza ma non in modo uniforme. Le misurazioni del virus rilasciato nel liquido circostante hanno mostrato che alcuni organoidi raggiungevano rapidamente un picco nei primi giorni e poi tendevano a calare; altri aumentavano più lentamente e restavano infettati fino a quattro settimane. In diversi organoidi con picco precoce, i livelli virali sono poi scesi al di sotto del limite di rilevazione, suggerendo che i mini‑cervelli fossero in grado di eliminare l’infezione autonomamente. È importante notare che gli organoidi non si disintegravano né mostravano danni visibili massivi, il che indica che il sistema può modellare sia l’infezione acuta sia quella più prolungata senza semplicemente crollare.
Dove il virus colpisce e chi risponde
Le immagini al microscopio hanno rivelato che il virus West Nile non si diffondeva in modo uniforme nei mini‑cervelli. Invece, le proteine virali comparivano in piccoli ammassi vicino alle regioni esterne simili alla corteccia, ricche di neuroni e astrociti. Il materiale virale tendeva ad accumularsi intorno ai nuclei cellulari, coerente con un’infezione attiva all’interno di queste cellule. Al contrario, le microglia erano distribuite negli strati più profondi e risultavano in gran parte assenti dalle aree positive per il virus, suggerendo che non fossero i principali bersagli precoci dell’infezione e non si raggruppassero sulle zone infettate in questo modello. Questo schema rispecchia i riscontri delle autopsie sui pazienti e degli studi animali, dove i neuroni sono bersagli primari ma altre cellule cerebrali modulano l’infiammazione circostante.
Segnali chimici dell’infiammazione cerebrale
Per capire come reagiscono questi piccoli cervelli, i ricercatori hanno misurato dozzine di molecole immunitarie e legate al danno secrete nel fluido di coltura nel tempo. Hanno osservato un’onda coordinata di segnali associati all’infiammazione cerebrale. All’inizio, la chemochina CXCL10 è aumentata bruscamente, seguita da altri segnali di richiamo come CCL2, CCL17 e CX3CL1 che normalmente reclutano cellule immunitarie circolanti nel cervello. Anche messaggeri infiammatori classici — tra cui IL‑6, TNF‑α e IL‑18 — sono aumentati, così come marcatori regolatori e legati al danno come l’antagonista del recettore IL‑1, sTREM‑1, sRAGE e il fattore di supporto neuronale BDNF. Molti di questi segnali sono rimasti elevati anche nelle fasi più tardive dell’infezione, suggerendo come l’infiammazione persistente possa contribuire ai sintomi duraturi anche dopo il controllo del virus.
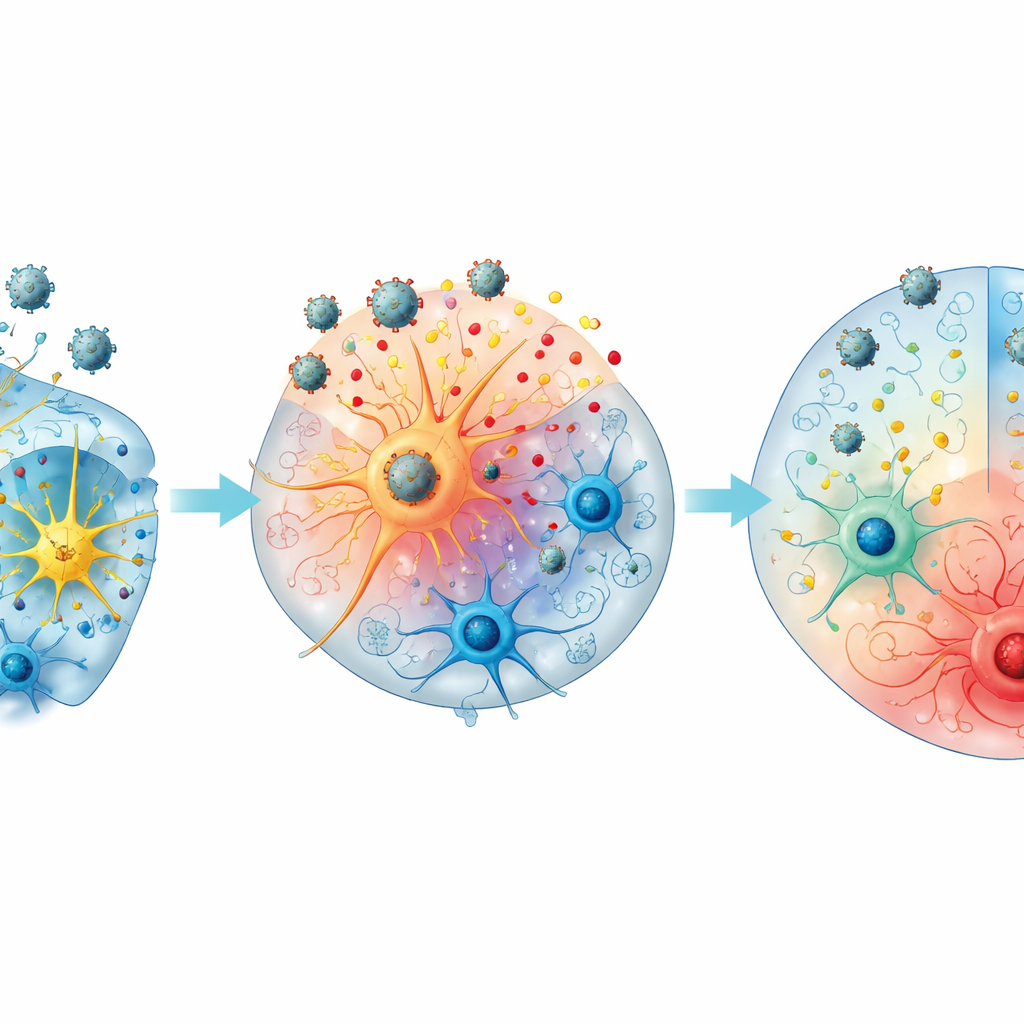
Percorsi divergenti: eliminare o sostenere l’infezione
Il team ha notato che gli organoidi seguivano due percorsi principali. I mini‑cervelli “Tipo A”, che raggiungevano il picco virale precocemente, erano più propensi a perdere successivamente il virus rilevabile e mostravano picchi più netti in alcuni segnali infiammatori e regolatori, tra cui CXCL10, l’antagonista del recettore IL‑1 e sTREM‑1. Gli organoidi “Tipo B”, con picchi più tardivi, mantenevano più spesso alti livelli virali e presentavano relativamente maggiori quantità di IL‑18 e di alcuni marcatori di danno, suggerendo una tendenza verso un’infiammazione prolungata. Gli organoidi che sviluppavano strutture simili al plesso coroideo tendevano a produrre ancora di più alcuni segnali come IL‑6, CXCL10, CX3CL1 e β‑NGF, indicando un possibile ruolo di questo tessuto barriera nel modulare la risposta cerebrale all’infezione.
Cosa significa per i pazienti
Dimostrando che organoidi cerebrali umani possono essere infettati dal virus West Nile, montare risposte immunitarie complesse e talvolta persino eliminare il virus, questo studio stabilisce un potente sostituto del cervello umano. Per il lettore non specialistico, il punto chiave è che gli scienziati possono ora osservare in tempo reale come un tessuto cerebrale simile a quello umano contrasti un virus trasmesso dalle zanzare, senza sperimentare direttamente sui pazienti. Questo modello dovrebbe aiutare a capire perché alcune infezioni si risolvono mentre altre persistono, come le cellule cerebrali locali contribuiscano sia alla protezione sia al danno, e quali vie di segnalazione potrebbero essere mirate per prevenire problemi neurologici a lungo termine. In futuro, sistemi di organoidi simili potrebbero essere impiegati per testare antivirali, studiare vaccini e investigare altri virus che infettano il cervello in condizioni controllate.
Citazione: Steffen, J.F., Widerspick, L., Jansen, S. et al. A human cerebral organoid model of West Nile virus encephalitis shows innate immunocompetency. Nat Commun 17, 2318 (2026). https://doi.org/10.1038/s41467-026-70281-x
Parole chiave: virus West Nile, organoidi cerebrali, encefalite virale, infiammazione cerebrale, virus neurotrofici