Clear Sky Science · it
NAA40 e NAC cooperano nell'acetilazione co-traduzionale degli istoni negli esseri umani
Come le cellule affinano i loro interruttori genetici
All'interno di ogni cellula umana, le proteine appena sintetizzate vengono modificate chimicamente mentre emergono dalle macchine che le producono, i ribosomi. Questi piccoli aggiustamenti possono determinare dove va una proteina, quanto a lungo vive e persino come vengono attivati o disattivati i nostri geni. Questo articolo si concentra su una proteina molto specifica chiamata NAA40 e su un complesso ausiliario denominato NAC, rivelando come cooperino sul ribosoma per modificare le proteine istoniche — i rocchetti attorno a cui il DNA è avvolto — influenzando così l'attività genica e, potenzialmente, lo sviluppo del cancro.
Un piccolo cappuccio che modifica il comportamento degli istoni
Molte proteine umane ricevono una piccola modifica chimica all'estremità iniziale, un processo noto come acetilazione N-terminale. Gli istoni H2A e H4, che aiutano a impaccare il DNA in cromatina, sono quasi sempre modificati in questo modo. NAA40 è insolito tra gli enzimi perché si specializza quasi esclusivamente nell'aggiungere questo cappuccio a questi istoni mentre vengono prodotti. Questo marcatore acetile compete con altri segni chimici, come fosforilazione e metilazione, sulla stessa regione degli istoni, quindi l'azione o meno di NAA40 può modificare il grado di compattamento del DNA e la regolazione genica. È importante sottolineare che livelli alterati di NAA40 sono stati collegati a diversi tumori, rendendolo un bersaglio promettente per nuove terapie.
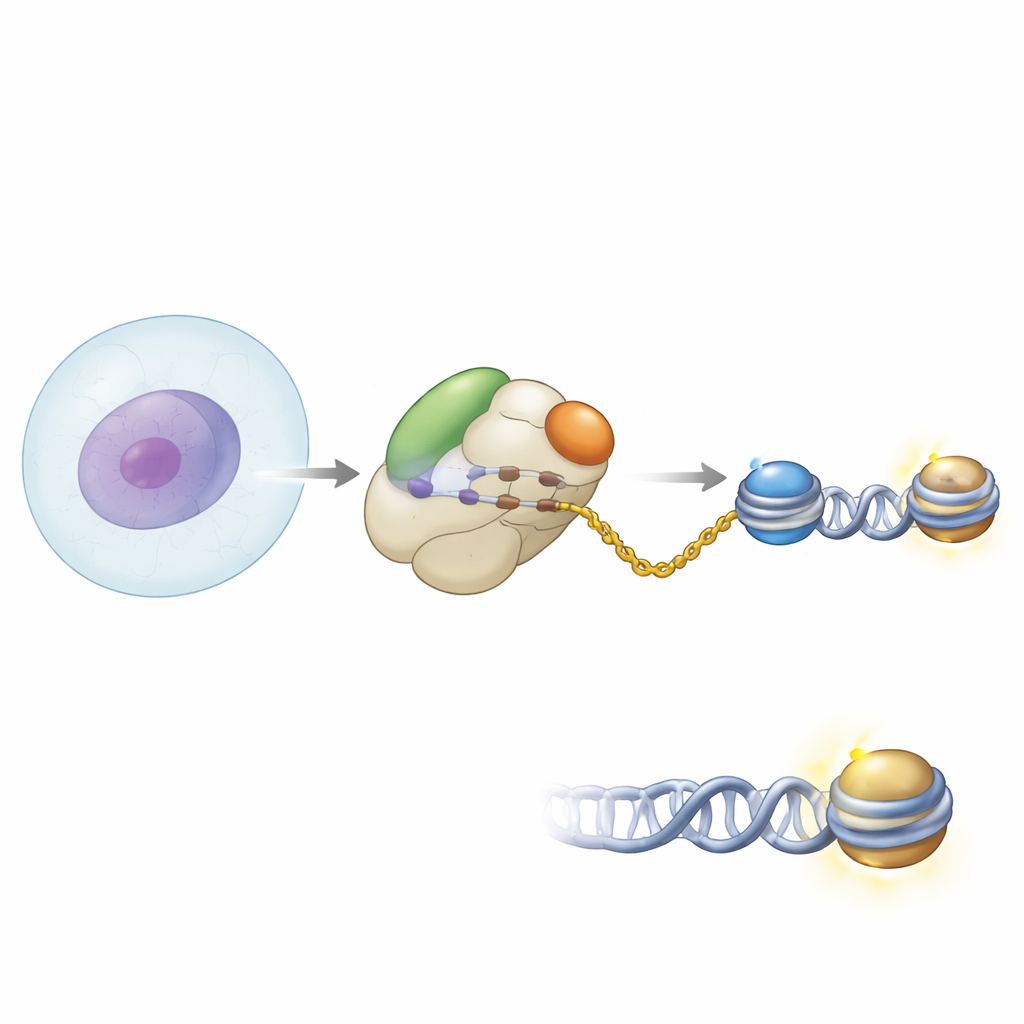
Una collaborazione alla porta della fabbrica delle proteine
Gli autori hanno usato metodi biochimici e microscopia crio-elettronica ad alta risoluzione per osservare come NAA40 sia posizionato sul ribosoma umano. Hanno scoperto che NAA40 si trova proprio all'uscita del tunnel dove emergono le catene proteiche neosintetizzate. Lì non agisce da solo: si lega accanto al complesso associato al polipeptide nascente, o NAC, un comune assistente legato al ribosoma che sorveglia le nuove proteine mentre escono. I fotogrammi strutturali hanno mostrato NAA40 ancorato al ribosoma da un segmento elicoidale carico positivamente alla sua estremità iniziale, mentre NAC è fissato tramite una delle sue subunità alla superficie ribosomale. Un dominio flessibile di NAC si estende per contattare NAA40, fungendo di fatto da ponte che collega l'enzima al ribosoma.
Perché NAC è necessario per il controllo degli istoni
Per verificare l'importanza di questa collaborazione, i ricercatori hanno ricostituito queste interazioni con componenti purificati in provetta. Hanno osservato che NAA40 da solo si lega ai ribosomi in modo debole, ma quando è presente NAC il legame al ribosoma diventa molto più forte. Se hanno rimosso una specifica regione “UBA” di NAC che contatta NAA40, questo aumento del legame scompare. Nelle cellule umane, l'eliminazione di NAC ha portato a una riduzione dell'acetilazione di H4 dipendente da NAA40 e a un corrispondente aumento di un marcatore concorrente di fosforilazione sulla stessa coda istonica. Questo cambiamento avveniva senza alterare la quantità o la localizzazione di NAA40 stesso, indicando che il ruolo principale di NAC è reclutare e posizionare correttamente NAA40 sui ribosomi traducenti in modo che gli istoni possano essere modificati in modo efficiente mentre vengono sintetizzati.
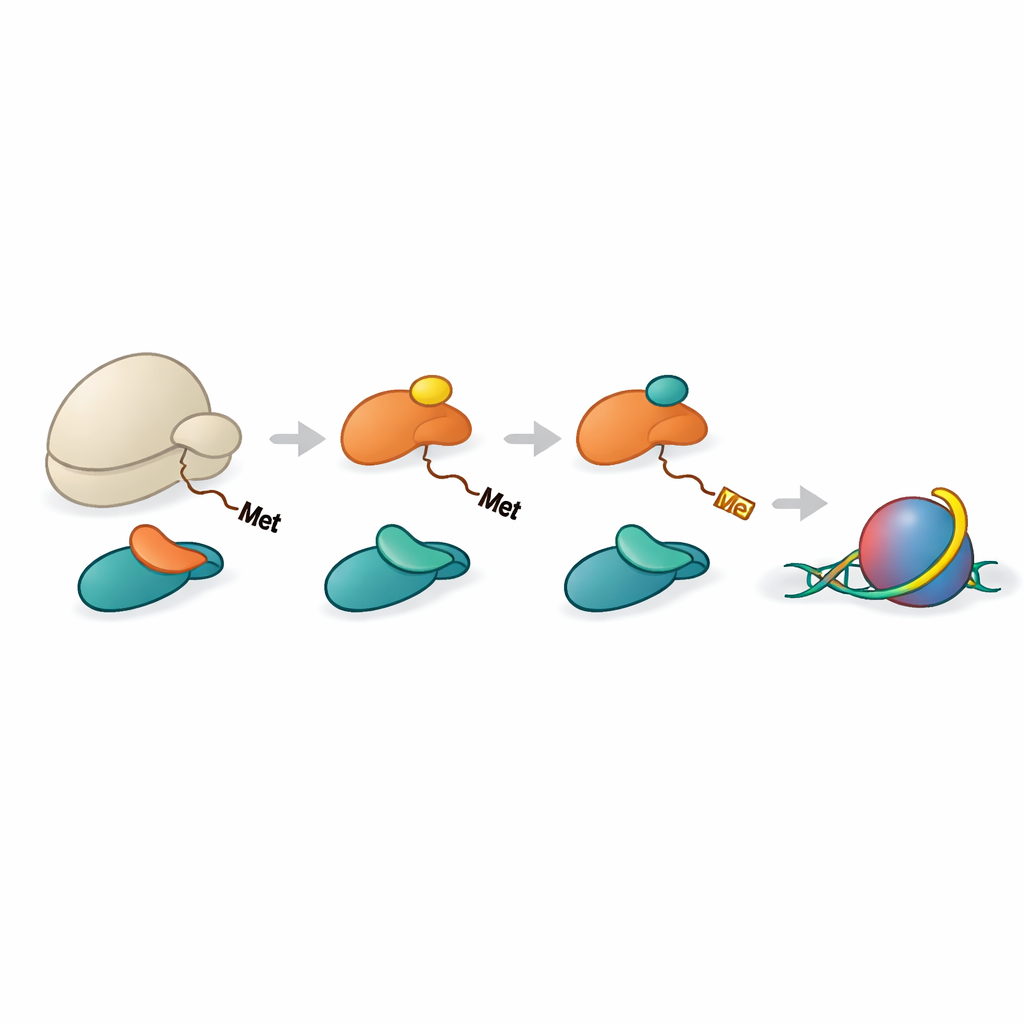
Una linea di assemblaggio coordinata per la lavorazione degli istoni
Gli istoni H2A e H4 devono prima perdere il loro amminoacido metionina iniziale prima che NAA40 possa riconoscerli. Un altro enzima, METAP1, esegue questo taglio. Il gruppo ha mostrato che NAC può aiutare a mettere insieme METAP1 e NAA40 sul ribosoma, formando una stazione multi-enzimatica all'uscita del peptide. Strutture ad alta risoluzione di complessi ricostituiti hanno rivelato METAP1 e NAA40 legati fianco a fianco sul ribosoma, con i loro siti attivi posizionati a distanze quasi uguali dall'uscita del tunnel. Questa geometria implica che, non appena una coda istonica si estende di una dozzina circa di amminoacidi oltre il ribosoma, METAP1 può rimuovere la metionina iniziale e NAA40 può immediatamente aggiungere il cappuccio acetile, minimizzando qualsiasi ritardo tra i due passaggi.
Implicazioni per il controllo genico e il cancro
Complessivamente, lo studio mostra che NAA40 non vaga semplicemente nella cellula alla ricerca di istoni da modificare. Piuttosto, è ancorato al ribosoma da NAC, diventando parte di una stazione di lavorazione organizzata che prepara gli istoni nel momento stesso in cui vengono sintetizzati. Accoppiando strettamente la rimozione della metionina e l'aggiunta dell'acetile, la cellula garantisce che gli istoni H2A, H4 e la variante legata al danno al DNA H2A.X ricevano rapidamente un marcatore acetile in grado di plasmare la struttura della cromatina e l'espressione genica. Poiché le interruzioni in questo primo passaggio di marcatura degli istoni possono favorire la crescita cancerosa, comprendere l'esatta disposizione di NAA40, NAC e METAP1 sul ribosoma fornisce un progetto strutturale che potrebbe guidare la progettazione di farmaci mirati a modulare questo punto critico del controllo epigenetico.
Citazione: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Parole chiave: acetilazione degli istoni, NAA40, ribosoma, complesso associato al polipeptide nascente, regolazione epigenetica