Clear Sky Science · it
Una transizione dipendente dal ciclo cellulare da acetilazione a fosforilazione regola la maturazione tempestiva del centrosoma
Tenere al sicuro il nostro carico genetico
Ogni volta che una cellula del nostro organismo si divide, deve distribuire il suo DNA con precisione estrema. Quando questo processo fallisce, le cellule possono perdere o acquisire cromosomi, una condizione pericolosa legata al cancro e ad altre patologie. Questo studio scopre un dispositivo molecolare di temporizzazione che aiuta le cellule a costruire le piccole strutture necessarie a separare correttamente i cromosomi, rivelando un possibile punto debole che future terapie antitumorali potrebbero sfruttare.
I piccoli snodi del traffico cellulare
Al centro di ogni cellula in divisione si trovano i centrosomi, piccole strutture che fungono da snodi per le fibre che separano i cromosomi. Prima che la cellula entri in divisione, questi snodi devono «maturare»: si arricchiscono di proteine ausiliarie e diventano potenti organizzatori dei microtubuli, le fibre dinamiche che formano il fuso di divisione. Se questa maturazione avviene troppo presto, troppo tardi o non avviene affatto, i cromosomi possono essere distribuiti in modo errato, portando a cellule con un numero anomalo di cromosomi. Capire come le cellule attivino i centrosomi al momento giusto è da tempo una questione centrale nella biologia cellulare.
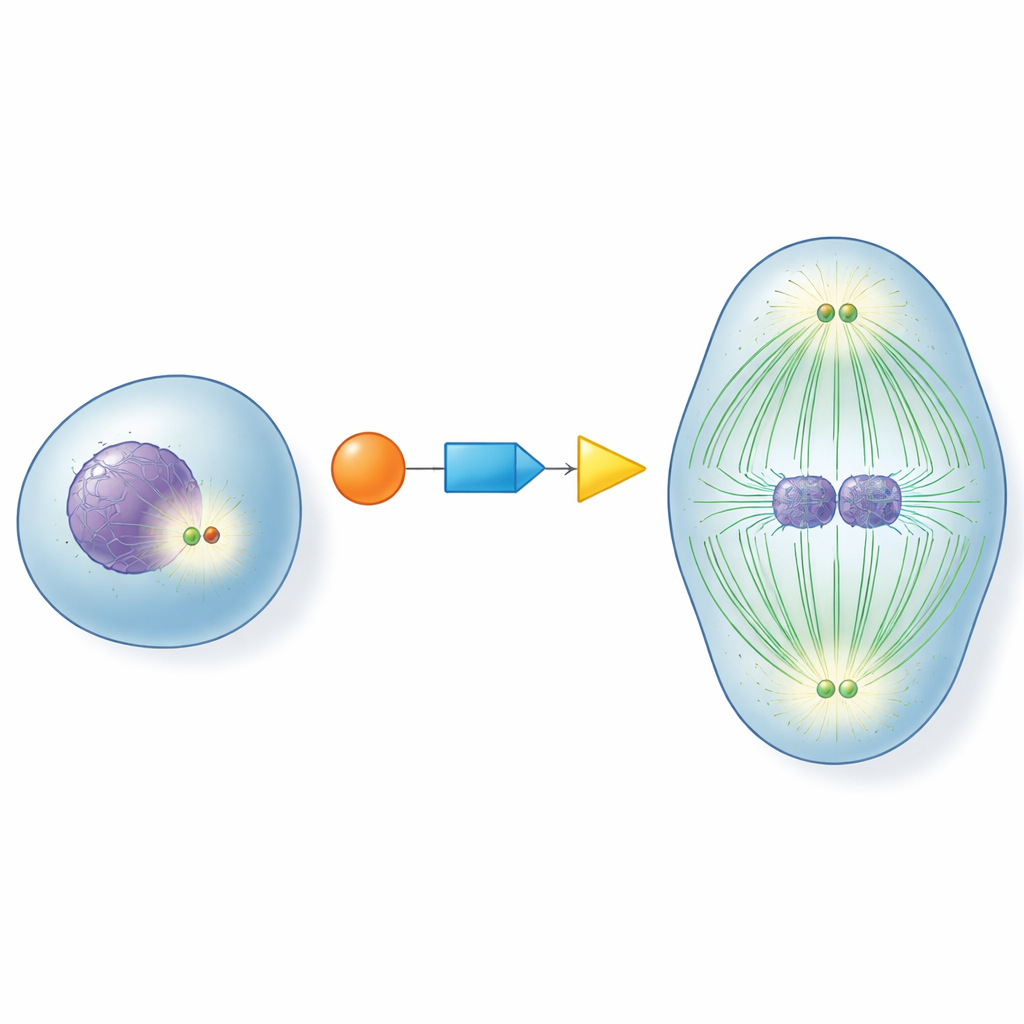
Un relais molecolare per la sincronizzazione perfetta
Gli autori si sono concentrati su tre proteine chiave che agiscono insieme come un relais: CDK1, un regolatore maestro del ciclo cellulare; RNF40, nota in precedenza soprattutto per modificare le proteine che impacchettano il DNA; e PLK1, un importante motore della divisione cellulare. Hanno scoperto che RNF40 è presente fisicamente ai centrosomi durante tutto il ciclo cellulare e si lega direttamente a PLK1. Avvicinandosi alla divisione, CDK1 marca chimicamente RNF40 in due punti specifici, rendendo RNF40 un sito di ancoraggio più favorevole per PLK1. Questa catena CDK1–RNF40–PLK1 assicura che PLK1 arrivi ai centrosomi proprio nella fase tardiva di preparazione alla divisione, innescando una solida maturazione del centrosoma, la crescita dei microtubuli e l’assemblaggio di un fuso bipolare ben formato.
Un interruttore proteico che cambia forma
È interessante notare che RNF40 non accetta sempre questi marcatori attivatori. Nelle fasi non divisionali e durante la duplicazione del DNA, RNF40 porta una diversa modifica chimica—gruppi acetile—su due posizioni vicine. Questi marcatori di acetilazione sono aggiunti da un enzima chiamato PCAF e rimossi successivamente da un partner deacetilante, HDAC1. La versione acetilata di RNF40 resiste alla modifica da parte di CDK1, bloccando di fatto il passaggio successivo del relais. Quando le cellule entrano nell’ultima fase pre-divisionale, HDAC1 cancella gradualmente i segni di acetilazione, permettendo a CDK1 di aggiungere gruppi fosfato al loro posto. Questo passaggio attentamente temporizzato dall’acetilazione alla fosforilazione trasforma RNF40 da uno stato di «standby» a uno stato «attivo», pronto a reclutare PLK1 e ad alimentare il centrosoma.
Cosa succede quando la temporizzazione fallisce
Per valutare l’importanza di questo interruttore, i ricercatori hanno ingegnerizzato cellule in cui RNF40 non poteva più essere fosforilata, o in cui era forzata a rimanere in uno stato che imita l’acetilazione. In entrambi i casi, PLK1 non si accumulò correttamente ai centrosomi. Queste cellule mostrarono una crescita ridotta dei microtubuli dai centrosomi, fusi malformati e cromosomi mal allineati. Molte finirono con cromosomi in eccesso o mancanti—una condizione anomala nota come aneuploidia—e alcune divennero binucleate, segni di errori catastrofici nella divisione. Nei modelli tumorali, le cellule bloccate nello stato di RNF40 «acetilato» formarono tumori più piccoli nei topi e risultarono più sensibili ai comuni farmaci chemioterapici usati nel trattamento del carcinoma colorettale, suggerendo che perturbare questo interruttore può rallentare la crescita tumorale.
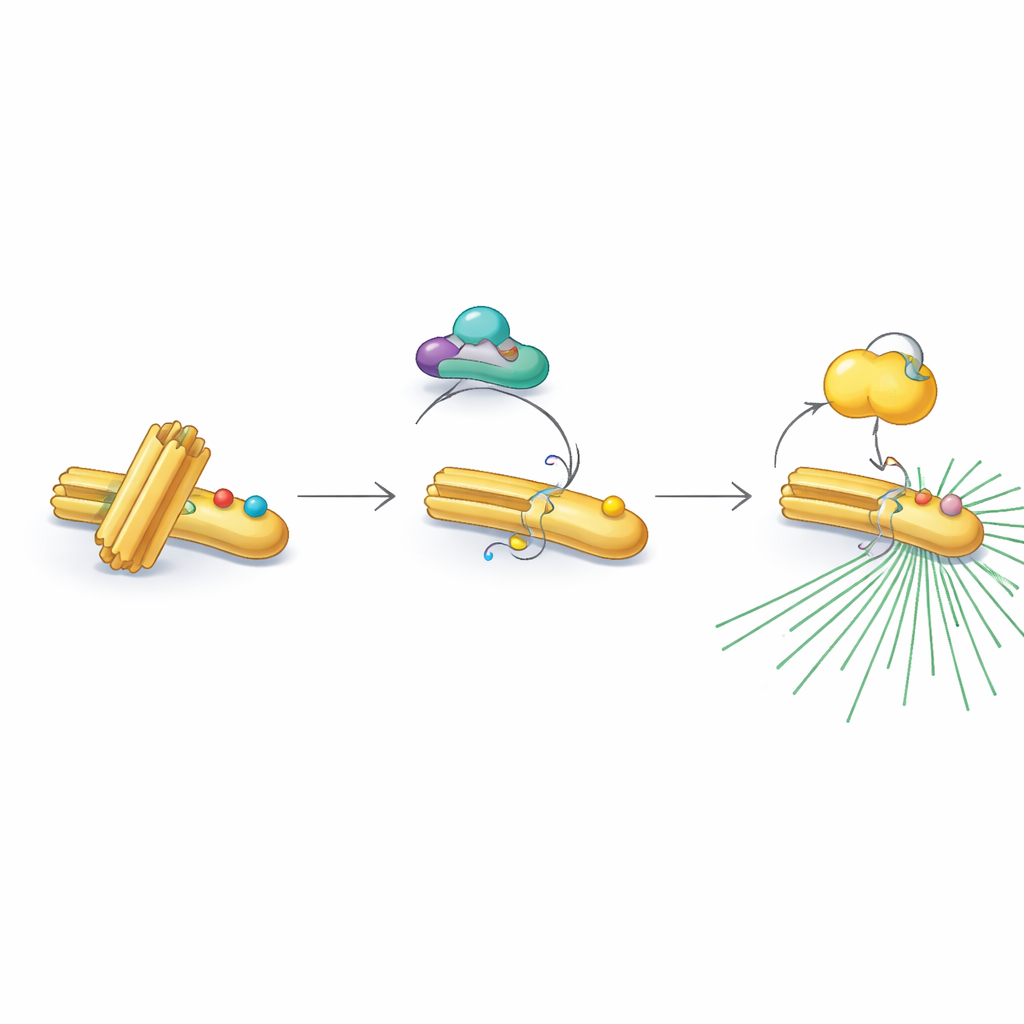
Connessioni con il cancro umano e possibilità future
Il team ha anche esaminato dati di pazienti e campioni tumorali. Hanno trovato che RNF40 è spesso abbondante in modo anomalo nei carcinomi colorettali e che alcune mutazioni associate al cancro vicino ai suoi siti di modifica disturbano la sua fosforilazione, compromettendo la corretta funzione del centrosoma. Queste osservazioni collegano il meccanismo di temporizzazione descritto direttamente alla malattia umana. Identificando una proteina specifica che coordina quando i centrosomi maturano e come i cromosomi vengono separati, lo studio mette in luce un «nodo» di segnalazione che potrebbe essere bersaglio per spingere le cellule tumorali in rapida divisione verso errori letali nella divisione, lasciando meno colpite le cellule sane.
Una nuova leva per la divisione cellulare fedele
Per i non specialisti, il messaggio chiave è che le cellule si affidano a un interruttore chimico finemente regolato su un’unica proteina, RNF40, per decidere esattamente quando attivare la macchina che separa i cromosomi. Questa transizione da acetilazione a fosforilazione si comporta come un semaforo a un incrocio trafficato, che diventa verde solo quando la cellula è davvero pronta a dividersi. Quando il semaforo si guasta, le cellule inciampano nella divisione, accumulano errori genetici e possono trasformarsi in cellule tumorali. Comprendere e controllare questo interruttore potrebbe aprire nuove strade per trattamenti che destabilizzino selettivamente le cellule cancerose sabotando la loro capacità di dividersi in modo corretto.
Citazione: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Parole chiave: maturazione del centrosoma, divisione cellulare, instabilità cromosomica, segnalazione PLK1, carcinoma colorettale