Clear Sky Science · it
Ripristinare la disregolazione sinaptica postnatale precoce salva la degenerazione dei motoneuroni in un modello murino dell’Atrofia Muscolare Spinale e Bulbare
Perché piccole alterazioni precoci possono contare per la debolezza muscolare futura
L’atrofia muscolare spinale e bulbare (SBMA) è una rara condizione ereditaria in cui gli adulti, generalmente uomini, perdono progressivamente forza negli arti, nel tronco e nella gola. I sintomi compaiono a metà età, ma problemi sottili iniziano molto prima. Questo studio pone una domanda sorprendente: potrebbero eventi brevi nei primi giorni dopo la nascita predisporre silenziosamente alla perdita di cellule nervose decenni dopo—e correggere quei difetti precoci potrebbe proteggere il movimento?
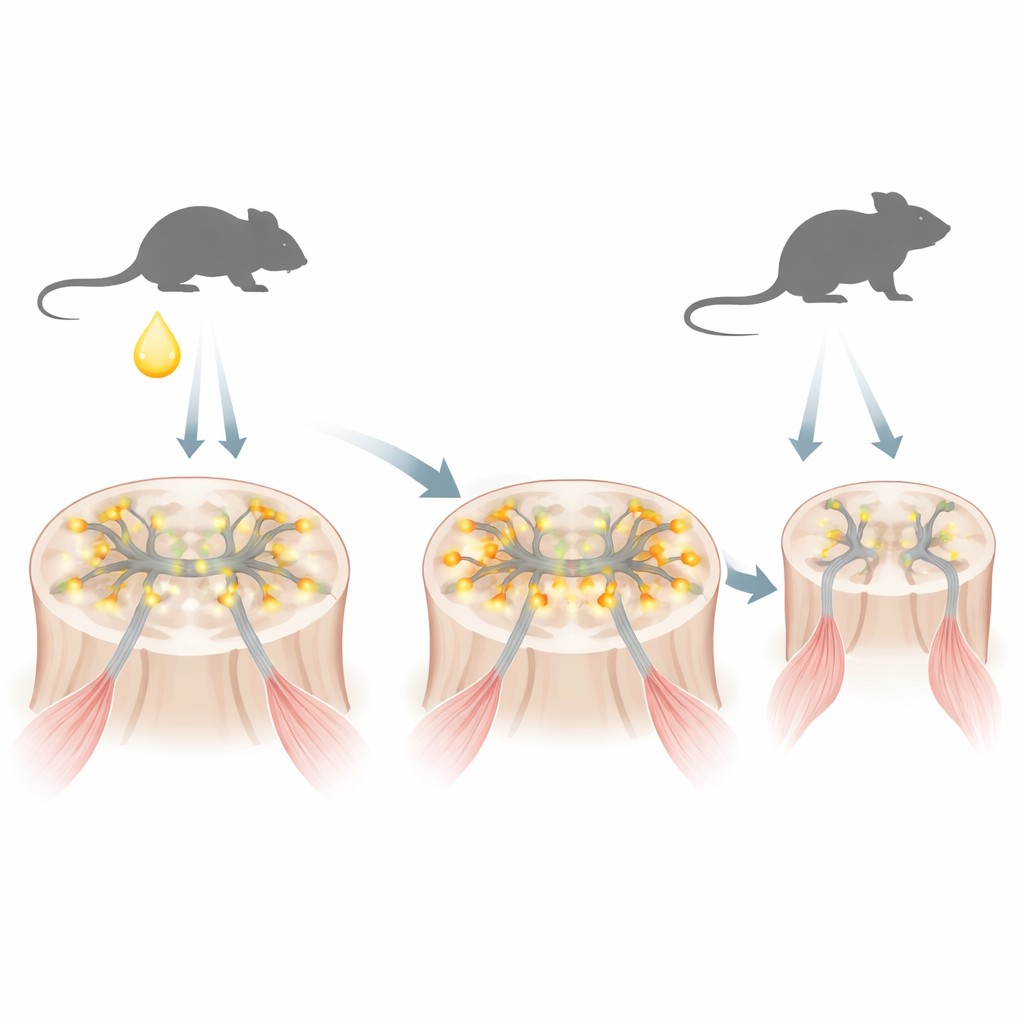
Una malattia radicata in un interruttore sensibile agli ormoni
La SBMA è causata da una versione alterata del recettore degli androgeni, una proteina che rileva ormoni maschili come il testosterone. Il recettore mutato porta una sequenza eccessivamente lunga dell’amminoacido glutammina. In un modello murino che imita la malattia umana, gli autori hanno osservato che subito dopo la nascita, quando il testosterone aumenta brevemente nei neonati maschi, questo recettore mutato si accumula rapidamente all’interno dei nuclei dei motoneuroni—le cellule nervose che controllano i muscoli. In questa fase precoce la proteina non si è ancora aggregata nelle grandi inclusioni tipicamente associate alla neurodegenerazione, ma sta già modificando quali geni vengono attivati o disattivati.
Sovraccarico sinaptico precoce e motoneuroni irrequieti
Con il sequenziamento dell’RNA a livello genomico delle regioni spinali di topi neonati, il gruppo ha scoperto che molti geni coinvolti nelle sinapsi eccitatorie—i punti di contatto in cui le cellule nervose si segnalano a vicenda—erano insolitamente attivi. Molti di questi geni codificano recettori del glutammato, che rendono i neuroni più propensi a entrare in attività elettrica. Il gruppo ha fatto risalire questo schema a una disfunzione di REST, una proteina “freno” maestro che normalmente mantiene sotto stretto controllo questi geni sinaptici durante lo sviluppo. Nei topi SBMA e nei motoneuroni derivati da cellule staminali pluripotenti indotte di pazienti, l’attività di REST era indebolita e veniva favorita una forma tronca chiamata REST4, sollevando il freno e potenziando i geni delle sinapsi glutamatergiche. Coerentemente con ciò, i motoneuroni neonatali SBMA mostravano livelli più elevati di c-Fos, un marcatore di attività recente, e i motoneuroni umani derivati da pazienti presentavano esplosioni di calcio più forti e più frequenti, segni di ipereccitabilità.
Un trattamento precoce e breve che modifica il corso della vita
Gli sperimentatori si sono quindi chiesti se ridurre il recettore mutato o ripristinare il freno REST solo durante questa finestra neonatale potesse cambiare il decorso a lungo termine della malattia. Hanno somministrato oligonucleotidi antisenso—brevi filamenti di materiale genetico modificato—nel fluido che circonda cervello e midollo spinale di topi SBMA di un giorno di vita. Un tipo di oligonucleotide abbassava temporaneamente sia il recettore degli androgeni mutato sia quello normale nel sistema nervoso centrale. Un secondo tipo orientava lo splicing di REST lontano da REST4 e di nuovo verso REST a lunghezza intera, reprimendo così i geni sinaptici. Sorprendentemente, sebbene questi trattamenti fossero somministrati una sola volta e i loro effetti molecolari diretti si attenuassero nel giro di poche settimane, i topi vissero più a lungo, camminarono meglio sulla rotarod e mantennero una presa più forte in età avanzata. I loro motoneuroni e le fibre muscolari erano meno atrofiche, e i marcatori precoci di iperattività neuronale e le successive impennate di neuropeptidi legati allo stress risultarono attenuati.
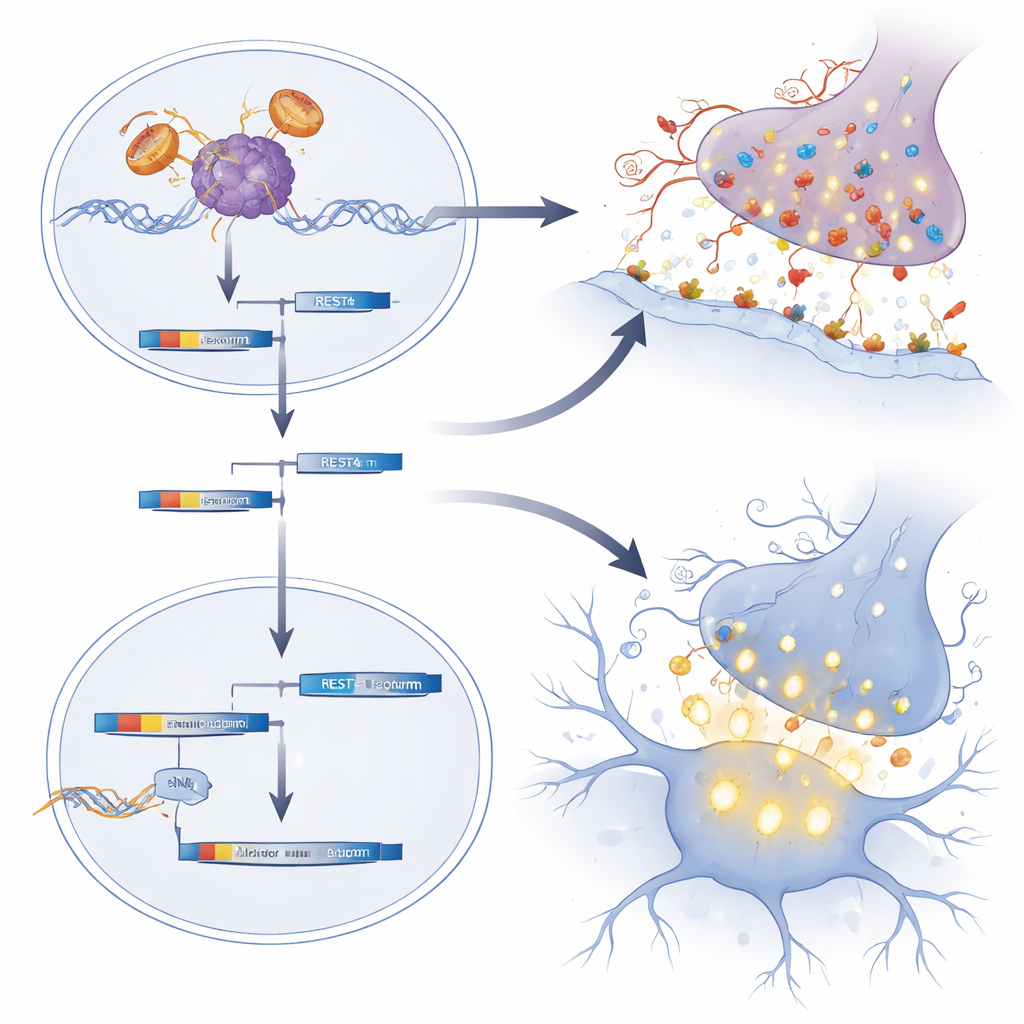
Come gli ormoni precoci e la modulazione genica plasmano la vulnerabilità
Il lavoro mette inoltre in evidenza la particolare vulnerabilità dei motoneuroni alla breve esplosione di testosterone che si verifica poco dopo la nascita. Quando ai neonati SBMA fu somministrato testosterone aggiuntivo, la loro debolezza e perdita di peso successive peggiorarono, e i programmi genici legati alla corretta maturazione dei motoneuroni furono ulteriormente disturbati. I topi normali non mostrarono questo danno, sottolineando che è la combinazione tra il recettore mutato e il picco ormonale a risultare dannosa. Nel complesso, i risultati suggeriscono che nella SBMA un eccesso di sinapsi eccitatorie e motoneuroni eccessivamente eccitabili precocemente nella vita spingono lentamente il sistema verso il collasso, anche se i sintomi evidenti non emergono fino all’età adulta media.
Cosa significa questo per le persone che vivono con SBMA
Per un non specialista, il messaggio chiave è che la SBMA può essere, in parte, una malattia di sinapsi temporaneamente disordinate e mal programmate nei primi giorni dopo la nascita. Un sensore ormonale difettoso spinge i motoneuroni in via di sviluppo in uno stato di iperattivazione, e questo stress precoce contribuisce alla loro degenerazione anni dopo. La notizia incoraggiante è che medicine genetiche progettate con cura, somministrate durante queste finestre critiche, possono riequilibrare i segnali nei motoneuroni, calmare la loro iperattività e ritardare o ridurre in modo significativo la perdita di cellule nervose nei modelli animali. Sebbene tradurre tali interventi in epoca neonatale nell’uomo richiederà grande cautela e ulteriori studi, questi risultati indicano nuove strategie che mirano alle radici della SBMA molto prima che compaia la debolezza.
Citazione: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
Parole chiave: atrofia muscolare spinale e bulbare, ipereccitabilità dei motoneuroni, recettore degli androgeni, regolazione sinaptica REST, terapia con oligonucleotidi antisenso