Clear Sky Science · it
Scelta del percorso tra reazioni click e trasferimento acilico guidate da fosfati amminoacilici
Perché il tempo importa nella chimica di tutti i giorni
All'interno di ogni cellula, molecole importanti vengono costruite e modificate in un ordine molto preciso, come i passaggi di una ricetta. Questo ordine stabilisce se una proteina si attiva, si disattiva o cambia conformazione. I chimici vorrebbero imitare questo tipo di programmazione intrinseca usando molecole semplici non viventi in acqua, senza fare affidamento su enzimi o stimoli esterni come luce o variazioni di pH. Questo articolo descrive un sistema di reazione sintetico che fa proprio questo: sfrutta la struttura di piccoli peptidi e una reazione di formazione di legami comune nella “chimica click” per decidere quale passaggio chimico avviene prima e quale deve aspettare il suo turno.
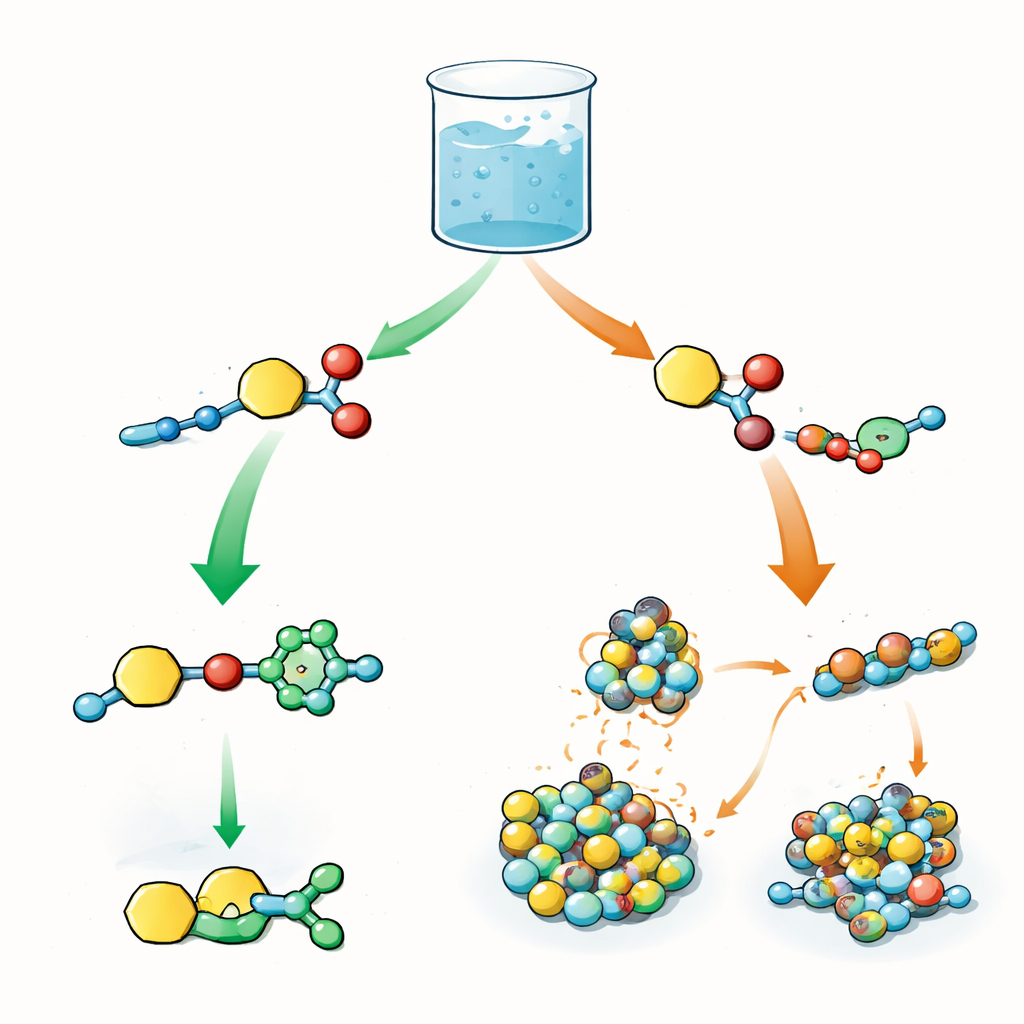
Due reazioni rivali in un unico recipiente
Gli autori progettano un blocco di costruzione centrale che porta due caratteristiche reattive: una capace di trasferire un gruppo acile (un piccolo frammento chimico spesso usato per modificare proteine) e un'altra in grado di subire una reazione click chiamata cicloadizione azide‑alchino catalizzata dal rame. Nello stesso becher, questo blocco viene miscelato con azidi e con brevi peptidi che fungono da nucleofili, cioè che catturano il gruppo acile. In biologia, l'ordine di tali passaggi—attivazione, trasferimento e modifiche successive—controlla il comportamento delle proteine. Qui la domanda è simile: quando entrambe le reazioni sono possibili contemporaneamente, il sistema sceglie prima la click, prima il trasferimento acilico o una miscela di entrambi?
Ossigeno lento, zolfo veloce
Il gruppo studia prima peptidi contenenti tirosina, un amminoacido con una catena laterale a base di ossigeno. In condizioni leggermente basiche, la reazione click procede rapidamente: alchino e azide si uniscono in fretta, mentre il trasferimento acilico sulla catena laterale della tirosina è lento e genera a malapena intermedi rilevabili. Si formano diversi prodotti derivati dalla click e non c'è un chiaro intervallo temporale tra i passaggi. Quando i ricercatori passano alla cisteina, un amminoacido con una catena laterale a base di zolfo, la situazione si ribalta. La cisteina forma rapidamente tioesteri—prodotti acilici legati allo zolfo—che compaiono in alto rendimento molto prima di qualsiasi prodotto della click. Solo dopo molte ore emergono prodotti da click. Questo cambiamento deriva dal fatto che lo zolfo non solo reagisce con maggiore reattività ma si coordina anche agli ioni rame, sequestrando il catalizzatore e «mettendo in pausa» temporaneamente il percorso click.
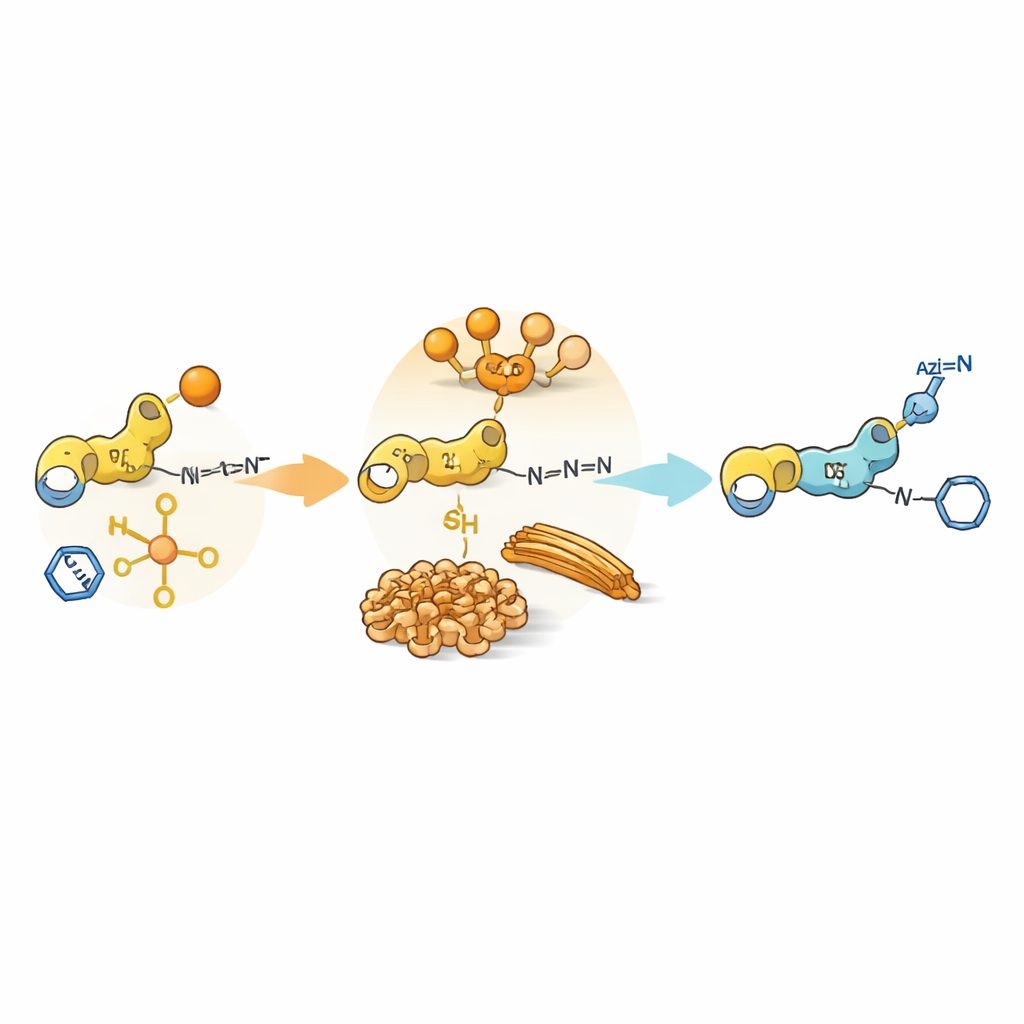
L'auto‑assemblaggio come cancello chimico
Oltre alla semplice reattività, i peptidi stessi possono aggregarsi in strutture più grandi, formando gel morbidi o fibre in acqua. Questi assemblaggi creano minuscoli domini dove alcuni partner sono concentrati e altri esclusi. Per certi dipeptidi contenenti tirosina o cisteina che portano gruppi aromatici aggiuntivi, gli intermedi si autoassemblano in fibrille o particelle dense. All'interno di queste regioni compatte, il trasferimento acilico è favorito perché nucleofilo e donatore di acile stanno uno accanto all'altro, mentre l'azide e il catalizzatore a base di rame rimangono per lo più nella soluzione circostante. Di conseguenza, anche se la reazione click è intrinsecamente veloce in soluzione libera, viene rallentata dalla necessità di raggiungere siti reattivi sepolti. Questo «disallineamento di fase» tra dove vive il catalizzatore e dove si trovano i substrati allunga la vita degli intermedi acilati e ritarda l'insorgenza della chimica click.
Programmare cascate e scelte
Per testare fino a che punto possono spingere questa programmazione intrinseca, gli autori progettano situazioni più complesse. In un caso, un singolo peptide contiene sia cisteina sia tirosina, offrendo due diversi siti di trasferimento acilico. La reazione procede come una cascata in tre passaggi: prima si forma un tioestere sulla cisteina, poi un secondo gruppo acile si trasferisce sulla tirosina e solo dopo questi passaggi compaiono prodotti da click. In un altro set di esperimenti, due azidi differenti—uno flessibile e alifatico, l'altro rigido e aromatico—competono per lo stesso centro reattivo. Sorprendentemente, il sistema preferisce costantemente l'azide alifatico, rivelando che persino la forma e il carattere elettronico dell'azide possono indirizzare quali prodotti prevalgono, mentre il timing del trasferimento acilico resta sotto controllo del peptide.
Cosa significa per i materiali intelligenti futuri
In termini semplici, questo lavoro mostra come sia possibile ospitare più reazioni potenzialmente in competizione nella stessa miscela acquosa semplice e farle avvenire in un ordine prestabilito—senza enzimi, pompe o interruttori esterni. Scegliendo se un peptide porta ossigeno o zolfo, modulando la sua tendenza ad autoassemblarsi e regolando la natura del partner azide, gli autori codificano una sorta di orologio interno in una piccola rete chimica. Trasferimenti acilici iniziali e reversibili creano intermedi di breve durata che influenzano quando e come avviene il passo click robusto e quasi irreversibile. Sequenze programmate di questo tipo potrebbero diventare la base per materiali intelligenti e reti reattive sintetiche che “decidono” il proprio percorso nel tempo, in modo analogo alla chimica finemente temporizzata che opera nelle cellule viventi.
Citazione: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Parole chiave: chimica click, trasferimento acilico, assemblaggio supramolecolare, reti reattive, chimica dei peptidi