Clear Sky Science · it
Mappatura molecolare in DNA-PAINT tramite modello di miscela gaussiana modificato
Vedere il mondo invisibile delle molecole
La biologia moderna si basa sempre più su microscopi in grado di vedere non solo le cellule, ma le singole molecole al loro interno. Tuttavia trasformare la luce debole e intermittente emessa da queste molecole in una «mappa» affidabile delle loro posizioni è sorprendentemente difficile. Questo studio presenta un nuovo metodo computazionale, chiamato G5M, che rende queste mappe molecolari molto più accurate e dettagliate, aiutando gli scienziati a capire come le proteine siano disposte e raggruppate nelle cellule reali, fino a poche miliardesime di metro.
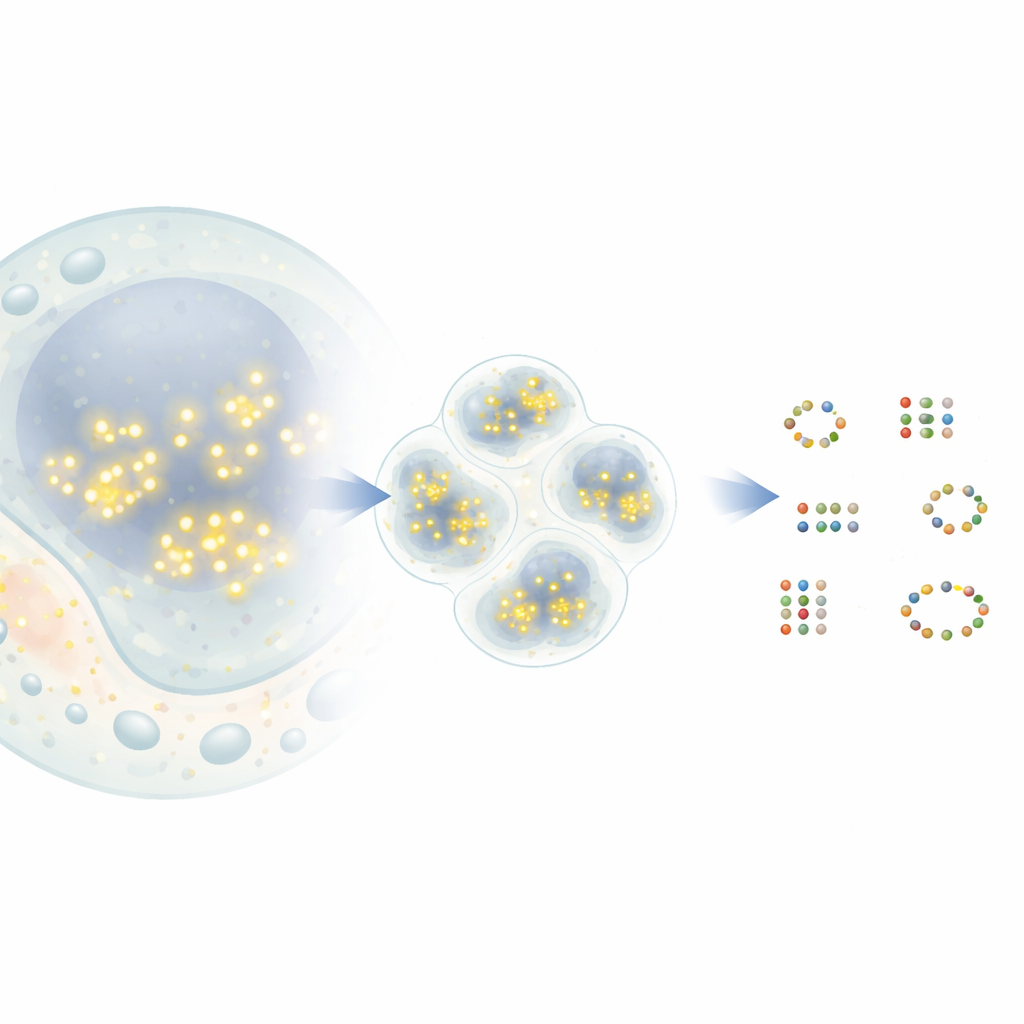
Dai puntini che lampeggiano alle mappe molecolari
In una tecnica di super-risoluzione molto usata, chiamata DNA-PAINT, brevi filamenti di DNA con coloranti fluorescenti si legano temporaneamente a brevi tag di DNA attaccati alle proteine bersaglio. Ogni volta che un colorante si lega, appare come un puntino luminoso al microscopio prima di svanire di nuovo. Nel tempo, molti di questi eventi creano una nube di puntini attorno a ciascuna proteina. In linea di principio, il centro di ogni nube indica la reale posizione di una proteina con precisione nanometrica. In pratica, però, i puntini provenienti da proteine vicine possono sovrapporsi e alcuni provengono da segnali di fondo casuali. Gli strumenti di analisi esistenti spesso fondono vicini troppo ravvicinati in una singola proteina o, al contrario, inventano proteine inesistenti, limitando quante informazioni biologiche si possono estrarre.
Un modo più intelligente per trovare le molecole reali
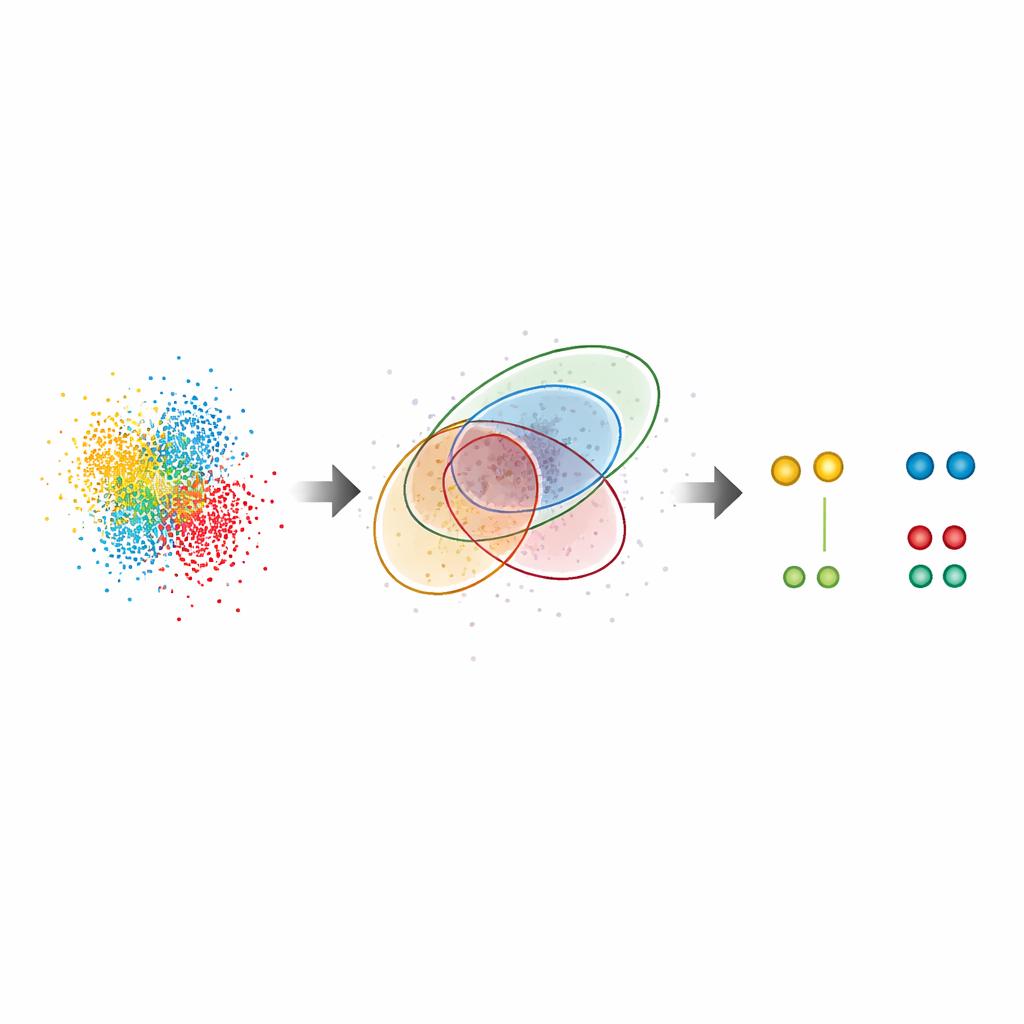
Il nuovo metodo, G5M, considera lo sciame di puntini come una miscela di semplici nubi a forma di campana, ognuna corrispondente a una molecola reale. Anziché raggruppare i puntini vicini solo in base alla densità, G5M usa un modello probabilistico che incorpora ciò che è già noto sull’esperimento: quanto precisamente si possono misurare le posizioni, quanto velocemente i filamenti di DNA si legano e si staccano, e come il microscopio sfoca la luce in due o tre dimensioni. Il metodo valuta quindi diverse possibili spiegazioni—diversi numeri e forme di nubi—e sceglie automaticamente quella che bilancia al meglio adattamento e semplicità. Ulteriori controlli scartano soluzioni sospette, come nubi troppo strette, troppo larghe, basate su troppo pochi puntini o non chiaramente separate l’una dall’altra.
Dimostrazione dell’efficacia in simulazioni e nanostrutture di DNA
Per testare G5M, gli autori hanno prima usato simulazioni realistiche al computer di scene semplici: coppie di molecole e piccole griglie di dodici molecole distanziate solo di pochi nanometri. Rispetto al metodo leader attuale, noto come Gradient Ascent, G5M ha trovato molte più delle molecole che dovrebbero essere visibili al limite teorico di risoluzione, pur segnalando quasi mai molecole inesistenti. In casi chiave, ha recuperato coppie molto vicine ventisette volte più spesso rispetto al metodo precedente e ha migliorato la risoluzione effettiva di oltre la metà. Il team ha poi confermato questi vantaggi sperimentalmente usando strutture di DNA origami—forme di DNA artificiali con siti di docking posti in posizioni precisamente note—dimostrando che G5M poteva contare e localizzare in modo affidabile quasi tutti i siti attesi in un’ampia gamma di condizioni di imaging.
Rivelare pattern nascosti nelle cellule reali
Oltre ai campioni di prova, G5M è stato applicato a sistemi biologici complessi. Nei complessi del poro nucleare, giganteschi portali nel nucleo della cellula, il metodo ha recuperato la nota disposizione ad anello di una proteina chiave, Nup96, anche dove i partner erano separati di soli circa dieci nanometri. Ha trovato quasi il doppio delle coppie proteiche rispetto al metodo standard e ha riprodotto stime indipendenti dell’efficienza di marcatura, suggerendo che non perde molte molecole né ne aggiunge di spurie. Gli autori hanno inoltre analizzato CD20, un recettore di superficie coinvolto nei tumori del sangue e bersaglio di anticorpi terapeutici. In questo caso G5M ha rivelato significativamente più piccoli ammassi (dimeri, trimeri e tetrameri) di CD20 sulla membrana cellulare, chiarendo come un anticorpo antitumorale e formati farmacologici correlati riorganizzino questi recettori. Ha persino migliorato le prestazioni di un approccio ad altissima risoluzione chiamato RESI, che si basa sulla separazione dei segnali in più round di imaging.
Cosa significa per la microscopia futura
Ottenendo informazioni più affidabili dai dati DNA-PAINT esistenti, G5M dimostra che un software migliore da solo può sbloccare nuovi dettagli biologici, senza cambiare microscopi o coloranti. L’algoritmo mantiene le rilevazioni false estremamente basse risolvendo molecole quasi a contatto, cosa essenziale quando si vuole sapere quante proteine sono in un complesso, come sono distanziate o come un farmaco ne altera l’organizzazione. Integrato nella piattaforma open-source Picasso e robusto alle impostazioni tipiche, G5M è destinato a diventare uno strumento standard per trasformare la fluorescenza lampeggiante in mappe molecolari affidabili, aiutando i ricercatori a mappare l’organizzazione su scala nanometrica della vita nelle cellule.
Citazione: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Parole chiave: microscopia a super-risoluzione, DNA-PAINT, mappatura molecolare, oligomerizzazione proteica, algoritmi di analisi delle immagini