Clear Sky Science · it
La multiomica a singola cellula rivela un asse meccanosensibile PIEZO1-IL-33 nell’endotelio che guida la fibrosi polmonare
Perché i polmoni rigidi sono importanti
La fibrosi polmonare è una malattia devastante in cui le alveoli — una volta elastici — si trasformano lentamente in tessuto cicatriziale rigido, rendendo ogni respiro faticoso. Oggi i medici possono solo rallentare la malattia, non fermarla né invertirla. Questo studio propone una domanda apparentemente semplice ma dalle grandi implicazioni: come fanno le cellule che rivestono i vasi sanguigni polmonari a percepire che il tessuto circostante è diventato anormalmente rigido, e come questa sensazione si trasforma in ulteriore cicatrizzazione? Tracciando questa catena di eventi fino alla singola cellula e ai singoli geni, i ricercatori identificano un “interruttore” meccanico nei vasi sanguigni che potrebbe essere bersaglio farmacologico.
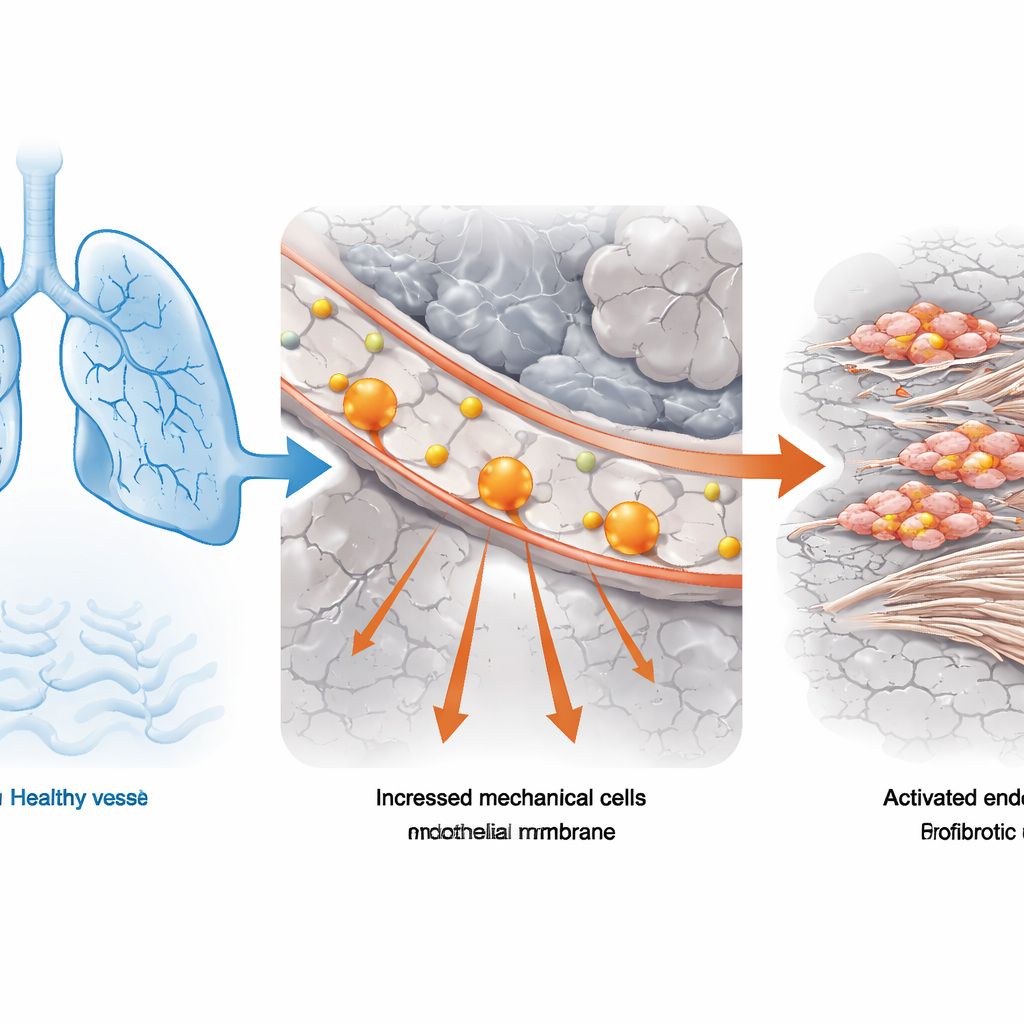
Dai test di funzionalità polmonare alle singole cellule
Il team ha iniziato con tessuto polmonare proveniente da persone con fibrosi polmonare idiopatica, la forma più comune della malattia, e da donatori con polmoni normali. Hanno combinato misure cliniche standard della funzione polmonare (la quantità d’aria che una persona può espirare con forza) con potenti analisi di RNA a singola cellula, che rilevano quali geni sono attivi in migliaia di singole cellule. Utilizzando uno strumento computazionale che collega dati clinici aggregati ai profili a singola cellula, hanno individuato i tipi cellulari più strettamente associati a una funzionalità polmonare gravemente compromessa. Le cellule endoteliali vascolari — che formano il rivestimento interno dei vasi — sono emerse come particolarmente arricchite nei pazienti la cui capacità polmonare era inferiore alla metà del normale. In queste cellule endoteliali, i programmi genici correlati allo “stress meccanico” risultavano costantemente aumentati, suggerendo che forze fisiche anomale contribuissero al problema.
Lo stress meccanico come fattore nascosto
Per verificare se questo legame tra rilevamento dello stress e malattia fosse generale, i ricercatori si sono rivolti a due modelli murini di cicatrizzazione polmonare: uno indotto dal farmaco chemioterapico bleomicina, l’altro dall’esposizione cronica alla polvere di silice, un rischio occupazionale. Applicando metodi a singola cellula a questi polmoni sperimentali, hanno nuovamente trovato che le cellule endoteliali portavano chiare firme di stress meccanico aumentato. In entrambi i modelli, man mano che il tessuto polmonare circostante si ispessiva e irrigidiva, il rivestimento dei vasi sembrava passare a uno stato maladattivo. Questa convergenza tra campioni umani e modelli animali rafforza l’idea che forze fisiche alterate nel polmone, più che solo infiammazione o attività immunitaria, siano centrali per lo sviluppo e la progressione della fibrosi.
Un sensore di pressione con un ruolo critico
Approfondendo, il gruppo ha cercato specifici “meccanosensori” — proteine che convertono l’allungamento fisico in segnali biochimici — che risultassero sovraespressi nelle cellule endoteliali sotto stress. Una proteina canale, chiamata PIEZO1, è emersa ripetutamente come sospetto principale. Sia nei topi sia negli esseri umani con fibrosi, i livelli di PIEZO1 erano marcatamente più alti nelle cellule endoteliali vascolari rispetto ai controlli sani. Quando i ricercatori hanno generato topi in cui PIEZO1 era eliminato solo nell’endotelio, questi animali sono risultati molto più resistenti alla fibrosi polmonare indotta da bleomicina: avevano meno accumulo di collagene, meno cellule attivate produttrici di cicatrice e livelli inferiori di un marcatore chimico di fibrosi. Il blocco farmacologico di PIEZO1 con un inibitore peptidico ha attenuato la cicatrizzazione, mentre la sua attivazione ha peggiorato la fibrosi — a meno che il recettore non fosse assente nelle cellule endoteliali. Nel complesso, questi esperimenti dimostrano che PIEZO1 nelle cellule che rivestono i vasi non è un mero spettatore, ma un motore necessario della malattia.
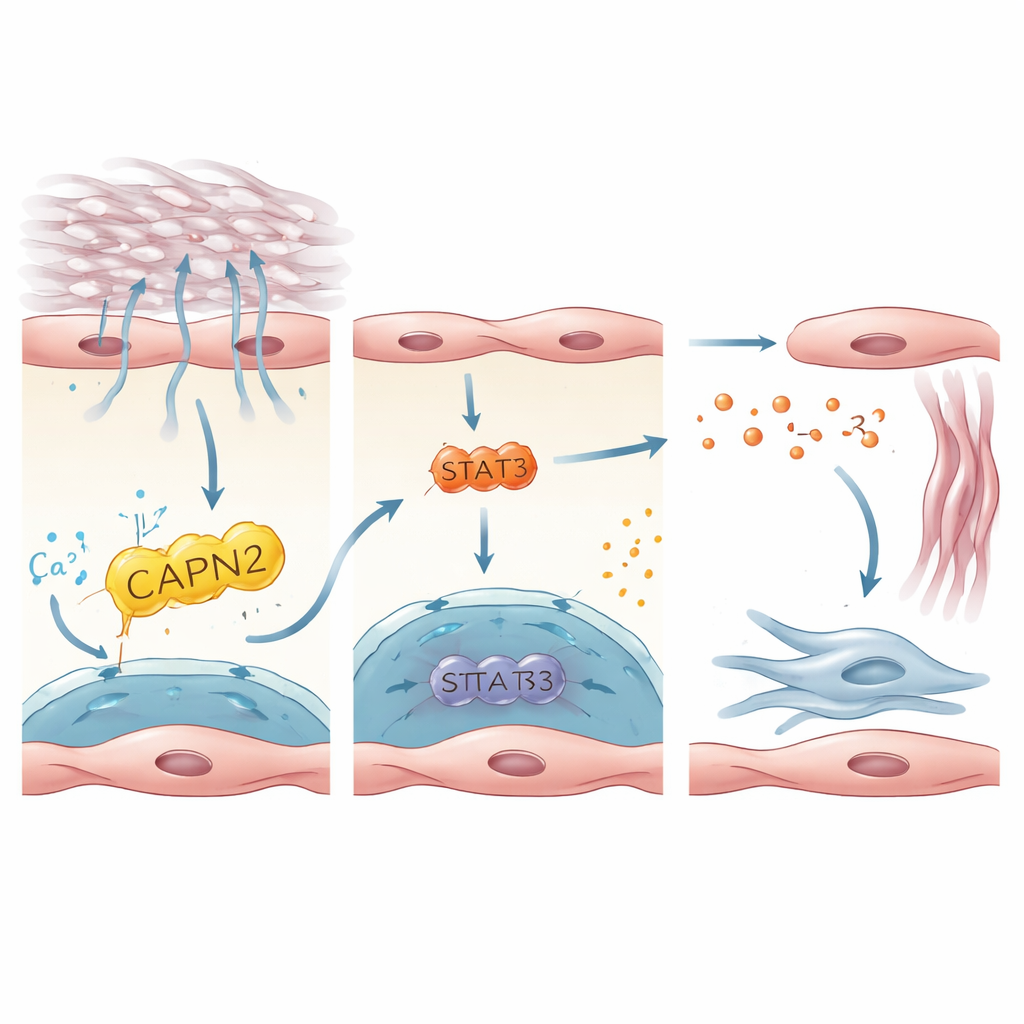
Una catena di segnalazione che risveglia le cellule produttrici di cicatrice
Lo studio ha poi tracciato come l’attivazione di PIEZO1 nelle cellule endoteliali si traduca in segnali che risvegliano i fibroblasti, le cellule che depositano tessuto cicatriziale. Integrando dataset umani e murini, gli autori hanno individuato l’interleuchina‑33 (IL‑33), una piccola proteina rilasciata da cellule stressate o danneggiate, come messaggero chiave. IL‑33 era fortemente espressa nelle cellule endoteliali positive per PIEZO1 e aumentata nei polmoni di pazienti e topi con fibrosi. In colture di cellule endoteliali umane cresciute su substrati rigidi o sottoposte a stiramento per mimare la respirazione contro un polmone rigido, l’attivazione di PIEZO1 aumentava la produzione di IL‑33. Ciò dipendeva da un enzima a valle, CAPN2, e da un fattore di trascrizione, STAT3, che insieme modulavano l’attività genica di IL‑33. Nei topi, l’eliminazione di IL‑33 specificamente nelle cellule endoteliali proteggeva dalla fibrosi, mentre costringere le cellule endoteliali a sovraprodurre IL‑33 annullava l’effetto protettivo della perdita di PIEZO1. Questi risultati delineano un asse lineare: stress meccanico → PIEZO1 → CAPN2/STAT3 → IL‑33 → attivazione dei fibroblasti e formazione di cicatrice.
Cosa significa per i trattamenti futuri
Per i non specialisti, il messaggio è che la fibrosi polmonare non è guidata solo da cellule immunitarie “fuori controllo”; è anche una malattia di un difettoso «tatto» nei vasi sanguigni. Le cellule endoteliali percepiscono che l’ambiente circostante è diventato troppo rigido, attivano l’interruttore PIEZO1 e rilasciano IL‑33, un segnale di pericolo che stimola i fibroblasti vicini a continuare a depositare cicatrice. Dissecando questa catena dalla forza meccanica all’espressione genica, il lavoro mette in luce diversi bersagli promettenti — lo stesso PIEZO1, il relè CAPN2‑STAT3 e IL‑33 — per terapie volte a interrompere il ciclo auto‑rinforzante di rigidità e cicatrizzazione. Pur richiedendo ulteriori studi per modulare in sicurezza queste vie nell’uomo, questo asse endoteliale meccanosensibile offre un nuovo approccio, fondato sulla fisica, per affrontare una malattia che a lungo ha resistito ai trattamenti efficaci.
Citazione: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Parole chiave: fibrosi polmonare, cellule endoteliali, meccanotrasduzione, PIEZO1, IL-33