Clear Sky Science · it
Adattamenti nella tubulina di Plasmodium determinano architetture, meccanica e sensibilità ai farmaci microtubulari distinti
Perché lo scheletro della malaria conta
I parassiti della malaria sopravvivono all’interno dei globuli rossi umani, ma devono anche insinuarsi attraverso le zanzare e diversi tessuti. Per farlo si appoggiano a un’impalcatura interna costituita da tubi microscopici chiamati microtubuli. Questo studio pone una domanda semplice ma significativa: come possono i microtubuli del parassita essere così specializzati e robusti se i loro mattoni di base somigliano tanto a quelli delle nostre cellule? La risposta rivela non solo come il parassita mantiene la sua forma, ma anche come potremmo progettare farmaci che colpiscano il suo scheletro senza danneggiare il nostro. 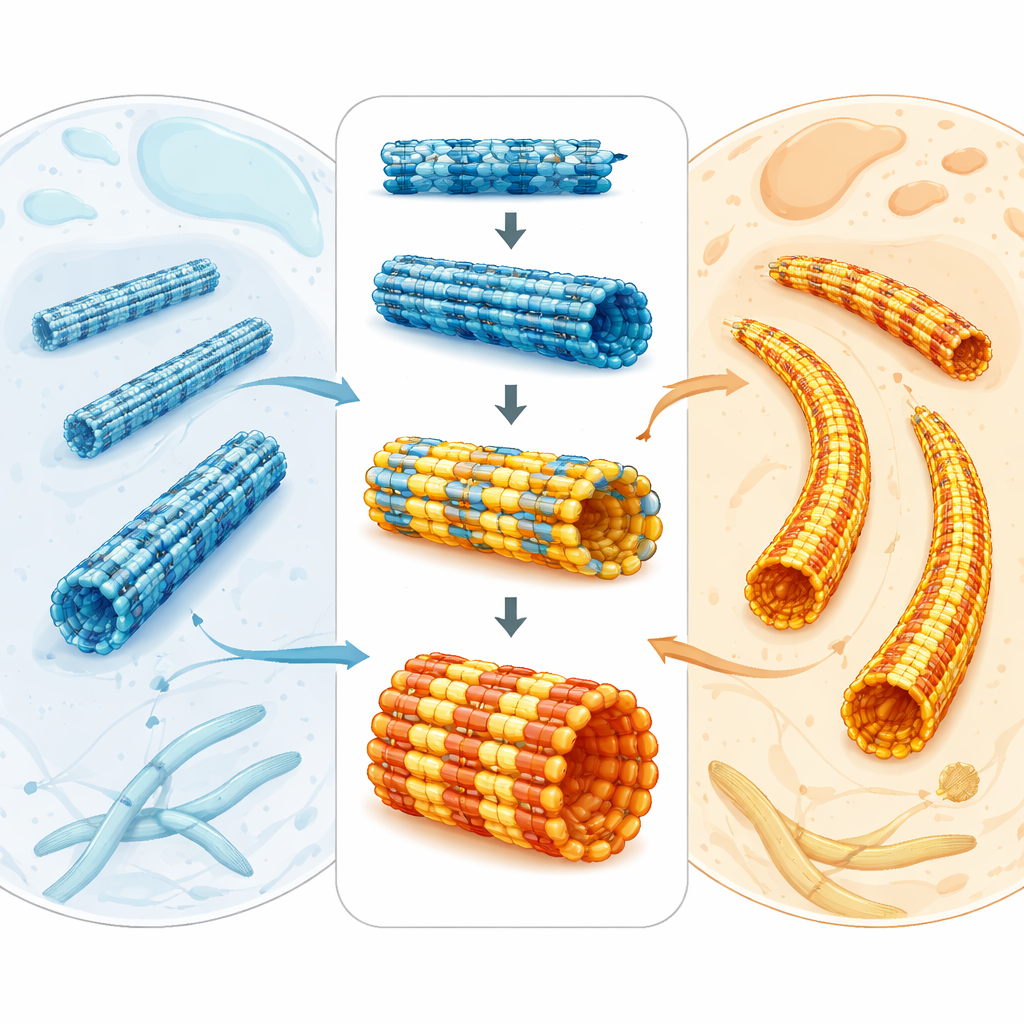
I minuscoli tubi che danno forma a un parassita letale
I microtubuli sono tubi proteici cavi che aiutano le cellule a dividersi, muoversi e mantenere la loro forma. Sono costruiti da unità proteiche a coppie chiamate tubulina. In animali, piante e parassiti la tubulina è sorprendentemente simile, il che rende difficile spiegare perché i microtubuli possano apparire e comportarsi in modo così diverso tra gli organismi. In Plasmodium falciparum, il parassita della malaria, i microtubuli formano disposizioni diverse: alcuni sono dinamici e servono durante la divisione cellulare, mentre altri sono lunghi e rigidi e fungono da supporti sotto la membrana esterna del parassita. Poiché queste strutture sono essenziali per la crescita e la trasmissione del parassita, rappresentano bersagli interessanti per i farmaci antimalarici, soprattutto mentre continua ad aumentare la resistenza ai trattamenti attuali.
Osservare la tubulina del parassita in dettaglio atomico
I ricercatori hanno purificato la tubulina direttamente dai parassiti di P. falciparum e hanno usato la crio–microscopia elettronica ad alta risoluzione per vedere come essa si assembla in microtubuli. Hanno confrontato queste strutture con i microtubuli ben studiati del cervello dei mammiferi. A prima vista la tubulina del parassita sembra quasi identica a quella umana e adotta lo stesso ripiegamento complessivo. Ma il confronto attento ha rivelato gruppi di piccoli cambiamenti di sequenza intorno a tasche chiave dove si legano molecole che trasportano energia (GTP e GDP) e dove interagiscono alcuni farmaci. Questi spostamenti sottili modificano il posizionamento di eliche e anse vicine, specialmente sulla superficie del dimero di tubulina dove si attaccano altre proteine e farmaci. Il lavoro suggerisce che, pur essendo lo schema generale conservato, ritocchi locali nel parassita rimodellano sottilmente questi siti importanti.
Tubi più rigidi grazie a legami laterali più forti
I microtubuli sono polimeri: molti dimeri di tubulina si impilano estremità contro estremità in protofilamenti, e diversi protofilamenti si affiancano per formare la parete del tubo. Il gruppo ha scoperto che nei microtubuli del parassita i contatti longitudinali lungo ciascun protofilamento appaiono molto simili a quelli dei microtubuli cerebrali. La differenza emerge nei contatti laterali, tra protofilamenti adiacenti. Sebbene l’area di contatto sia in realtà un po’ più piccola nel parassita, le simulazioni rivelano che queste connessioni laterali sono collettivamente più forti, rendendo il reticolo più rigido. La modellizzazione al computer di pezze della parete microtubulare ha mostrato che la tubulina del parassita si piega e si torce meno rispetto a quella cerebrale. La tomografia elettronica di veri estremi microtubulari ha confermato che i microtubuli del parassita hanno riccioli di protofilamenti più corti e meno aperti, un marcatore di un tubo più robusto. 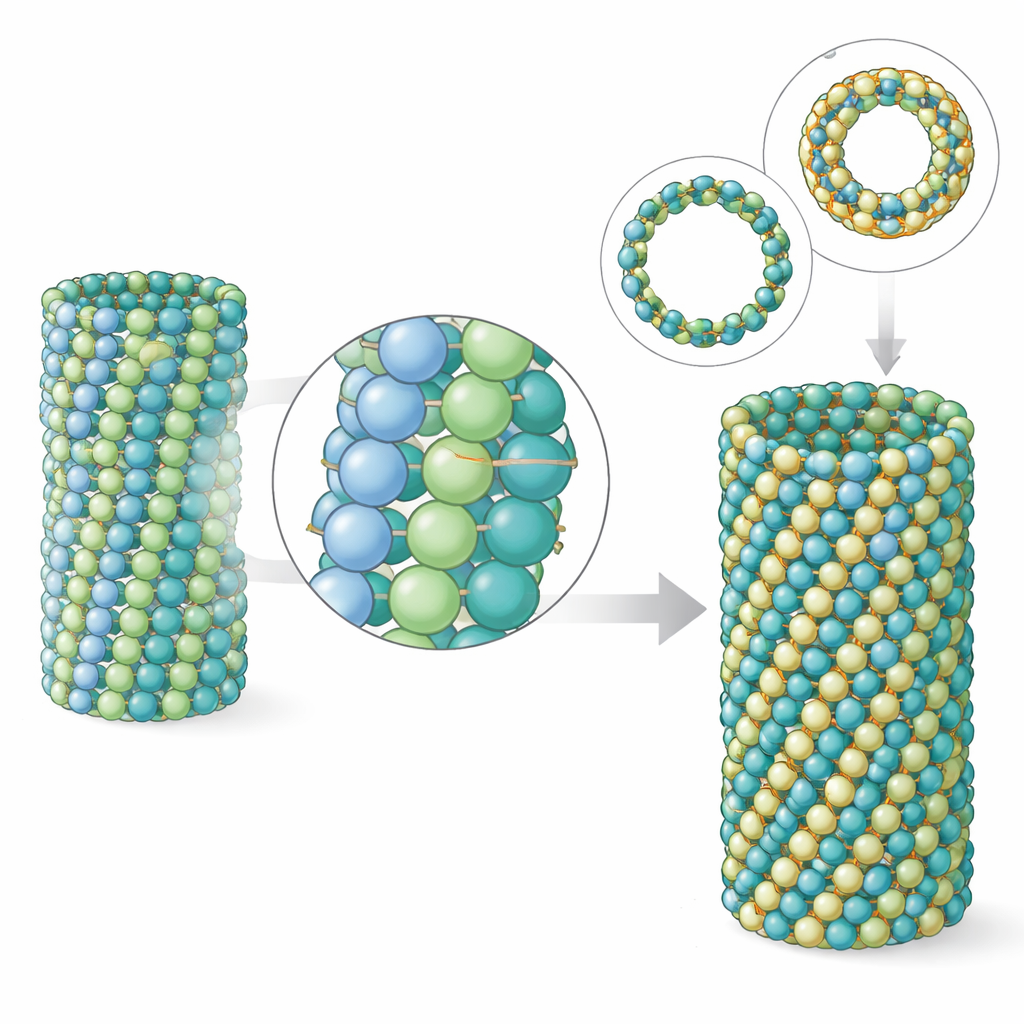
Dimensioni insolite dei tubi che corrispondono al comportamento del parassita
Un’altra caratteristica sorprendente di P. falciparum è che, in alcune fasi della sua vita, i suoi microtubuli contengono più elementi attorno alla circonferenza rispetto ai consueti 13 presenti nella maggior parte delle cellule animali—spesso 15 o addirittura 17 file di protofilamenti. Il team ha ricreato questo comportamento in provetta cambiando il nucleotide usato durante l’assemblaggio. Con una molecola simile al GTP che stabilizza lo stato in crescita, la tubulina del parassita tende naturalmente a formare microtubuli a 15 protofilamenti. Gli autori hanno risolto la struttura di questi tubi più spessi e hanno mostrato come essi accolgono i protofilamenti extra con un leggero disallineamento del reticolo, pur rimanendo quasi perfettamente cilindrici. Quando hanno confrontato questi tubi a 15 protofilamenti prodotti in laboratorio con quelli osservati all’interno delle cellule del parassita, la corrispondenza in forma e dimensioni è risultata sorprendentemente vicina, indicando che proprietà intrinseche della tubulina stessa—piuttosto che una folla di proteine ausiliarie—sono sufficienti a generare le architetture distintive del parassita.
Indizi per futuri farmaci specifici per il parassita
La conclusione dello studio è che l’evoluzione ha tarato la tubulina del parassita tramite piccoli cambiamenti di sequenza sparsi che collettivamente alterano la meccanica, l’architettura e la sensibilità ai farmaci dei microtubuli. Questi ritocchi rendono i microtubuli del parassita più rigidi e capaci di formare dimensioni tubolari non standard adatte al loro ciclo di vita esigente, pur mantenendo riconoscibile il disegno base della tubulina. Importante per la medicina, alcune tasche di legame dei farmaci appaiono quasi identiche tra parassita e ospite (come per il farmaco antitumorale paclitaxel), suggerendo che siano scarsi bersagli per antimalarici selettivi. Altre regioni, come quella ritenuta legare il composto tipo erbicida orizalin, mostrano sia spostamenti di sequenza sia lievi spostamenti strutturali che potrebbero spiegare perché i microtubuli del parassita sono più vulnerabili lì rispetto a quelli umani. Mappare queste differenze sfumate fornisce una mappa stradale per progettare futuri farmaci che interrompano lo scheletro del parassita della malaria lasciando in gran parte intatte le nostre cellule.
Citazione: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Parole chiave: parassita della malaria, microtubuli, struttura della tubulina, bersagli farmacologici, crio-microscopia elettronica