Clear Sky Science · it
Catalizzatori monoatomici Zn-N2O2 asimmetrici ispirati alla natura tramite scheletro naturale per un’efficiente N-alchilazione di nitroareni con alcoli
Trasformare gusci di scarto in strumenti chimici utili
Molti farmaci importanti, prodotti per la protezione delle colture e materiali speciali contengono una semplice caratteristica strutturale: un atomo di azoto legato a una piccola catena di carbonio. Produrre queste molecole “N‑alchilate” su scala industriale di solito richiede reagenti aggressivi, alte temperature e metalli costosi. Questo studio presenta un’alternativa più sostenibile ispirata dalla natura stessa, impiegando atomi di zinco ancorati a un supporto ricavato dal chitosano — un materiale derivato dai gusci di frutti di mare scartati — per condurre queste reazioni in modo più efficiente e con meno rifiuti.
Perché la chimica dell’azoto più verde è importante
I metodi convenzionali per legare catene carboniose all’azoto si basano su reagenti alogenati reattivi e additivi forti che generano grandi quantità di sottoprodotti. Spesso richiedono anche metalli preziosi rari e costosi come palladio o platino come catalizzatori. Al contrario, un approccio più recente chiamato strategia del “borrowing hydrogen” utilizza alcoli comuni sia come sorgente della catena carboniosa sia dell’idrogeno, con l’acqua come principale sottoprodotto. Sebbene il concetto sia attraente, i catalizzatori a base di metalli non nobili esistenti in genere funzionano solo in condizioni severe o con un ventaglio limitato di substrati. La sfida è progettare un catalizzatore a basso costo e riciclabile che possa promuovere questa reazione in modo efficiente a condizioni più miti.
Borrowing hydrogen con atomi singoli di zinco
I ricercatori hanno affrontato il problema usando la catalisi monoatomica, nella quale singoli atomi di metallo anziché particelle più grandi sono ancorati a una superficie solida. Hanno disciolto il chitosano, un polimero biodegradabile ricco di gruppi ossigeno e azoto, e lo hanno trasformato in microsfere porose tridimensionali mediante un processo sol‑gel. Sono stati quindi introdotti ioni zinco e riscaldati delicatamente, bloccando atomi isolati di zinco nella matrice di chitosano in una disposizione che gli autori descrivono come Zn‑N2O2: ogni atomo di zinco è circondato da due atomi di azoto e due di ossigeno provenienti dal supporto. Questo ambiente locale ispirato alla biologia imita il modo in cui i metalli sono coordinati in molti enzimi naturali e massimizza il numero di siti attivi disponibili per la reazione.
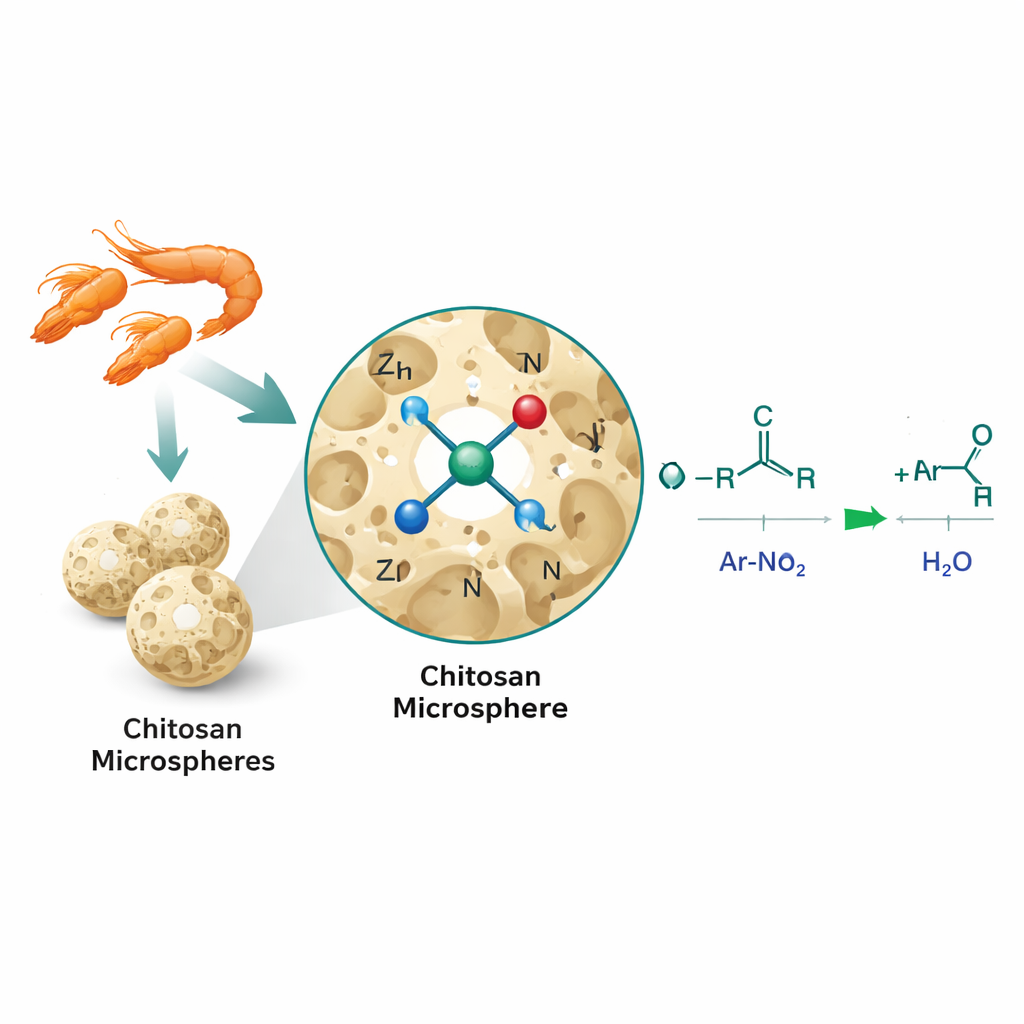
Dimostrare struttura e prestazioni
Per confermare che lo zinco esistesse realmente come atomi singoli piuttosto che come particelle più grandi, il team ha combinato diverse tecniche avanzate di imaging e spettroscopia. I microscopi elettronici hanno mostrato sfere di chitosano porose ma nessun aggregato visibile di zinco, mentre immagini ad alto angolo in campo scuro hanno rivelato piccoli punti luminosi corrispondenti a singoli atomi di zinco distribuiti uniformemente sulla superficie. Tecniche basate sui raggi X hanno inoltre indicato che lo zinco era legato principalmente ad azoto e ossigeno, senza legami zinco–zinco rilevabili, a sostegno dell’ipotesi degli atomi singoli. Queste caratteristiche strutturali si sono tradotte in prestazioni notevoli: in una reazione modello tra nitrobenzene e benzilalcol, il catalizzatore zinco‑su‑chitosano (Zn/CS) ha fornito rese molto elevate con cariche metalliche eccezionalmente basse e ha superato zinco commerciale su carbone, nanoparticelle di zinco e semplici sali di zinco disciolti. Ha funzionato inoltre per 56 diverse combinazioni di composti nitro e alcoli, inclusi blocchi complessi usati nella scoperta di farmaci, e poteva essere riutilizzato almeno cinque volte con perdita minima di attività.
Come funziona realmente il catalizzatore
A livello molecolare, il processo di borrowing‑hydrogen segue una sequenza di passaggi. Prima, l’alcol viene temporaneamente ossidato a un aldeide trasferendo idrogeno al sito di zinco. Quell’idrogeno viene poi usato per ridurre il gruppo nitro ad ammina. L’aldeide e la nuova ammina si combinano per formare un’immina, che viene infine ridotta al prodotto N‑alchilato desiderato, chiudendo il ciclo. Risonanza magnetica nucleare tempo‑risolta, cromatografia su gas e reazioni di controllo progettate con cura hanno confermato la presenza di intermedi chiave lungo questa via. Esperimenti di marcatura con deuterio, in cui alcuni atomi di idrogeno sono stati sostituiti con un isotopo più pesante, hanno mostrato che la specie zinco–idrogeno gioca il ruolo dominante nelle fasi di riduzione. Simulazioni al computer hanno aiutato a spiegare perché questo catalizzatore è così efficace: l’ambiente asimmetrico Zn‑N2O2 allontana densità elettronica dallo zinco, rendendolo leggermente povero di elettroni. Questa modulazione elettronica rende lo zinco migliore nell’adsorbire e attivare l’intermedio derivato dall’alcol, abbassando la barriera energetica per il passaggio più difficile — la rimozione iniziale dell’idrogeno dall’alcol.
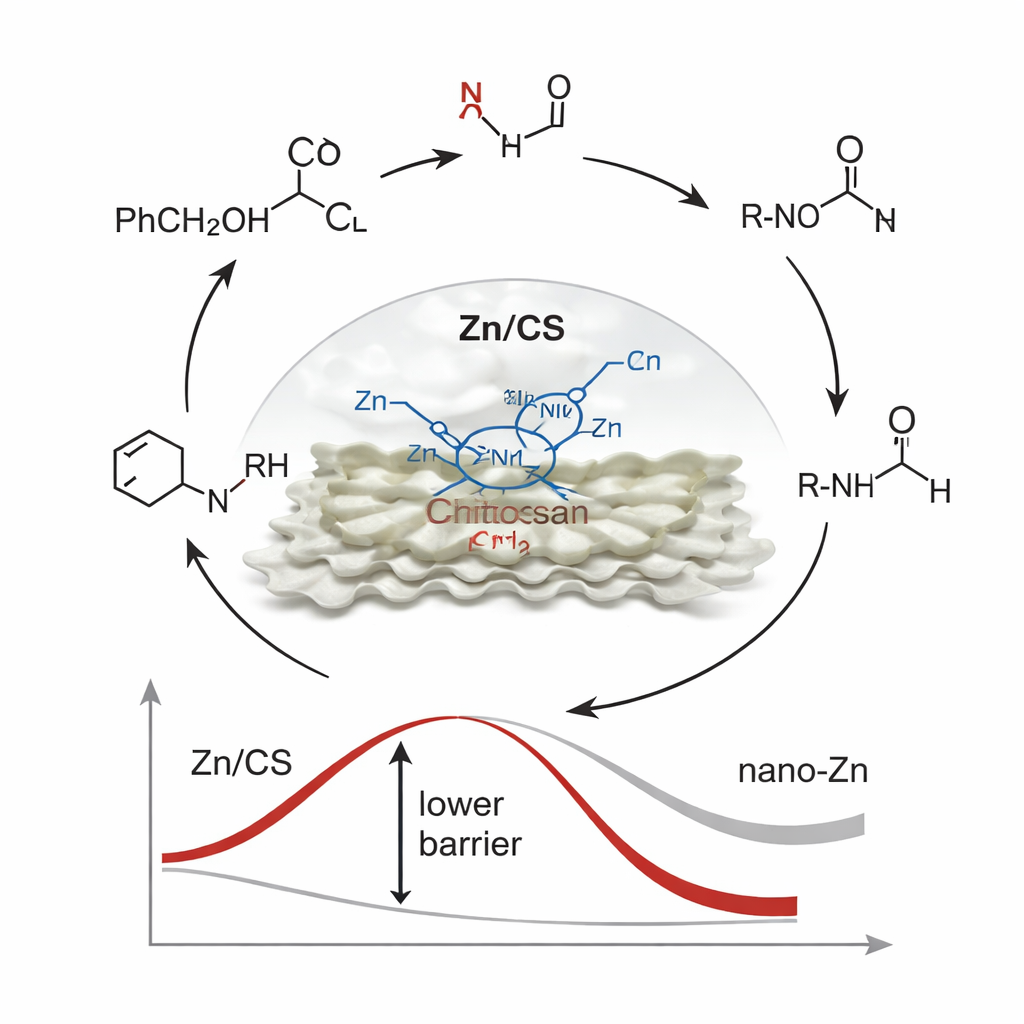
Dai rifiuti marini a catalizzatori intelligenti
In termini accessibili, questo lavoro mostra come singoli atomi di zinco, disposti con precisione su un supporto naturale a struttura spugnosa ricavato dai rifiuti del mare, possano superare molti catalizzatori metallici tradizionali in una classe importante di reazioni chimiche. Usando alcoli anziché reagenti tossici e generando principalmente acqua come sottoprodotto, il sistema offre un modo più pulito e potenzialmente più economico per produrre un’ampia gamma di molecole contenenti azoto, inclusi motivi farmacologici. La combinazione di un supporto in biopolimero rinnovabile con siti monoatomici finemente regolati illustra una strada promettente verso una chimica più sostenibile, in cui reazioni utili a livello industriale prendono in prestito principi di progettazione — e parte delle materie prime — dalla natura.
Citazione: Huang, Y., Li, Y., Yin, X. et al. Bio-inspired asymmetric Zn-N2O2 single-atom catalysts via natural skeleton for efficient N-alkylation of nitroarenes with alcohols. Nat Commun 17, 2242 (2026). https://doi.org/10.1038/s41467-026-70172-1
Parole chiave: catalisi monoatomica, chimica verde, borrowing hydrogen, chitosano, catalizzatore a zinco