Clear Sky Science · it
Il montaggio del “warhead” covalente nella biosintesi della fostriecina coinvolge malonilazione-lattonizzazione da parte di una tioesterasi bifunzionale e demalonilazione enzimatica
Come la natura costruisce un minuscolo warhead chimico
I farmaci antitumorali e gli antibiotici spesso dipendono da pochi atomi disposti in modo preciso: un piccolo “warhead” che si lega a una proteina e la blocca. Il composto naturale fostriecina è una di queste molecole, con potente attività contro enzimi coinvolti nella crescita cellulare. Ma la sua struttura complessa ne rende difficile la produzione o la modifica in laboratorio. Questo studio svela, passo dopo passo, come i batteri assemblano il warhead cruciale della fostriecina, rivelando espedienti enzimatici che i chimici possono ora prendere in prestito per progettare nuovi farmaci.
L’uncino speciale nei potenti farmaci naturali
Molti promettenti farmaci derivati da batteri del suolo appartengono a una famiglia chiamata polichetidi. All’interno di questa famiglia, un sottogruppo porta un anello reattivo, noto ai chimici come un δ-lattone α,β-insaturo, che agisce come un amo molecolare. Può formare un legame permanente con specifici amminoacidi nelle proteine, spegnendo interruttori biologici chiave. Nella fostriecina e in molecole correlate, questo uncino è abbinato a un gruppo fosfato che aiuta a indirizzare il composto verso enzimi specifici che controllano la divisione cellulare. Queste caratteristiche li rendono interessanti come lead anticancro, ma la stessa reattività e complessità strutturale li rendono difficili da sintetizzare e instabili durante lo stoccaggio.
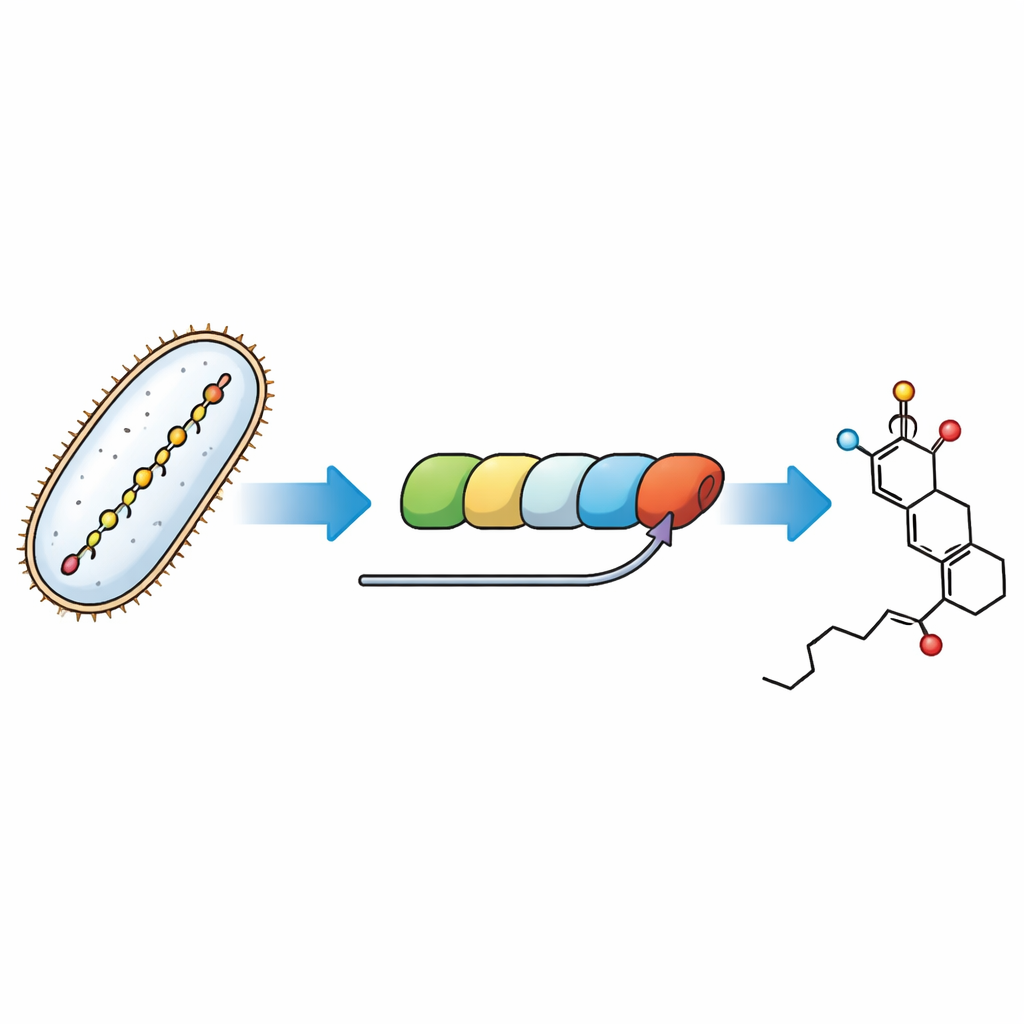
Tracciare gli ultimi passaggi di una catena di montaggio molecolare
I batteri costruiscono la fostriecina usando una massiccia macchina proteica modulare chiamata polichetide sintetasi—una catena di montaggio dove ogni stazione allunga e modella una catena carboniosa in crescita. Il rompicapo affrontato qui è come il modulo finale di questa macchina forgi l’anello warhead e installi una “maniglia” temporanea chiamata gruppo malonile che dovrà poi essere rimossa. Ricreando la via biosintetica in provetta con enzimi purificati e sostituti molecolari appositamente progettati per gli intermedi naturali, i ricercatori hanno potuto osservare i singoli passaggi e attribuirli a parti specifiche della catena di montaggio.
Un enzima multitasking con un talento inaspettato
Il team ha scoperto che la stazione finale della catena di montaggio, un dominio chiamato FosTE, si comporta in modo mai visto prima. Le versioni tipiche di questo dominio semplicemente tagliano i prodotti finiti dalla catena. FosTE, invece, prima preleva un frammento malonile da un comune mattoncino cellulare e lo trasferisce su un preciso sito ossigeno della catena in crescita, e poi aiuta la catena a ripiegarsi chiudendosi nell’anello warhead. Mutare una singola serina reattiva in FosTE interrompe entrambe le attività. La modellizzazione strutturale evidenzia due residui di arginina carichi positivamente nel sito attivo che cullano il frammento malonile e lo posizionano per il trasferimento—funzioni normalmente svolte da un diverso tipo di enzima. Sostituire queste arginine con residui neutri cancella il passaggio di trasferimento del malonile lasciando sostanzialmente intatta la formazione dell’anello, confermandone il ruolo critico.
Fissare il warhead e prevenire gli sprechi
Una volta che l’anello si è formato e porta il suo gruppo malonile temporaneo, un altro enzima, FosM, deve rimuovere questo gruppo per svelare il warhead completamente armato. Lo studio mostra che FosM funziona in modo efficiente solo dopo che un ulteriore enzima, una chinasi di ampia specificità chiamata FosH, ha aggiunto un fosfato in una posizione vicina sulla molecola. Quando i ricercatori hanno fornito l’anello malonilato a FosM da solo, si è osservata solo una modesta conversione. Aggiungere prima FosH ha portato a una quasi completa rimozione del gruppo malonile e alla formazione dell’unità reattiva finale. È importante che FosH possa anche aggiungere il fosfato a intermedi “di scarto” correlati che si formano da reazioni laterali, recuperandoli in modo che possano essere processati correttamente invece di andare perduti come prodotti morti.
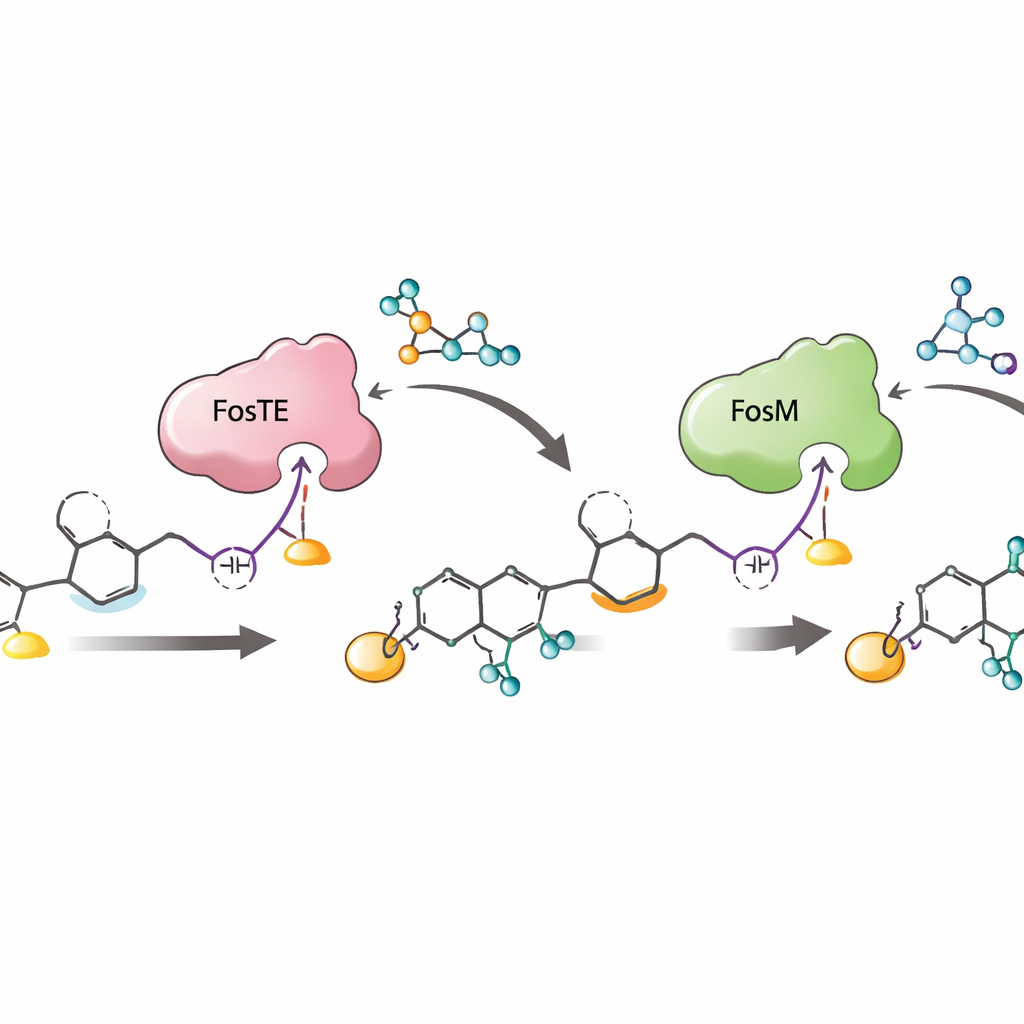
Perché questa coreografia enzimatica è importante
Nel complesso, il lavoro rivela una sequenza strettamente coreografata: estensione della catena sulla catena di montaggio, aggiunta di malonile e chiusura dell’anello guidate da FosTE, fosforilazione da parte di FosH e infine rimozione del malonile innescata da FosM. Quest’ordine non solo costruisce il delicato warhead in modo efficiente, ma protegge anche gli intermedi instabili dal disgregarsi e massimizza la produzione della forma fosforilata desiderata, la più attiva come lead farmaceutico. Mostrando come un singolo dominio enzimatico possa sia decorare sia rilasciare una molecola in crescita—e come gli enzimi partner rifiniscano e recuperino gli intermedi reattivi—lo studio offre una guida per l’ingegneria di nuovi polichetidi con warhead e per la costruzione di percorsi sintetici più brevi ed efficienti verso complessi agenti anticancro come la fostriecina.
Citazione: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Parole chiave: fostriecina, biosintesi dei polichetidi, ingegneria enzimatica, warhead di prodotti naturali, sintesi chemoenzimatica