Clear Sky Science · it
Regolazione della traduzione mediante desolfurazione ossidativa delle modifiche del tRNA
Come le cellule regolano la produzione proteica sotto stress
Ogni cellula deve decidere quali proteine produrre, con quale velocità e quando rallentare. Questo studio mette in luce un sottile interruttore chimico sui trasfer RNA (tRNA) che aiuta le cellule a ridurre la produzione proteica quando l’ambiente cellulare diventa più ossidante, ad esempio durante l’infiammazione o lo stress metabolico. Osservando il comportamento di questo interruttore in cellule di mammifero e in sistemi in vitro, i ricercatori rivelano un nuovo modo in cui cambiamenti simili a danni nell’RNA possono funzionare come segnali regolatori.
Piccole marche sul tRNA con grandi conseguenze
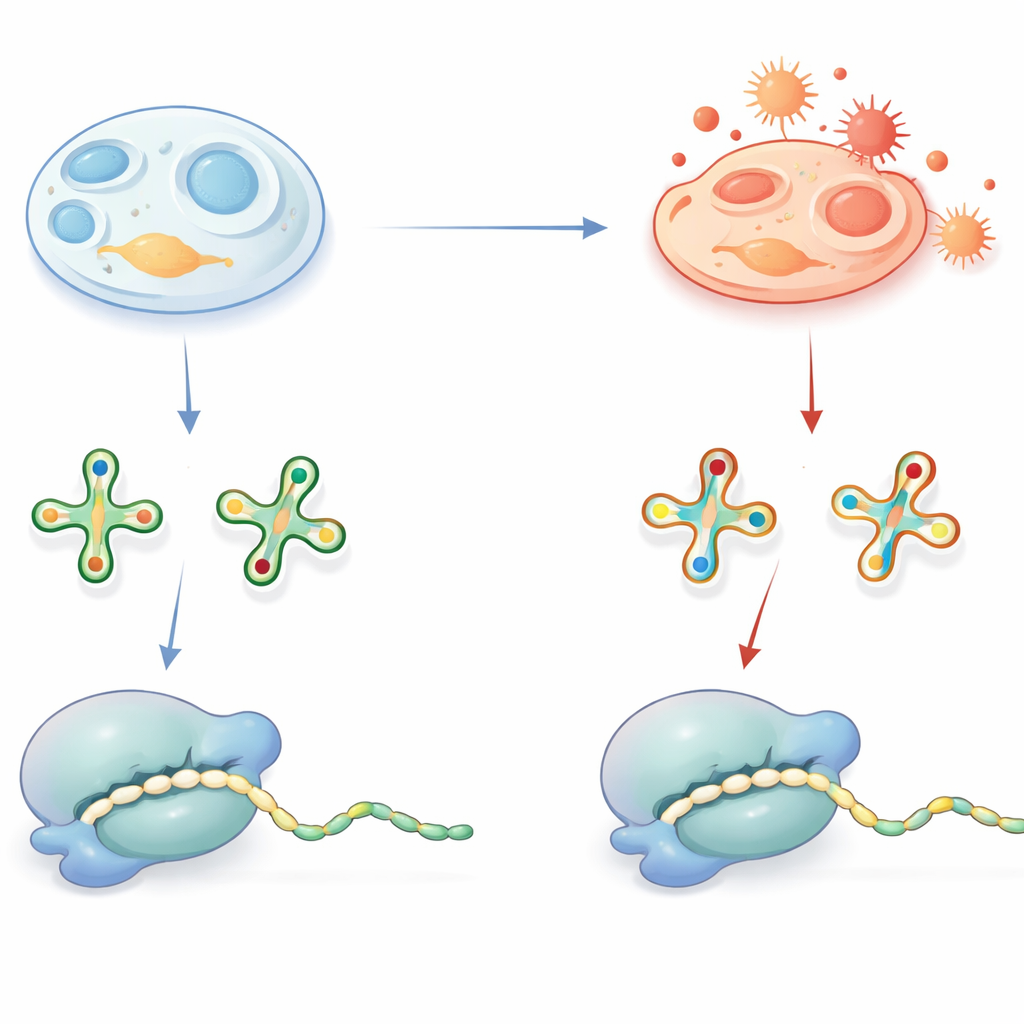
I tRNA agiscono da adattatori che leggono le “parole” di tre lettere dell’mRNA e consegnano gli amminoacidi corrispondenti durante la sintesi proteica. Per svolgere questo compito in modo accurato ed efficiente, molti tRNA portano particolari decorazioni chimiche, in particolare in una posizione chiave che contatta la terza lettera di ciascun codone. Una decorazione diffusa è un gruppo contenente zolfo su una base uridina, spesso indicata come un derivato della 2-tio-uridina. In condizioni sane questo gruppo solforato aiuta il tRNA a riconoscere i codoni corretti terminanti con le lettere A o G e supporta una traduzione rapida e senza errori. Difetti in queste modifiche sono già noti per causare malattie umane, sottolineandone l’importanza.
Quando lo stress ossidativo riscrive il tRNA
Il gruppo solforato che migliora il decoding ha però uno svantaggio: è chimicamente vulnerabile all’ossidazione. Il gruppo di lavoro ha chiesto se, all’interno delle cellule, questo gruppo venga effettivamente rimosso in condizioni ossidative e cosa ciò comporterebbe per la sintesi proteica. Usando spettrometria di massa sensibile, hanno identificato versioni ossidate e prive di zolfo di queste basi tRNA—chiamate derivati h2U—in tessuti di topo, mitocondri di maiale, batteri, lievito e in diverse linee cellulari umane. Un ingegnoso esperimento di spike-in con un tracciante di tRNA batterico ha dimostrato che queste marche h2U non sono artefatti creati durante la preparazione dei campioni, ma si formano all’interno delle cellule vive. Sebbene le versioni ossidate fossero presenti solo in una frazione dei tRNA, la loro abbondanza variava tra tessuti e tipi cellulari, suggerendo che lo stato redox cellulare e la capacità antiossidante influenzano la frequenza di questa conversione.
Come i tRNA ossidati rallentano la catena di montaggio
I ricercatori hanno poi verificato come questi tRNA alterati si comportano durante la sintesi proteica. Hanno convertito chimicamente la forma contenente zolfo nella forma ossidata h2U nel pool di tRNA e hanno utilizzato un sistema di traduzione umano completamente ricostituito in vitro. Una proteina reporter la cui produzione dipende fortemente da questi tRNA modificati mostrò un calo netto della resa quando i tRNA erano desolfurati, mentre un reporter di controllo che evita i codoni interessati traduceva normalmente. Saggi biochimici hanno rivelato il motivo: i tRNA ossidati per lisina, glutammina e glutammato erano caricati con i rispettivi amminoacidi molto meno efficientemente, mentre i tRNA corrispondenti all’arginina erano in gran parte risparmiati. È importante che i tRNA contenenti h2U apparivano ancora nelle frazioni legate ai ribosomi (polisomiche) provenienti dalle cellule, indicando che partecipano comunque alla traduzione ma con scarsa efficienza.
Una visione strutturale del decoding indebolito
Per vedere esattamente come l’ossidazione altera il decoding, il team ha utilizzato microscopia crioelettronica ad alta risoluzione per immaginare ribosomi batterici programmati con tRNA umano per la lisina e codoni specifici. Nello stato normale, con zolfo, la base modificata nella posizione di “wobble” del tRNA formava o una coppia di basi standard con un codone terminante in A o una coppia di wobble speciale con un codone terminante in G, entrambe saldamente collocate nel centro di decoding del ribosoma. Dopo la desolfurazione, la stessa base poteva stabilire soltanto un singolo contatto debole con il codone terminante in A e formava una coppia di wobble meno stabile con il codone terminante in G. Esperimenti di legame confermarono queste strutture: il tRNA per la lisina ossidato perdeva sostanzialmente la capacità di riconoscere il codone AAA e riconosceva il codone AAG con molta minore efficienza. Complessivamente, questi risultati mostrano come una piccola modifica chimica possa tradursi in rallentamenti della sintesi proteica specifici per certi codoni.
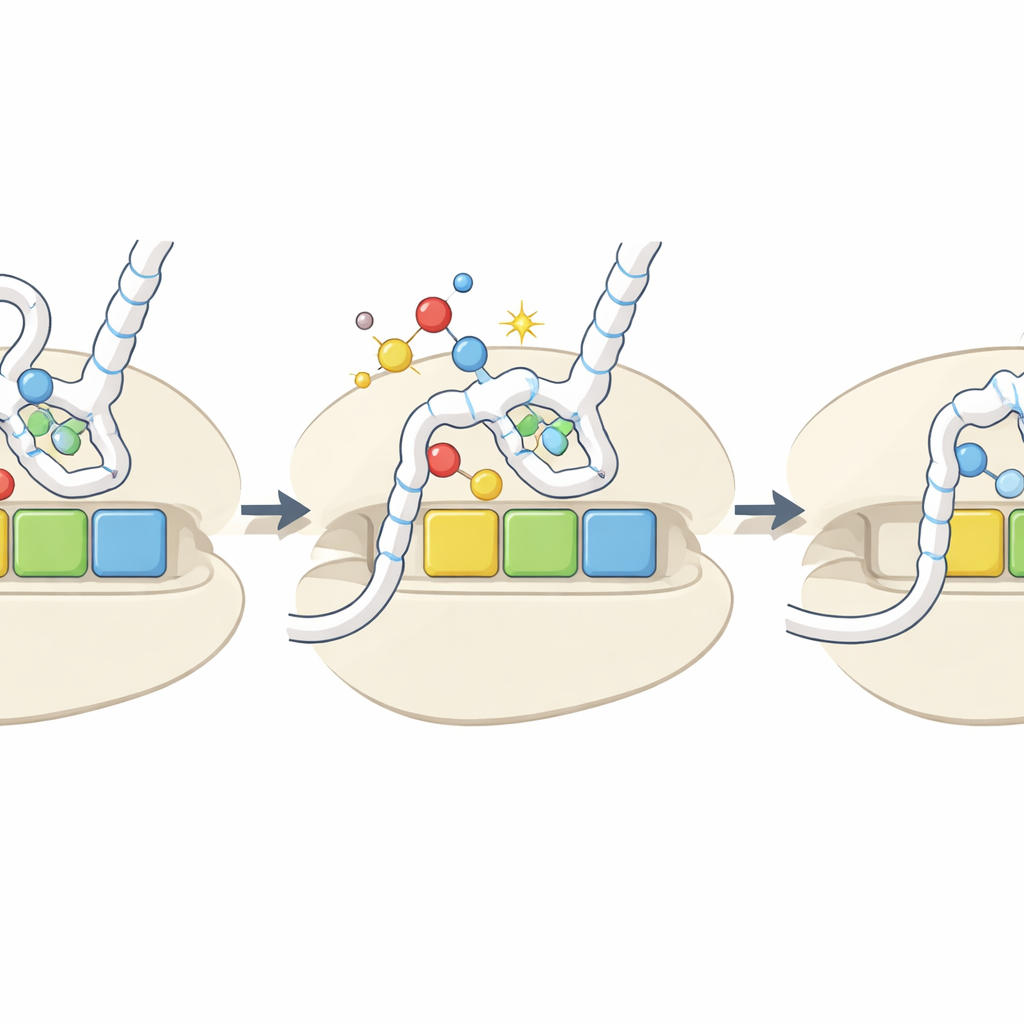
Un segnale di danno che diventa una manopola regolatrice
Nel complesso, lo studio propone che la rimozione ossidativa dello zolfo da basi chiave del tRNA funzioni come un sensore intrinseco dello stato redox della cellula. Sotto stress ossidativo, più tRNA vengono convertiti nella forma h2U, che vengono caricati male e si legano debolmente a certi codoni. Questo rallenta selettivamente la traduzione su quei codoni, potenzialmente alterando la stabilità degli mRNA interessati, modificando il modo in cui le proteine si ripiegano e attivando percorsi di risposta allo stress quando i ribosomi si bloccano. Sebbene le marche ossidate siano relativamente rare e i loro livelli non aumentino sempre drasticamente sotto stress sperimentale, i loro effetti specifici per codone e amminoacido significano che anche cambiamenti modesti potrebbero rimodellare quali proteine vengono sintetizzate e con quale velocità in condizioni difficili.
Citazione: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Parole chiave: modifica del tRNA, stress ossidativo, sintesi proteica, regolazione della traduzione, danno all'RNA