Clear Sky Science · it
Colpire l’uso della tirosina dipendente da tRNA svela una vulnerabilità metabolica nel carcinoma epatocellulare
Affamare le cellule tumorali di un blocco costitutivo comune
Le cellule del cancro al fegato, come tutte le cellule in rapida proliferazione, hanno bisogno di un apporto costante di amminoacidi—i minuscoli mattoni delle proteine. Questo studio rivela che il carcinoma epatocellulare, la forma più comune di tumore del fegato, presenta una debolezza inaspettata: dipende fortemente dall’amminoacido tirosina sia per la produzione di energia sia per la sopravvivenza. Limitando selettivamente l’uso della tirosina da parte delle cellule tumorali, i ricercatori sono riusciti a rallentare la crescita del tumore, danneggiare le centrali energetiche delle cellule cancerose e innescare una forma di morte cellulare che potrebbe essere sfruttata per nuovi trattamenti.
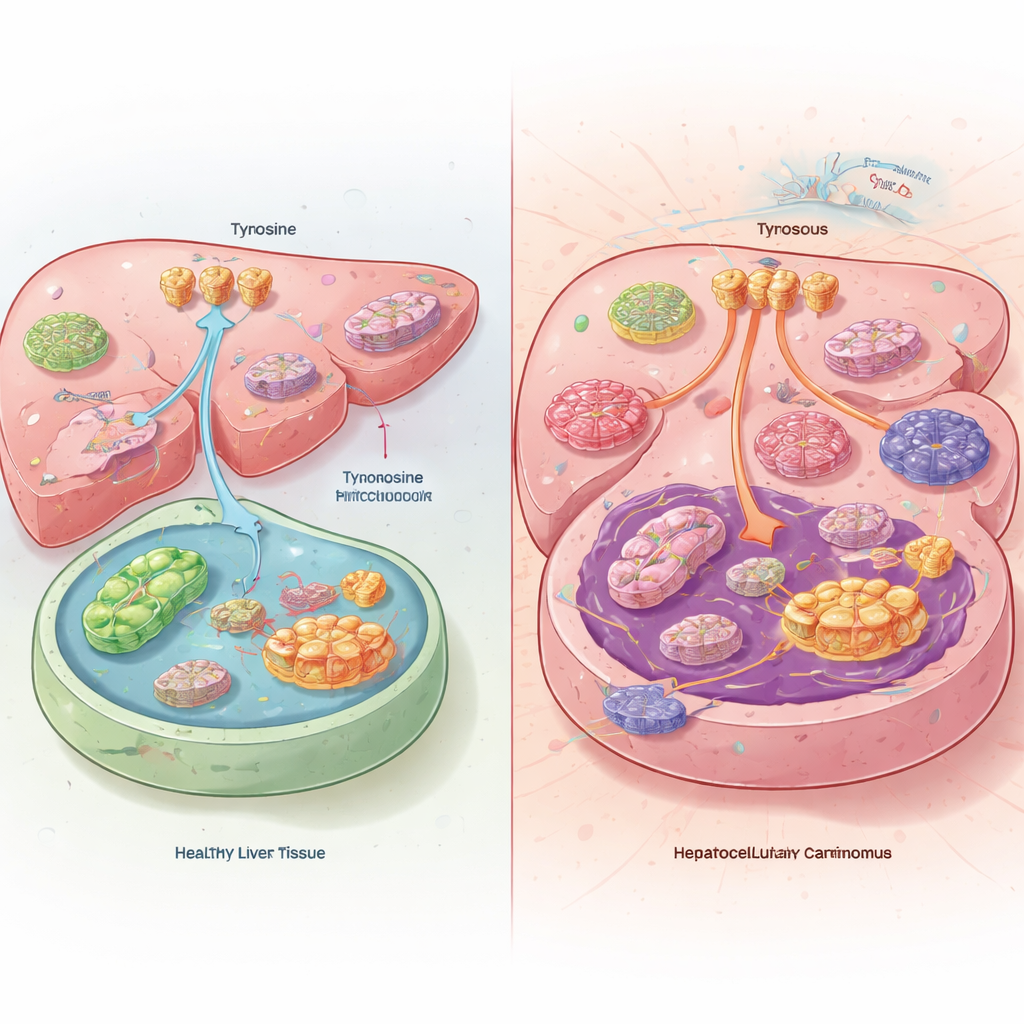
Un squilibrio nascosto nei tumori del fegato
Quando il gruppo ha confrontato i tumori epatici con il tessuto epatico sano di pazienti e topi, ha trovato qualcosa di sorprendente. All’interno delle cellule tumorali, i livelli di tirosina risultavano in realtà bassi, nonostante i tumori assorbissero più tirosina dal flusso sanguigno e ne degradassero meno. Invece di bruciare la tirosina come combustibile, i tumori epatici la reindirizzavano verso la sintesi proteica. Le neoplasie ottennero questo aumentando l’attività dei trasportatori di tirosina sulla superficie cellulare e riducendo gli enzimi che normalmente degradano la tirosina nel fegato. I topi nutriti con una dieta priva di tirosina svilupparono tumori più piccoli e vissero più a lungo, mentre un eccesso di tirosina nella dieta accelerò la crescita tumorale.
Come il cancro riorganizza la produzione proteica
I ricercatori hanno ricondotto questa fame di tirosina a un potente gene promotore di tumori chiamato MYC. Nei tumori epatici, MYC attiva una proteina chiamata YARS1, che lega la tirosina a un transfer RNA specifico (tRNA-TyrGUA). Questo tRNA caricato è ciò che i ribosomi utilizzano per costruire proteine ricche di tirosina. Lo studio ha dimostrato che i tumori epatici aumentano sia YARS1 sia il tRNA corrispondente, garantendo una via preferenziale della tirosina verso la sintesi proteica. Interrompere questa linea—abbassando i livelli di tirosina, silenziando YARS1 o il tRNA-TyrGUA, o bloccando il caricamento della tirosina—rese le cellule del cancro del fegato molto meno competitive in coltura e nei topi, rivelando una vulnerabilità metabolica strettamente collegata alle loro elevate esigenze di produzione proteica.
Gegnare le centrali e l’equilibrio lipidico
Combinando misure su scala genomica di RNA, produzione proteica e metaboliti, il team identificò due obiettivi particolarmente sensibili alla restrizione della tirosina. Il primo, NDUFB8, è una componente del complesso I mitocondriale, parte centrale della macchina che genera energia cellulare. L’altro, SCD1, aiuta a convertire i grassi saturi in grassi monoinsaturi più sicuri da immagazzinare nelle membrane e nelle gocce lipidiche. Quando la tirosina destinata alla traduzione venne limitata, la produzione di NDUFB8 e SCD1 calò, mentre i loro livelli di RNA rimasero in gran parte invariati—evidenza chiara che era la traduzione, non l’espressione genica, a essere colpita. Ciò portò a un assemblaggio difettoso del complesso I, a una respirazione cellulare ridotta, a eccesso di specie reattive dell’ossigeno e a uno spostamento dei lipidi da forme monoinsature verso forme polinsature più fragili e facilmente ossidabili.
Spingere le cellule tumorali verso una morte guidata dal ferro
Il danno mitocondriale combinato e l’instabilità lipidica spinsero le cellule del cancro del fegato verso la ferroptosi, una forma di morte cellulare dipendente dal ferro e guidata dalla perossidazione lipidica. I tumori tentarono di difendersi aumentando bloccanti naturali della ferroptosi come GPX4 e molecole correlate, ma un’ampia schermata CRISPR dimostrò che disabilitare questi protettori rendeva la restrizione della tirosina ancora più letale. Nei modelli cellulari e murini, associare strategie di limitazione della tirosina con farmaci che inibiscono GPX4 o BCL2—o con farmaci già usati contro il cancro del fegato come sorafenib e venetoclax—produsse un controllo tumorale più efficace, un carico tumorale ridotto e una sopravvivenza più lunga.
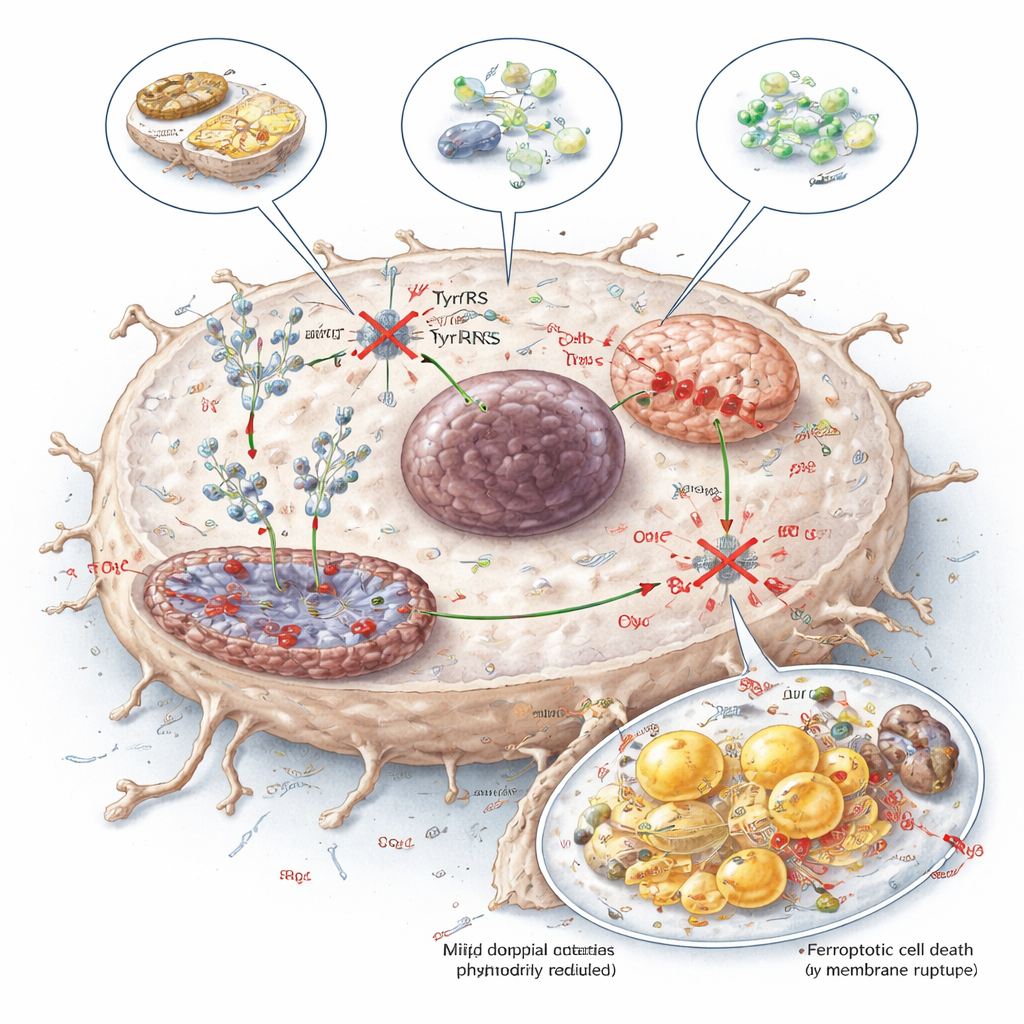
Trasformare una debolezza metabolica in terapia
Per esplorare modi pratici di sfruttare questa vulnerabilità, i ricercatori testarono tre approcci: una dieta a restrizione di tirosina, un enzima (TAL) che degrada enzimaticamente la tirosina, e una piccola molecola chiamata tirosinolo che compete con la tirosina per il legame a YARS1. Tutti e tre ridussero la disponibilità di tirosina per la sintesi proteica, abbassarono i livelli di NDUFB8 e SCD1, danneggiarono la funzione mitocondriale e aumentarono la ferroptosi nei tumori del fegato, mostrando al contempo effetti gestibili sui tessuti normali nei topi. In termini semplici, il messaggio è che i tumori epatici sembrano dipendere dalla tirosina non solo come nutriente, ma come carburante preciso per la loro macchina di produzione proteica. Targetizzare questa dipendenza—con dieta, enzimi o farmaci—offre un nuovo approccio promettente per indebolire i tumori e potenziare l’efficacia delle terapie esistenti.
Citazione: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Parole chiave: cancro al fegato, metabolismo degli amminoacidi, tirosina, mitocondri, ferroptosi