Clear Sky Science · it
Identificazione sistematica delle interazioni specifiche di variante tra struttura dell'RNA e piccole molecole esemplificata dai G-quadruplex di RNA
Perché piccole modifiche nell'RNA contano per i farmaci del futuro
La maggior parte di noi eredita piccole differenze nel DNA che ci rendono unici. Questi minuscoli cambiamenti possono rimodellare in modo sottile le pieghe delle molecole di RNA all'interno delle nostre cellule. Il nuovo studio introduce un modo per osservare come tali variazioni genetiche modifichino l'aderenza di farmaci sperimentali diretti all'RNA. Questo è importante perché lo stesso medicinale potrebbe comportarsi in modo molto diverso da una persona all'altra, specialmente nei casi di cancro o malattie genetiche.
Un nuovo modo per vedere dove i farmaci toccano l'RNA
Molti sviluppatori di farmaci stanno ora guardando all'RNA, non solo alle proteine, come bersagli terapeutici. Le piccole molecole possono agganciarsi a forme strutturali particolari dell'RNA e influenzare la lettura dei geni, ma fino ad ora la maggior parte dei metodi funzionava solo su una singola sequenza di riferimento. Questi approcci hanno in larga misura ignorato le innumerevoli variazioni di una singola lettera presenti nei pazienti reali. Gli autori hanno creato un approccio ad alto rendimento chiamato BIVID-MaP che può testare simultaneamente migliaia di varianti di RNA e individuare dove una piccola molecola si lega a ciascuna di esse, con risoluzione fino al singolo nucleotide. 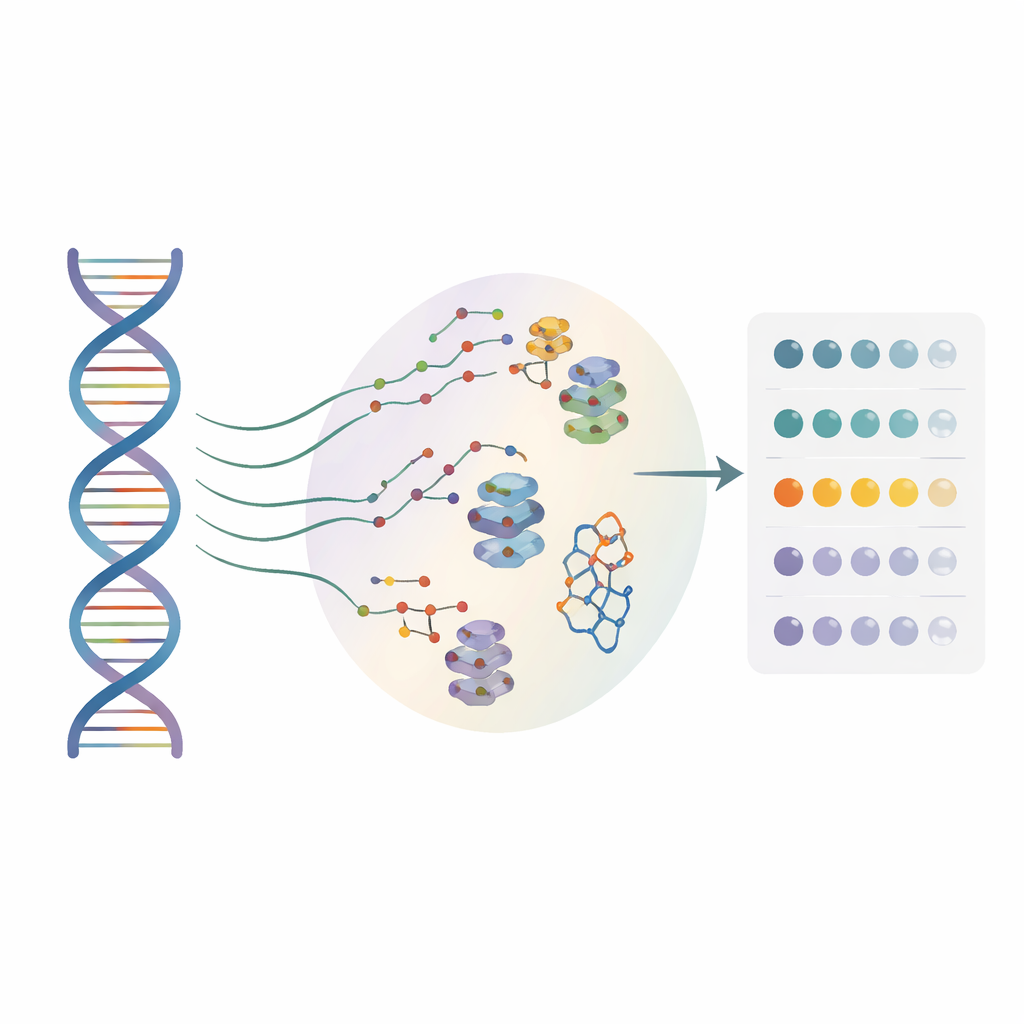
Trasformare marche chimiche in un segnale leggibile
BIVID-MaP funziona in tre passaggi principali. Per prima cosa, il gruppo lega un marcatore reattivo a una piccola molecola che si lega all'RNA. Quando questo composto marcato si inserisce nella sua struttura RNA preferita, come un G-quadruplex compatto formato da sequenze ricche di guanine, il marcatore forma un legame chimico permanente con una base vicina dell'RNA. In secondo luogo, un enzima speciale copia l'RNA modificato in DNA. Quando incontra una di queste marche chimiche tende a “saltare” una singola base, creando una piccola delezione nella copia. In terzo luogo, il sequenziamento profondo rileva queste firme di delezione attraverso milioni di molecole. Poiché quasi tutta la sequenza circostante è preservata, le delezioni possono essere assegnate con precisione a varianti genetiche specifiche in una popolazione mista.
Dimostrare il metodo con un caso di test controllato
Per confermare che BIVID-MaP rileva davvero il legame specifico per variante, i ricercatori hanno studiato un segmento di RNA del gene CD44 che normalmente forma un G-quadruplex. Una singola sostituzione da G ad A altera questa struttura. In una miscela contenente entrambe le versioni, solo la forma intatta ha mostrato segnali intensi di delezione vicino alla regione piegata quando esposta a una sonda a base di berberina, e saggi indipendenti hanno verificato un legame più forte in quel sito. Il mutante, che non può formare la stessa conformazione, ha prodotto molte meno delezioni e un legame più debole. Altre tecniche di mappatura comuni o non hanno rilevato questa differenza o hanno prodotto rumore confondente, sottolineando la maggiore sensibilità e specificità del nuovo approccio.
Scansionare mutazioni legate al cancro in molti geni
Il gruppo ha quindi aumentato la scala. Hanno costruito una libreria di RNA delle regioni non tradotte 5′ (5′ UTR) di 283 geni correlati al cancro, ciascuna abbinata a mutazioni somatiche reali riportate nei tumori. Utilizzando una sonda che riconosce strutture simili ai G-quadruplex, BIVID-MaP ha individuato numerose mutazioni che o rafforzavano o indebolivano il legame con piccole molecole. In geni come DAXX e ING2, cambi di singole lettere in tratti ricchi di guanine hanno alterato marcatamente il legame, in accordo con saggi biofisici indipendenti sulla formazione di G-quadruplex e misurazioni dirette del legame mediante spettrometria di massa. In alcuni casi, mutazioni al di fuori dei tratti evidenti di G hanno comunque spostato il legame modificando sottilmente la probabilità di appaiamento delle basi vicine, rimodellando l’“insieme” strutturale senza alterare grossolanamente la piega complessiva prevista. 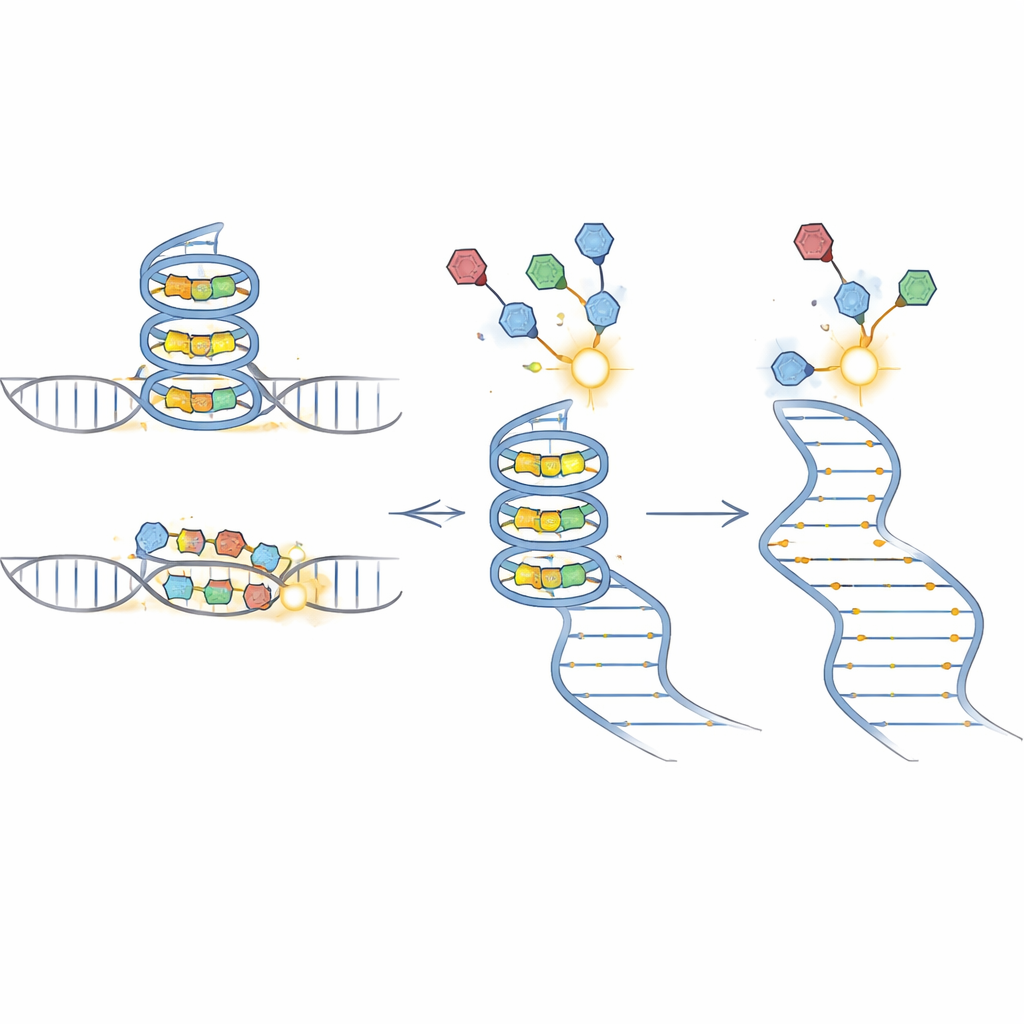
Ciò che le predizioni al computer non colgono
È importante notare che gli strumenti esistenti per predire la struttura dell'RNA e i G-quadruplex spesso non sono riusciti a prevedere i cambiamenti che BIVID-MaP ha rivelato. Alcune varianti che modificavano appena i punteggi computazionali hanno prodotto grandi differenze reali nel legame. Altre sembravano influenzare il legame in una famiglia di composti che prendono di mira i G-quadruplex, mentre certe mutazioni avevano effetti specifici per un dato farmaco. Questo mostra che le varianti a singolo nucleotide possono modulare il panorama delle pieghe dell'RNA e dei contatti con i farmaci in modi difficili da inferire solo dalla sequenza.
Cosa significa per i farmaci personalizzati che mirano all'RNA
Gli autori concludono che BIVID-MaP offre una via potente per mappare come le differenze genetiche individuali rimodellano le strutture dell'RNA e le loro interazioni con piccole molecole farmacologiche. Convertendo modifiche chimiche locali in precise firme di delezione, il metodo può esaminare migliaia di varianti in parallelo e mettere in luce quelle che modificano in modo significativo il legame con i farmaci. A lungo termine, tali mappe potrebbero orientare la progettazione di farmaci che mirano all'RNA più efficaci e sicuri in pazienti diversi, e rivelare strutture di RNA precedentemente nascoste che potrebbero servire come nuovi bersagli terapeutici.
Citazione: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Parole chiave: farmaci mirati all'RNA, G-quadruplex, varianti genetiche, legame con piccole molecole, mutazioni tumorali