Clear Sky Science · it
Ottimizzazione dell’organizzazione spaziale degli anelli FtsZ per una costrizione su larga scala in cellule sintetiche
Perché contano gli anelli minuscoli nella costruzione di cellule sintetiche
Immaginate di costruire una cellula artificiale semplice che possa crescere e dividersi da sola. Per farlo, gli scienziati devono imparare a pizzicare una membrana morbida, simile a una bolla di sapone, in modo controllato usando solo pochi componenti biologici. Questo studio mostra come una proteina batterica possa essere aiutata a formare anelli grandi e stabili su bolle lipidiche giganti, permettendo a questi “modelli” di cellule di contrarsi quasi fino alla divisione. Rivela quale tipo di architettura proteica è necessaria per piegare e rimodellare una membrana alla scala di un’intera cellula.
Prendere in prestito gli strumenti della divisione dalla natura
Molti batteri si dividono usando una proteina chiamata FtsZ, un lontano parente della tubulina che costruisce lo scheletro interno delle nostre cellule. FtsZ si assembla in filamenti che si raccolgono in un anello al punto medio della cellula, segnando dove la cellula si dividerà. Nei batteri vivi, una serie di proteine ausiliarie collega questo anello alla membrana interna, lo posiziona al centro e lo collega a enzimi che rimodellano la parete cellulare. Tentativi precedenti in laboratorio di ricreare questa macchina in vescicole grandi quanto una cellula erano riusciti a formare anelli e a provocare piccole rientranze nella membrana, ma non una costrizione progressiva e omogenea che rimodelli una vescicola gigante in due metà quasi separate.
Un approccio minimalista a un involucro che si divide
Gli autori si sono chiesti se potessero ridurre questo sistema a soltanto due componenti: una versione di FtsZ in grado di aderire direttamente alle membrane e una breve coda carica positivamente di un’altra proteina di divisione, FtsN. Hanno incapsulato questi componenti all’interno di grandi vescicole unilamellari — sfere cave di lipidi che assomigliano a cellule semplificate — e le hanno fornite con la molecola energetica GTP e un analogo di GTP a lenta azione per modulare la dinamica delle proteine. Senza la coda di FtsN, FtsZ formava molti anelli e chiazze piccole che causavano solo avvallamenti locali. Con un eccesso del frammento di FtsN (chiamato cytoFtsN), quei piccoli anelli si riorganizzavano in un singolo anello grande che avvolgeva la vescicola vicino all’equatore ed era in grado di contrarsi nel corso di diverse ore.
Da una rete aggrovigliata a un unico anello contrattile
Per capire come questo piccolo peptide cambiasse il comportamento in modo così drastico, il gruppo ha osservato i filamenti di FtsZ su membrane supportate piatte con microscopia ad alta risoluzione. Normalmente, FtsZ su tali superfici forma vortici curvi e turbinanti. L’aggiunta di quantità crescenti di cytoFtsN cancellava gradualmente questi spirali e li sostituiva con fasci più dritti e allineati. L’analisi quantitativa delle immagini ha confermato che la rete diventava più coerente e ordinata all’aumentare della concentrazione del peptide. Esperimenti di recupero della fluorescenza hanno mostrato che i subunità all’interno di questi fasci si scambiavano più lentamente, indicando che il peptide stabilizza i filamenti e riduce la loro dinamica vorticosa.

“Velcro” elettrostatico che blocca insieme i filamenti
Misurazioni biochimiche hanno rivelato che cytoFtsN e FtsZ interagiscono principalmente tramite cariche elettriche opposte: FtsZ è complessivamente negativo, mentre il peptide porta gruppi di cariche positive. A livelli di sale più bassi, il peptide si legava più fortemente, favoriva la formazione di fasci di FtsZ più spessi in soluzione e rallentava la degradazione dei filamenti attenuando l’attività GTP‑asica della proteina. Quando i ricercatori modificarono residui chiave carichi positivamente nel peptide, o aumentarono la concentrazione di sale per schermare l’attrazione elettrostatica, gli effetti di bundling e riorganizzazione scomparvero. Ciò indica un meccanismo fisico semplice per cui il peptide carico positivamente agisce come un “Velcro” molecolare, riducendo la repulsione tra i filamenti di FtsZ affinché possano impaccarsi fianco a fianco in fasci rigidi.
Come un singolo anello rimodella una vescicola gigante
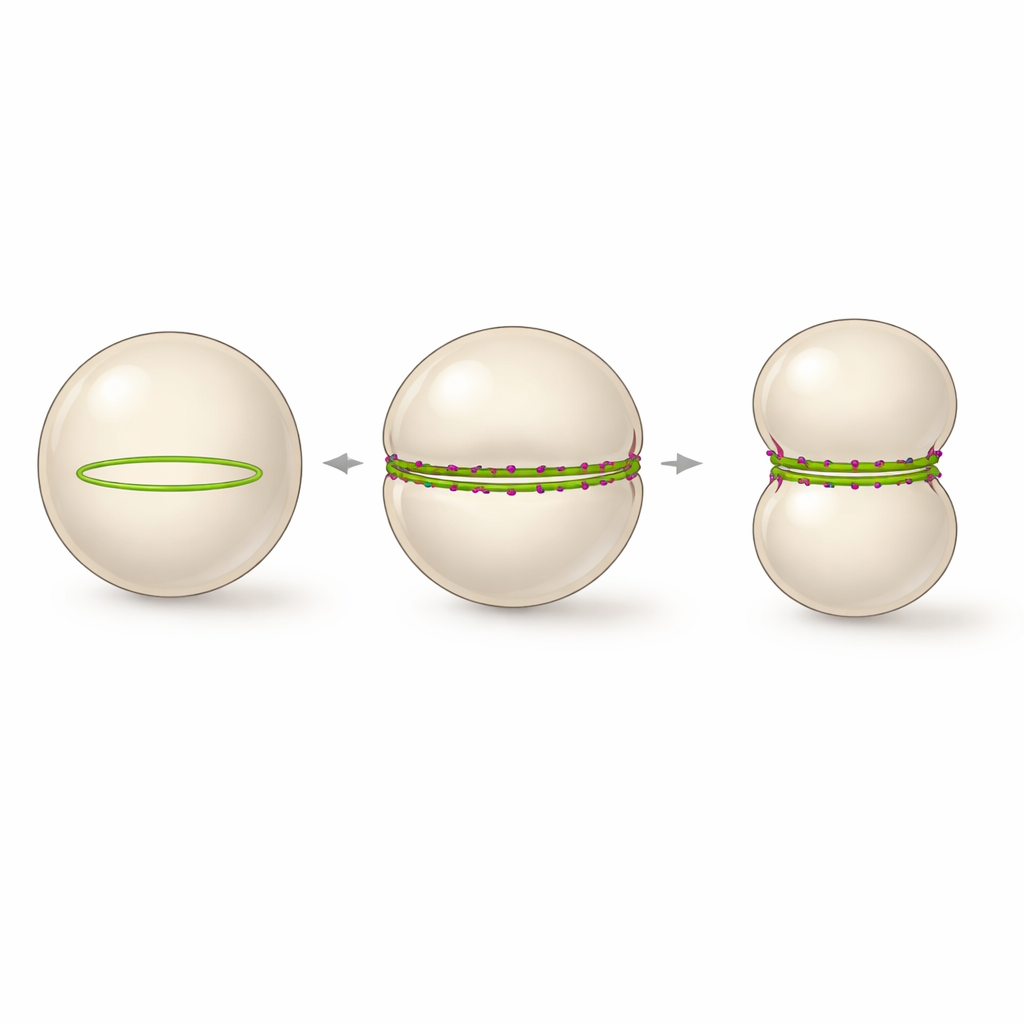
All’interno delle vescicole, questo bundling stabilizzato dal peptide ha una conseguenza notevole. Invece di molti piccoli anelli curvi, i fasci raddrizzati di FtsZ vengono costretti a seguire la grande curvatura della vescicola, assemblandosi in un unico anello continuo che percorre l’intera circonferenza. Le immagini in time‑lapse hanno mostrato che ogni volta che si formava un anello completamente chiuso, la vescicola si deformava in modo affidabile da sfera a bilobata, con una vita stretta dove l’anello era posizionato. Il processo poteva essere seguito in tempo reale mentre il diametro della vescicola si riduceva e la costrizione si approfondiva, quasi dividendo il compartimento in due, anche se la scissione finale non veniva raggiunta. Gli autori propongono che un anello di FtsZ stabile che attraversa l’equatore, con un turnover rallentato ma ancora attivo, sia l’architettura minimale necessaria per guidare una costrizione della membrana su larga scala in una cellula sintetica.
Cosa significa per la vita sintetica futura
Dimostrando che una variante di FtsZ ancorata alla membrana più un breve peptide cationico possono rimodellare vescicole lipidiche giganti quasi fino alla divisione, questo lavoro definisce una regola di progetto chiara per le cellule artificiali: un singolo anello proteico coerente che corrisponde alla dimensione della cellula ed è meccanicamente stabile nel tempo è sufficiente per pizzicare un confine soffice alla scala cellulare. Potrebbero comunque essere necessari fattori più complessi per tagliare completamente la membrana, ma lo studio dimostra che una costrizione controllata su larga scala non richiede il cast completo delle proteine di divisione batterica. Invece, la messa a punto dell’organizzazione e della dinamica dei filamenti può trasformare uno scaffold proteico semplice in un efficace anello contrattile, avvicinando di un passo le cellule sintetiche davvero auto‑divisive.
Citazione: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Parole chiave: divisione di cellule sintetiche, anello FtsZ, costrizione della membrana, divisoma minimale, auto-organizzazione del citoscheletro