Clear Sky Science · it
La proteomica subcellulare svela un progetto per l’integrazione dell’endosimbionte nel trypanosomatide Angomonas deanei
Partner nascosti all’interno della vita unicellulare
Molti organismi unicellulari non sono veramente soli. Alcuni ospitano batteri che vivono al loro interno come coinquilini permanenti, scambiando nutrienti e servizi in relazioni che ricordano le origini dei nostri mitocondri. Questo studio esplora una di queste collaborazioni in Angomonas deanei, un microscopico parassita degli insetti, per rivelare come un tempo batterio libero sia diventato profondamente integrato nel funzionamento interno della cellula ospite.
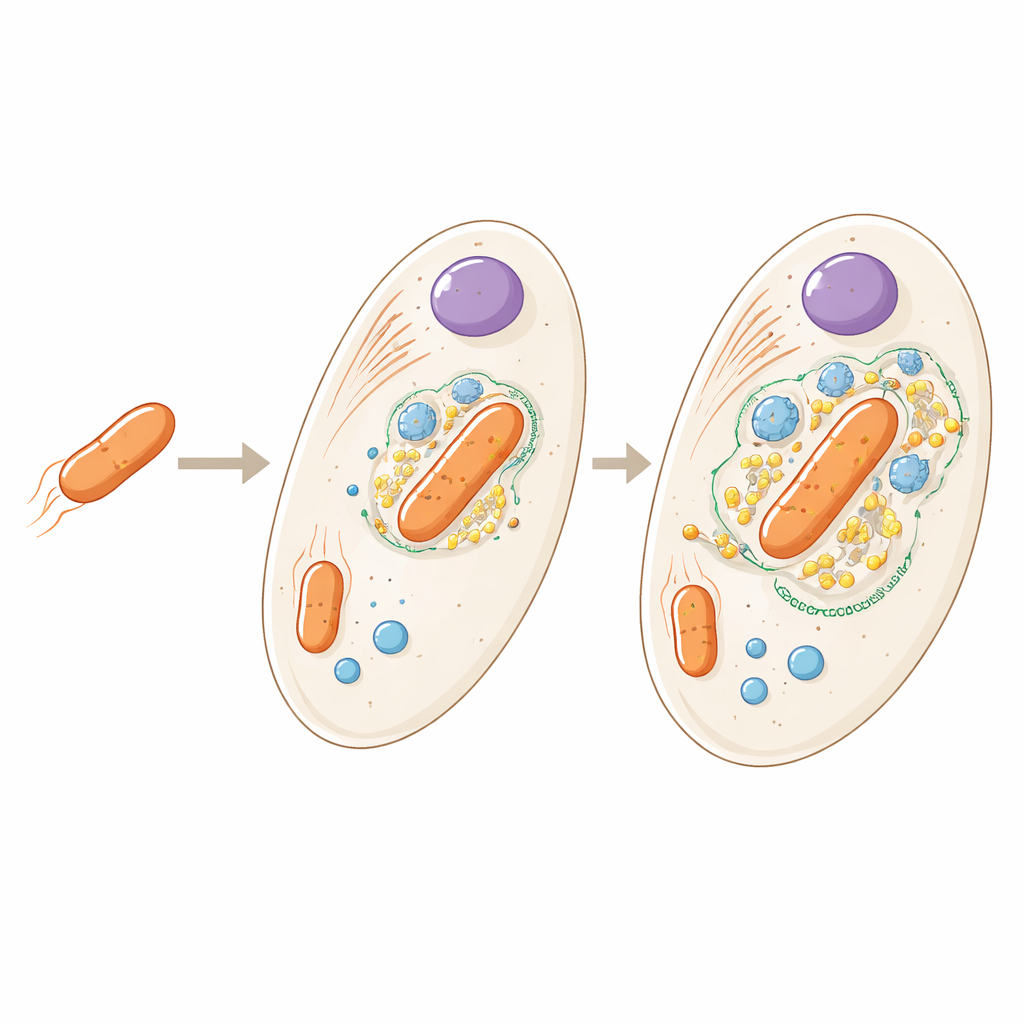
Da ospite a parte incorporata
Il batterio che vive all’interno di Angomonas deanei è un parente distante dei microrganismi di suolo liberi, ma qui esiste come copia singola per cellula ospite e non può più sopravvivere autonomamente. Lavori precedenti avevano mostrato che l’ospite produce proteine speciali che viaggiano dentro il batterio e perfino aiutano a controllare quando esso si divide. Il nuovo studio amplia la domanda: se osserviamo l’intera cellula, dove si trovano esattamente tutte le proteine dell’ospite e del batterio, e cosa ci dice questo su quanto strettamente i due partner sono integrati?
Mappare la città interna della cellula
Per rispondere, i ricercatori hanno aperto un gran numero di cellule in modo molto delicato in modo che le strutture interne rimanessero per lo più intatte. Hanno quindi separato questi componenti facendoli ruotare a diverse velocità e hanno identificato migliaia di proteine in ciascuna frazione usando spettrometria di massa ad alta risoluzione. Confrontando come le proteine si raggruppavano tra le frazioni e verificando con marker noti e microscopia a fluorescenza, hanno creato un dettagliato “libro degli indirizzi” della cellula, assegnando quasi 3.000 proteine a 21 regioni distinte come il nucleo, il mitocondrio, corpi specializzati di stoccaggio e l’endosimbionte batterico stesso.
Strumenti dell’ospite diretti contro il batterio convivente
All’interno di questa mappa, il team ha scoperto un insieme di proteine prodotte dall’ospite che viaggiano costantemente con l’endosimbionte, ampliando la collezione nota di proteine cosiddette targetizzate all’endosimbionte. Un nuovo esempio confermato, chiamato ETP10, riveste il batterio in modo simile a una proteina identificata in precedenza, suggerendo uno scheletro di fattori dell’ospite avvolto attorno al partner microbico. Un altro piccolo gruppo di proteine condivideva un comportamento fisico insolito con una proteina di tipo dinamina già nota per stringere il batterio durante la divisione. Insieme, questi risultati fanno pensare a una macchina specializzata costruita dall’ospite dedicata al posizionamento, alla modellazione e alla riproduzione dell’endosimbionte all’interno della cellula.
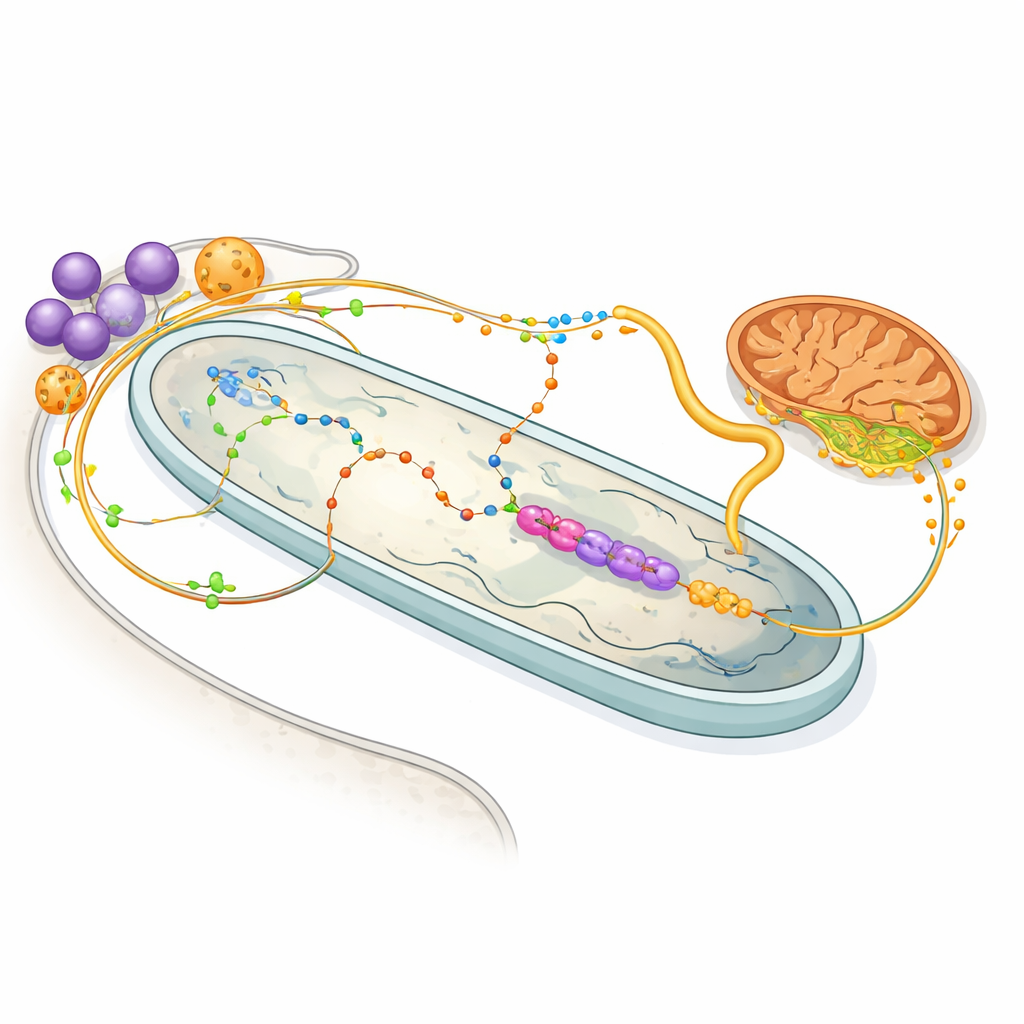
Condivisione energetica e rotte chimiche di scambio
La mappa delle proteine illumina anche il vivace scambio di molecole tra ospite e batterio. Gli enzimi nelle glicosome dell’ospite—organelli che gestiscono il metabolismo degli zuccheri e degli amminoacidi—sembrano sintonizzati per nutrire il batterio con l’amminoacido prolina e con il composto 2‑ossoglutarato, entrambi preziose fonti di energia. All’interno del batterio, un set semplificato di enzimi usa il 2‑ossoglutarato per generare NADH, che alimenta una catena respiratoria minima, quindi restituisce succinato al mitocondrio dell’ospite. Altri percorsi mostrano che il batterio esegue la maggior parte dei passaggi nella sintesi dell’eme, un pigmento vitale necessario all’ospite, contribuendo allo stesso tempo con elementi costitutivi cruciali per i nucleotidi. Di fatto, ciascun partner ha delegato compiti metabolici specifici all’altro, creando un sistema condiviso e interdipendente.
Nuove linee di comunicazione all’interno della cellula
Oltre al metabolismo, lo studio rivela legami fisici e probabilmente di segnalazione tra l’endosimbionte e altri organelli. Un gruppo distinto di proteine dell’ospite forma ciò che gli autori definiscono un cluster di “siti di contatto”, arricchito in componenti della membrana nucleare e del reticolo endoplasmatico che co-sedimentano fisicamente con il batterio. Due tipi di organelli di stoccaggio—glicosomi e acidocalcisomi—appaiono in due popolazioni: alcuni rimangono liberi nel citoplasma, mentre altri viaggiano costantemente col batterio. La microscopia conferma che sottogruppi di questi organelli si adagiano strettamente contro l’endosimbionte. Gli acidocalcisomi sono noti serbatoi di calcio e fosfato, quindi la loro stretta vicinanza suggerisce una via bidirezionale di segnalazione e traffico ionico che collega il batterio, questi depositi e il vicino reticolo endoplasmatico.
Un progetto per la vita fusa nella vita
Nel complesso, questo lavoro fornisce un ricco progetto a livello cellulare di come un batterio possa diventare funzionalmente fuso con il suo ospite senza essere ancora trasformato in un organello a pieno titolo come i mitocondri. Angomonas deanei dipende dall’endosimbionte per nutrienti chiave, mentre il batterio, a sua volta, dipende da proteine prodotte dall’ospite e da molecole ricche di energia ed è ancorato agli organelli dell’ospite per comunicazione e controllo. Per i non specialisti, la conclusione è che l’evoluzione può progressivamente codificare cooperazione tra forme di vita molto diverse, passo dopo passo, fino a rendere impossibile separarle. Questo sistema offre un’istantanea in vivo di quel processo in azione, aiutando gli scienziati a comprendere meglio come cellule complesse come la nostra siano nate da origini più semplici.
Citazione: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Parole chiave: endosimbiosi, metabolismo cellulare, evoluzione degli organelli, biologia dei protisti, interazioni ospite-microbo