Clear Sky Science · it
Lo stile di vita di Acinetobacter baumannii comprende la colonizzazione del suolo di materiale vegetale in decomposizione e la diffusione per via aerea
Perché il lato selvaggio di questo germe ospedaliero conta per voi
Acinetobacter baumannii è noto soprattutto come un germe ospedaliero difficile da eliminare, capace di resistere a molti antibiotici. Questo studio mostra che lo stesso microrganismo vive anche all’aperto in ambienti ricchi: nel suolo, nel materiale vegetale in decomposizione, negli animali e persino nell’aria. Identificando le sue sorgenti e i meccanismi di dispersione, il lavoro aiuta a spiegare perché questo batterio è così resistente e perché riesce ripetutamente a entrare negli ospedali di tutto il mondo.

Vita nascosta nei campi, nei fiumi e nei nidi di uccelli
I ricercatori sono partiti da un indizio inatteso: i pulcini di cicogna bianca in Polonia spesso ospitavano A. baumannii nelle vie aeree superiori, lontano da qualsiasi ospedale. Seguendo la dieta e l’ambiente degli uccelli, il team ha ricondotto il batterio non agli insetti o ai pesci, ma soprattutto ai piccoli mammiferi, ai lombrichi e — cosa più importante — ai suoli umidi ricchi di materiale vegetale in decomposizione lungo i fiumi e nei cumuli di compost. I suoli forestali, anche lungo i corsi d’acqua, raramente contenevano il batterio, mentre le rive fluviali fuori dalle foreste talvolta funzionavano da “hot spot” dove coesistevano fianco a fianco molteplici ceppi diversi.
Dal materiale vegetale in decomposizione all’aria aperta
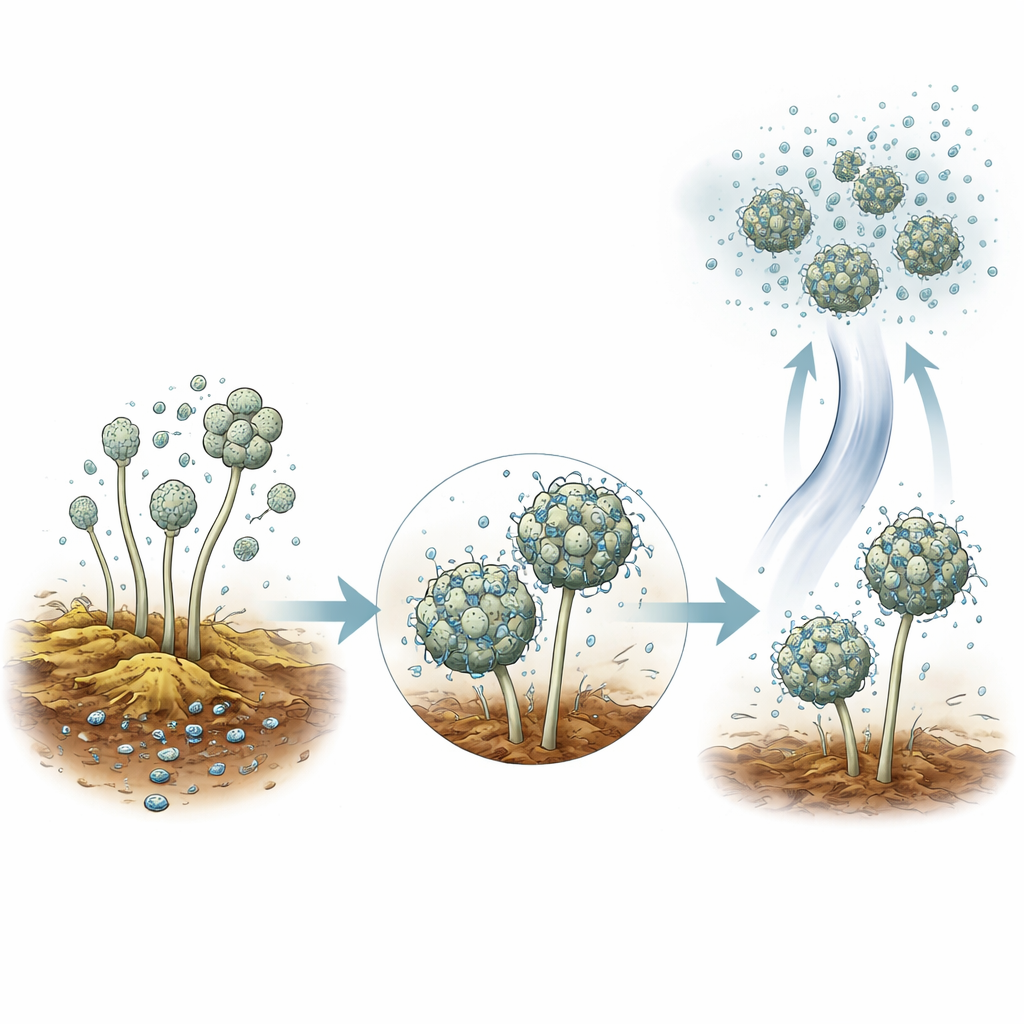
Esperimenti sul campo hanno mostrato che A. baumannii è attratto dal materiale vegetale in decomposizione. Quando gli autori hanno collocato ritagli vegetali sterilizzati in giardini, il materiale è stato colonizzato entro poche settimane — anche quando era sollevato dal suolo e accessibile solo attraverso l’aria. Trappole per l’aria posizionate appena sopra cumuli di compost attivi hanno raccolto anch’esse il batterio. In laboratorio il team ha scoperto che A. baumannii si lega facilmente alle spore di muffe comuni come Aspergillus e Penicillium. I batteri rivestivano gradualmente le spore e ne rallentavano persino la capacità di germinare. Poiché le spore fungine si aerosolizzano facilmente da compost e suoli, questa stretta associazione offre un modo semplice per il batterio di "prendere un passaggio" nell’atmosfera.
Viaggiatori globali con radici antiche
Per capire come questi ceppi selvatici si relazionano ai ceppi ospedalieri, il team ha sequenziato 401 nuovi genomi provenienti da cicogne, suolo, piante, lombrichi, roditori e altre fonti, e li ha confrontati con centinaia di genomi disponibili pubblicamente. L’albero genealogico risultante ha rivelato una diffusione notevole: isolati ambientali, animali e clinici umani erano sparsi sugli stessi rami, spesso diversi di solo pochi cambiamenti nel DNA. Alcuni parenti quasi identici sono stati trovati su continenti diversi, implicando che le stesse linee si siano spostate across gli oceani in poche decadi. In base al tasso di accumulo delle mutazioni, gli autori stimano che A. baumannii come specie sia sorprendentemente giovane — dell’ordine di 15.000 anni — e abbia subito una rapida diversificazione attorno al periodo in cui gli esseri umani hanno iniziato l’agricoltura su larga scala e la disboscazione.
Un vasto kit di adattamento, ma scarsa impronta umana in natura
Combinando tutti i genomi, i ricercatori hanno stimato che il set genico complessivo della specie — o pan-genoma — contiene circa 51.000 famiglie geniche distinte, più del doppio delle stime precedenti. Questo enorme arsenale genetico probabilmente sottende la sua capacità di adattarsi a condizioni di estrema secchezza, radiazioni, disinfettanti e antibiotici. Eppure la maggior parte degli isolati provenienti da fauna selvatica e suolo portava solo un piccolo numero di geni di resistenza riconosciuti e pochi elementi di DNA mobili, in contrasto con i ceppi ospedalieri che sono carichi di tali caratteristiche. Questo schema suggerisce che le popolazioni naturali campionate siano ancora relativamente poco influenzate dall’uso moderno di antibiotici, offrendo una visione di "base" della specie prima della piena adattazione ospedaliera.
Cosa significa per gli ospedali e la sanità pubblica
Lo studio ritrae A. baumannii non come un problema puramente creato dall’uomo, ma come un batterio naturalmente aerodisperso, associato a piante e suolo, che solo recentemente ha iniziato a sfruttare ospedali e allevamenti come nuovi habitat. La sua associazione con i funghi, la tolleranza a condizioni avverse e la vasta diversità genetica lo rendono adatto ai viaggi atmosferici a lunga distanza e all’evoluzione rapida. Per un lettore non specialista, la conclusione è che il controllo delle infezioni non può concentrarsi solo sulla trasmissione paziente-paziente all’interno degli ospedali. Picchi stagionali, ambienti interni contaminati da muffe, impianti di compostaggio e i cambiamenti nell’uso del territorio contribuiscono tutti a determinare quando e come questo germe resiliente entra negli ambienti umani — e comprendere il suo stile di vita all’aperto è fondamentale per anticipare future varianti resistenti ai farmaci.
Citazione: Wilharm, G., Skiebe, E., Michalska, A. et al. Acinetobacter baumannii’s lifestyle includes soil-dwelling colonization of decaying plant material and airborne spread. Nat Commun 17, 2316 (2026). https://doi.org/10.1038/s41467-026-70072-4
Parole chiave: Acinetobacter baumannii, batteri aerodispersi, microbioma del suolo, resistenza agli antibiotici, One Health