Clear Sky Science · it
La distribuzione dinamica delle amplificazioni tandem genetiche in una popolazione eteroresistente di Escherichia coli rivelata da sequenziamento ultra-profondo a letture lunghe
Anfratti nascosti di sopravvivenza
Quando i medici trattano infezioni batteriche con antibiotici, presumono che l’intero sciame microbico risponda allo stesso modo. Ma a volte, una frazione minuscola della popolazione resiste silenziosamente, sopravvive al trattamento e prepara il terreno per un insuccesso o una ricaduta. Questo studio svela come tali rari sopravvissuti emergano e cambino nel tempo in Escherichia coli, e introduce un metodo potente per osservare questi cambiamenti genetici molecola per molecola.
Piccole ripetizioni genetiche, grandi conseguenze
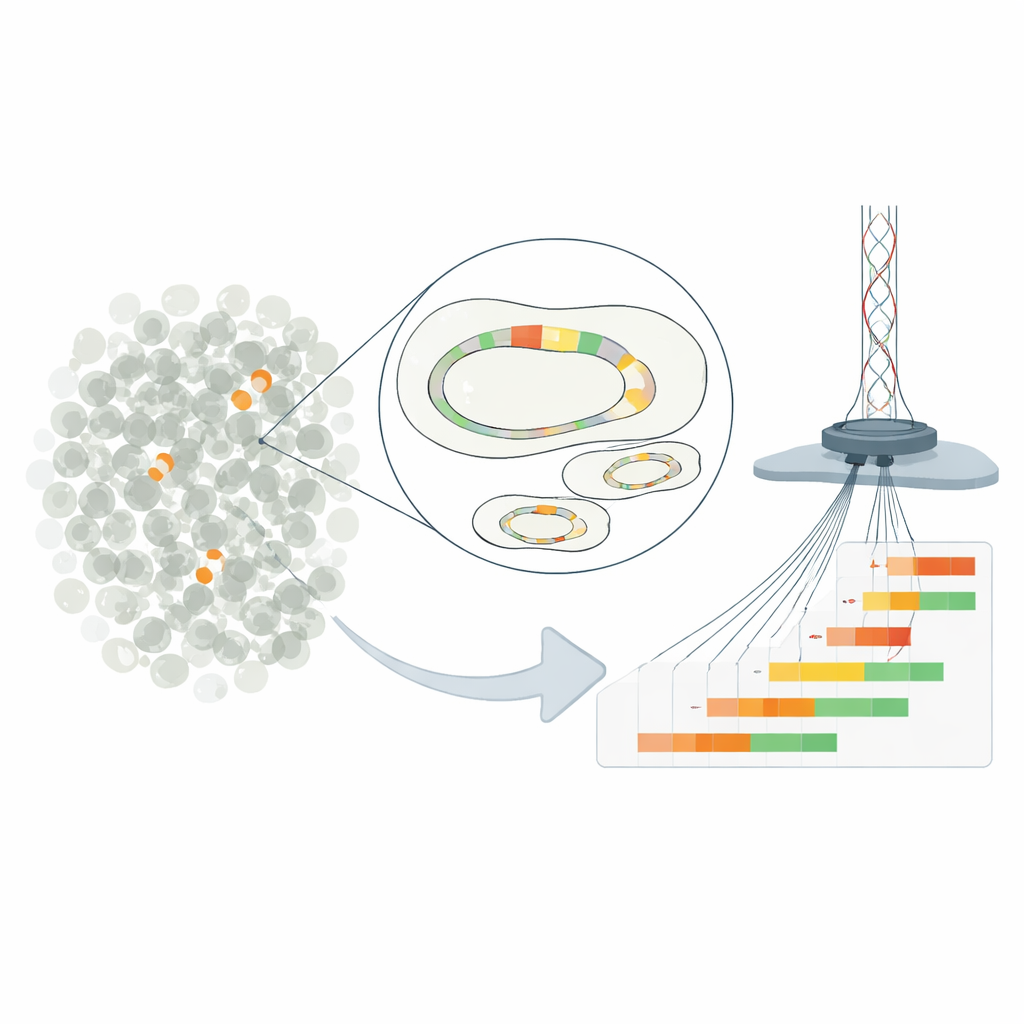
Il lavoro si concentra sull’“eteroresistenza”, una situazione in cui la maggior parte dei batteri in un campione sembra suscettibile a un farmaco, mentre una piccola minoranza può resistere a dosi molto più elevate. Nel ceppo di E. coli studiato, questo comportamento deriva da copie ripetute di un gene di resistenza portato su un plasmide — un piccolo cerchio di DNA separato dal cromosoma principale. Duplicando un breve segmento di DNA contenente un gene per una beta-lattamasi, i batteri possono aumentare la produzione di un enzima che inattiva l’antibiotico piperacillina-tazobactam. Più ripetizioni contiene una cellula, più enzima produce e maggiori sono le sue possibilità di sopravvivenza in presenza del farmaco.
Leggere i cerchi di DNA con dettaglio senza precedenti
I metodi tradizionali possono solo stimare il numero medio di copie geniche sull’intera popolazione batterica, mascherando la ricca diversità tra singole cellule. Per superare questo limite, i ricercatori hanno ingegnerizzato il plasmide clinico in modo da poterlo tagliare in un punto preciso e poi isolare dal resto del genoma. Hanno usato il sequenziamento Nanopore ultra-profondo a letture lunghe per leggere le molecole plasmidiche per intero, conteggiando esattamente quante unità di resistenza ripetute ciascuna contenesse. Questo approccio ha raggiunto una risoluzione fino a una cellula su 100.000, rivelando plasmidi con zero fino a oltre una dozzina di copie geniche che coesistono nella stessa coltura. Controlli con altre tecniche hanno confermato che, in media, il nuovo metodo riportava numeri di copie accurati.
Come gli antibiotici rimodellano la popolazione
Con questo strumento a disposizione, il team ha seguito cosa accadeva quando esponevano colture di E. coli a dosi crescenti di piperacillina-tazobactam e poi rimuovevano il farmaco. Con l’aumento dei livelli di antibiotico, la distribuzione complessiva si è spostata verso plasmidi con più copie del gene di resistenza, ma le cellule con meno copie non sono mai scomparse del tutto. Quando il farmaco è stato ritirato e i batteri sono stati coltivati per centinaia di generazioni, la popolazione è tornata gradualmente verso numeri di copie più bassi senza però ripristinare completamente lo stato iniziale. Test di crescita separati hanno mostrato che ogni copia genica aggiuntiva conferiva un aumento misurabile della tolleranza al farmaco, collegando strettamente le distribuzioni genetiche osservate al fenotipo di eteroresistenza visibile nei saggi di laboratorio standard.

Protezione dai vicini e costi silenziosi
Per spiegare perché le cellule a basso numero di copie persistevano anche sotto trattamento intenso, gli autori hanno costruito un modello matematico che combinava crescita batterica, degradazione dell’antibiotico e gli eventi probabilistici che aggiungono o rimuovono copie geniche. Le simulazioni hanno mostrato che la “resistenza indiretta” gioca un ruolo chiave: le cellule altamente resistenti rilasciano sufficiente beta-lattamasi da abbassare la concentrazione di farmaco nell’ambiente condiviso, proteggendo incidentalmente i vicini meno resistenti. Finché le copie geniche extra impongono solo un piccolo costo di crescita in assenza di farmaco, questo effetto protettivo aiuta a mantenere un’ampia dispersione dei numeri di copie, rallentando il ritorno a una popolazione completamente suscettibile. Il modello ha anche mostrato come l’adattamento ordinario al mezzo di crescita — mutazioni non correlate che migliorano la crescita — possa fissare particolari stati di numero di copie rendendo alcune sottopopolazioni più adatte di altre.
Perché questo conta per i pazienti e oltre
Per i non specialisti, il messaggio è che una coltura batterica non è un nemico uniforme: è un miscuglio in costante evoluzione di individui con diverse capacità di sopravvivere agli antibiotici. Contando direttamente le copie geniche su migliaia di singole molecole di DNA, questo studio collega in modo quantitativo quella diversità nascosta alla resistenza rilevante per il trattamento. Tali intuizioni potrebbero migliorare l’uso del sequenziamento genomico per prevedere l’eteroresistenza difficile da rilevare, aiutare a identificare ceppi batterici particolarmente inclini a causare fallimenti terapeutici e guidare test diagnostici migliori. Poiché le amplificazioni geniche in tandem guidano anche l’adattamento rapido in virus, tumori e altri organismi, la stessa strategia potrebbe essere adattata ben oltre E. coli, offrendo una nuova finestra su come frammenti ripetuti di DNA aiutino la vita a eludere le minacce.
Citazione: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Parole chiave: eteroresistenza agli antibiotici, amplificazione genica, Escherichia coli, sequelazione a letture lunghe, beta-lattamasi