Clear Sky Science · it
I movimenti di molecola singola rivelano che il solo legame dell’ATP alimenta la traslocazione del substrato da parte di un trasportatore ABC
Perché contano le piccole pompe cellulari
Ogni cellula del tuo corpo dipende da macchine microscopiche che spostano molecole attraverso le membrane, determinando tutto, dall’assorbimento di nutrienti alla difesa immunitaria. Una classe importante di queste macchine, chiamata trasportatori ABC, usa il carburante chimico della cellula, l’ATP, per spingere il carico contro i gradienti naturali. Eppure per decenni gli scienziati hanno dibattuto su una questione fondamentale: è il solo legame dell’ATP a fornire l’energia per il passaggio del substrato, o l’energia viene rilasciata solo quando l’ATP viene scisso? Questo studio si concentra su un singolo trasportatore, molecola per molecola, per risolvere il dibattito.
Osservare un trasportatore alla volta
Invece di misurare il comportamento combinato di milioni di molecole, i ricercatori hanno costruito un sistema che permette loro di seguire eventi di trasporto individuali in tempo reale. Si sono concentrati su TmrAB, un cugino batterico del trasportatore umano TAP che carica peptidi immunitari per la presentazione alle cellule T citotossiche. TmrAB è inserito in una membrana e trasporta brevi frammenti proteici (peptidi) da un lato all’altro usando ATP. Per osservare ogni singolo passaggio di trasporto, il team ha intrappolato una singola molecola di TmrAB in una bolla di membrana artificiale (una liposoma) e ha racchiuso dentro quella bolla un proteina "sensore" appositamente ingegnerizzata che cambia la sua fluorescenza quando cattura un peptide. Usando un microscopio altamente sensibile, hanno potuto così vedere, come brevi salti nel segnale luminoso, i momenti esatti in cui un peptide dopo l’altro arrivava all’interno della bolla.
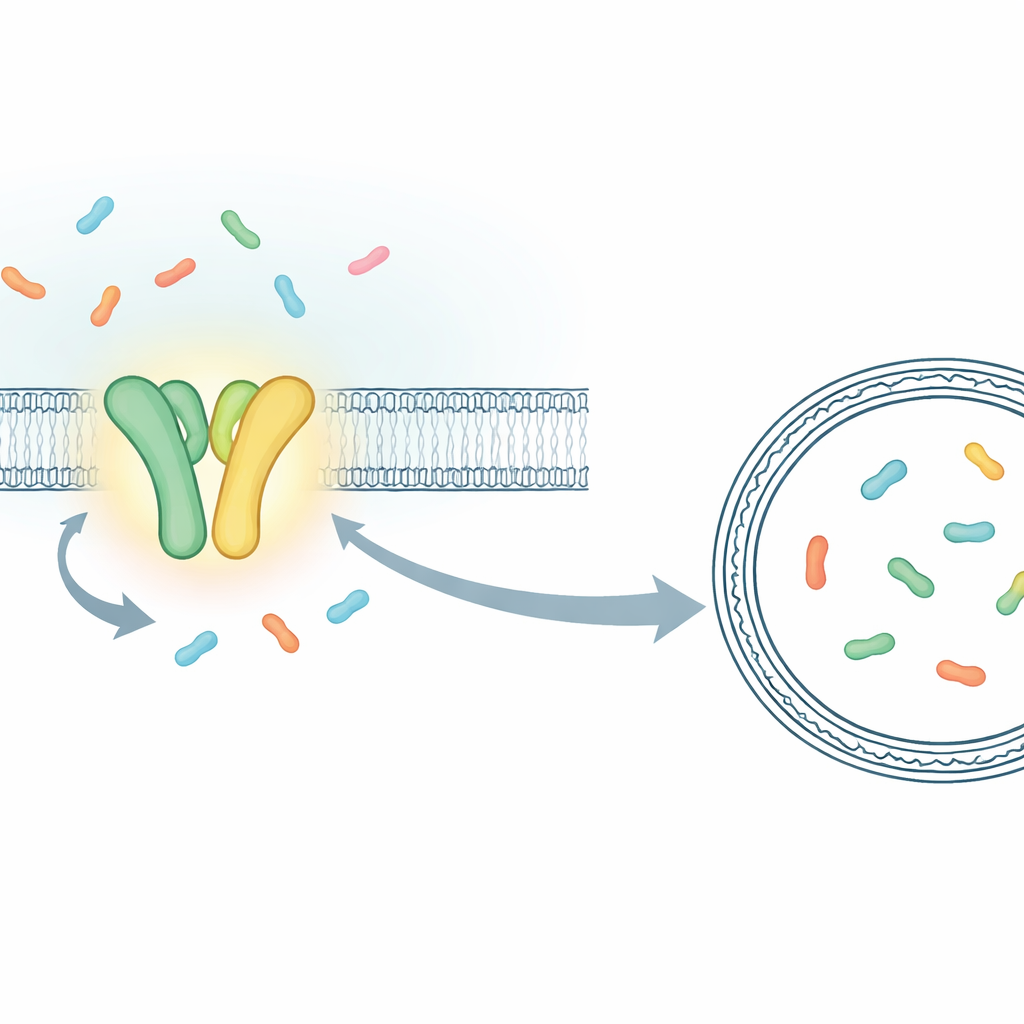
Dimostrare che un legame di ATP muove un peptide
Con questo saggi a molecola singola a disposizione, i ricercatori hanno confrontato il TmrAB normale con una versione modificata a turnover lento i cui cicli sono dilatati nel tempo. La variante lenta ha reso possibile distinguere singoli eventi che altrimenti si sovrapporrebbero. Hanno mostrato che quando ATP e peptidi erano presenti insieme, il sensore dentro il liposoma passava dal suo stato "vuoto" a quello "caricato" in passi discreti, ciascuno coerente con il trasporto di un singolo peptide. Analizzando la velocità con cui il sensore si chiudeva attorno ai peptidi e stimando il minuscolo volume all’interno di ogni liposoma, sono riusciti persino a tradurre questi cambiamenti di luce in concentrazioni approssimative di peptide. I numeri corrispondevano a quanto ci si aspetterebbe se uno, poi due peptidi si accumulassero in bolle di circa 100 nanometri di diametro, confermando che stavano contando gli eventi di trasporto uno per uno.
Il solo legame dell’ATP fa scattare l’interruttore molecolare
La controversia chiave riguarda gli ioni magnesio (Mg2+), che normalmente accompagnano l’ATP nelle cellule e sono noti per essere necessari per la scissione efficiente dell’ATP. Alcuni modelli suggerivano che il Mg2+ potesse essere richiesto anche per il legame dell’ATP o per la chiusura del trasportatore. Per separare questi ruoli, i ricercatori hanno rimosso il Mg2+ usando un agente chelante ma hanno comunque fornito ATP. In queste condizioni, sia il trasportatore normale sia quello lento sono stati in grado di effettuare esattamente un passaggio di trasporto del peptide per molecola, per poi fermarsi. Questo comportamento indica che l’ATP può comunque legarsi e costringere il trasportatore a passare da una conformazione rivolta verso l’interno a una rivolta verso l’esterno e a muovere un peptide, anche senza Mg2+. Tuttavia, senza Mg2+ il trasportatore non può scindere efficacemente l’ATP e quindi non può resettarsi per un altro ciclo.
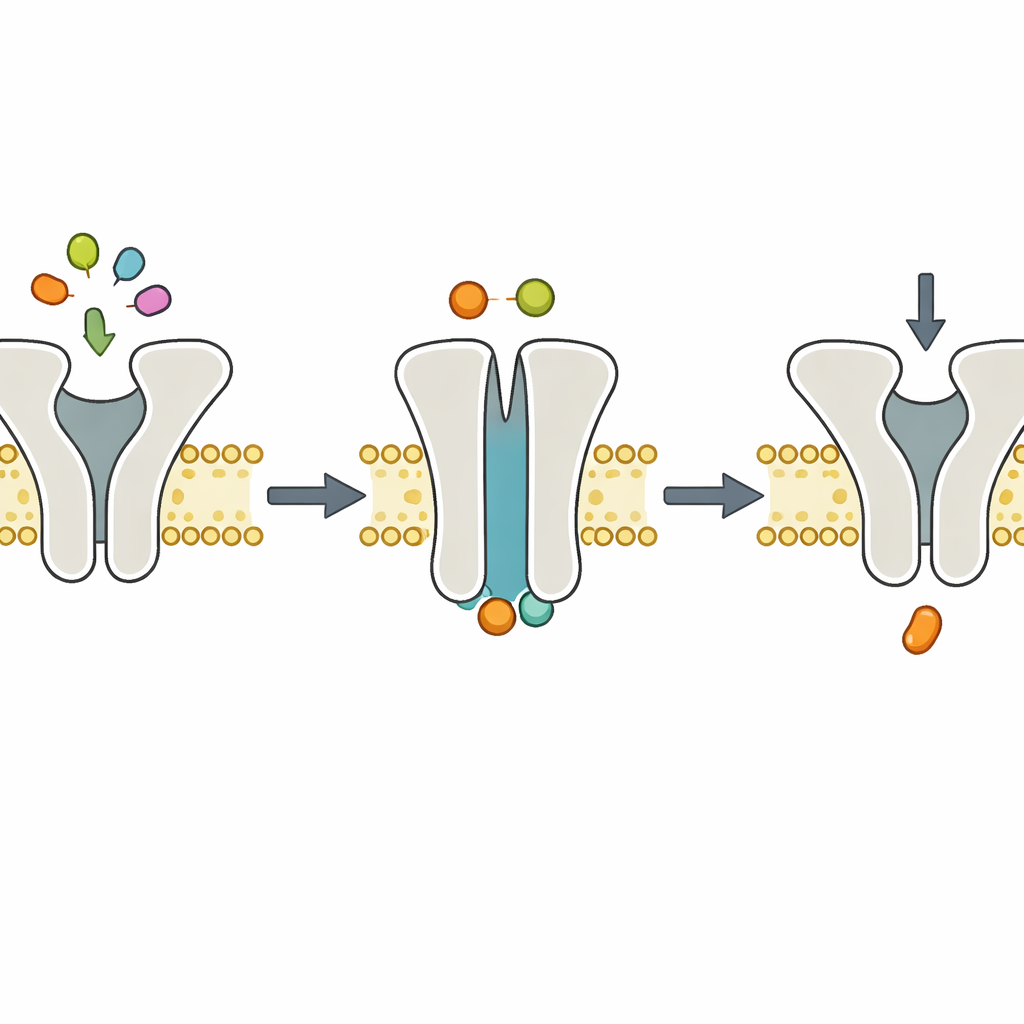
Istanti strutturali confermano la dinamica
Per vedere l’aspetto della macchina durante questo passaggio senza Mg2+, il team ha ricorso alla crio–microscopia elettronica, che fotografa molecole rapidissime congelate con dettaglio quasi atomico. Hanno ricostituito TmrAB in nanodischi lipidici, aggiunto ATP senza Mg2+ e congelato i complessi. Le strutture risultanti mostravano TmrAB in una conformazione rivolta verso l’esterno, "occlusa", con ATP incastrato in entrambe le sue tasche di legame interne, ma senza Mg2+ visibile. Questi istantanee erano sostanzialmente indistinguibili da strutture precedenti ottenute con ATP e Mg2+ presenti. Insieme agli saggi biochimici che mostrano come la scissione dell’ATP si arresti completamente senza Mg2+, le immagini supportano una semplice divisione dei compiti: il legame dell’ATP guida il cambio conformazionale che muove il peptide, mentre l’idrolisi dell’ATP dipendente da Mg2+ esegue il passo di recupero.
Un quadro più chiaro del funzionamento delle pompe cellulari
Osservando trasportatori singoli e risolvendo le loro strutture, questo lavoro risolve una domanda di lunga data sui trasportatori ABC: la corsa meccanica che sposta un peptide è innescata dal legame stesso dell’ATP, non dalla successiva scissione chimica dell’ATP. Il Mg2+ entra in gioco principalmente per permettere la scissione dell’ATP, che a sua volta resetta il trasportatore così che possa funzionare di nuovo. Oltre a chiarire un aspetto fondamentale della biologia cellulare, questo approccio a molecola singola offre una linea guida per scomporre altre macchine di membrana che sottendono l’immunità, la resistenza ai farmaci e molte malattie—una molecola e un passaggio di trasporto alla volta.
Citazione: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Parole chiave: Trasportatori ABC, Legame dell’ATP, FRET a molecola singola, trasporto di membrana, TAP e TmrAB