Clear Sky Science · it
Nanoparticelle di blu di Prussia mirate contro la PANoptosi mediata da più PANoptosomi per la terapia del danno ischemia-riperfusione miocardica
Perché proteggere il cuore in guarigione è importante
Quando una persona ha un infarto, i medici si affrettano a riaprire l’arteria bloccata e ripristinare il flusso sanguigno. Questo intervento salvavita, tuttavia, ha un costo nascosto: il ritorno improvviso dell’ossigeno può danneggiare il cuore, uccidere cellule e predisporre all’insufficienza cardiaca. Questo studio esplora una nanomedicina innovativa che mira a proteggere il cuore durante questa finestra vulnerabile bloccando contemporaneamente diverse vie intrecciate di morte cellulare, potenzialmente favorendo recuperi più gentili dopo un infarto.
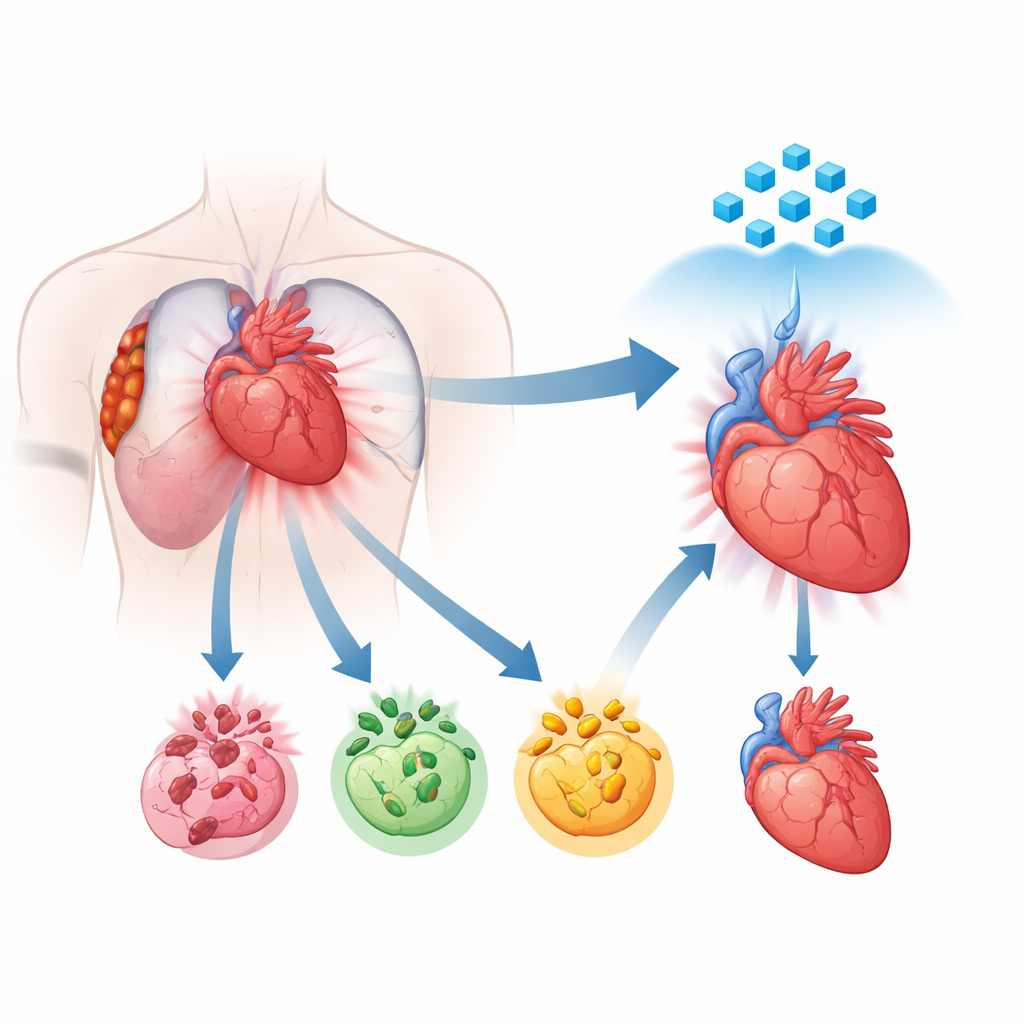
Una nuova prospettiva su come muoiono le cellule cardiache
Per anni gli scienziati hanno saputo che le cellule cardiache danneggiate possono morire attraverso diverse vie programmate, tra cui apoptosi, necroptosi e piroptosi. Ognuna segue il proprio copione molecolare, ma prove crescenti mostrano che queste vie non operano isolatamente. Piuttosto, comunicano tra loro e possono unirsi in un processo combinato e incontrollato chiamato PANoptosi. In questo stato, diversi programmi di morte si attivano insieme, rendendo frustrantemente deboli le terapie che bloccano una sola via. Gli autori hanno usato il sequenziamento dell’RNA a singolo nucleo su tessuto cardiaco umano di pazienti con infarti recenti per mappare dove e quanto intensamente questi programmi di morte sono attivati. Hanno rilevato che nelle aree più danneggiate le cellule del muscolo cardiaco mostravano uno spostamento potente verso questa modalità di morte combinata, indicando la PANoptosi come un motore centrale del danno.
Progettare un piccolo strumento multiuso per il cuore ferito
Per affrontare un processo così complesso, il team si è rivolto al blu di Prussia, un composto medico approvato da tempo noto soprattutto come antidoto per alcuni avvelenamenti da metalli. Alla scala nanometrica, le particelle di blu di Prussia si comportano come piccoli robot catalitici in grado di spegnere molecole nocive e influenzare il comportamento cellulare. Tramite simulazioni al computer, i ricercatori hanno mostrato che queste nanoparticelle potrebbero legarsi direttamente a tre nodi proteici chiave—RIPK1, ZBP1 e AIM2—che aiutano ad assemblare la macchina molecolare della PANoptosi. Legandosi a questi nodi in modi diversi, le particelle erano previste interferire con la costruzione dei complessi che inducono la morte e coordinano le tre vie di morte cellulare.
Dirigere le nanoparticelle direttamente sul tessuto cardiaco danneggiato
Le nanoparticelle funzionano solo se raggiungono il posto giusto, quindi il team ha rivestito le particelle di blu di Prussia con membrane naturali ottenute da piastrine, le cellule del sangue che si dirigono verso i vasi lesionati. Questo rivestimento ha creato PB@PM, un vettore biomimetico che circola come una piastrina ma consegna un carico terapeutico. In topi sottoposti a un infarto controllato e alla riapertura dell’arteria, le immagini hanno mostrato che PB@PM si accumulava molto più intensamente nella regione cardiaca danneggiata rispetto alle particelle non rivestite, evitando in gran parte gli organi sani. È importante che le particelle rivestite siano state ben tollerate: esami del sangue e analisi tissutali non hanno rivelato tossicità evidente, sostenendo il loro potenziale per uno sviluppo successivo.
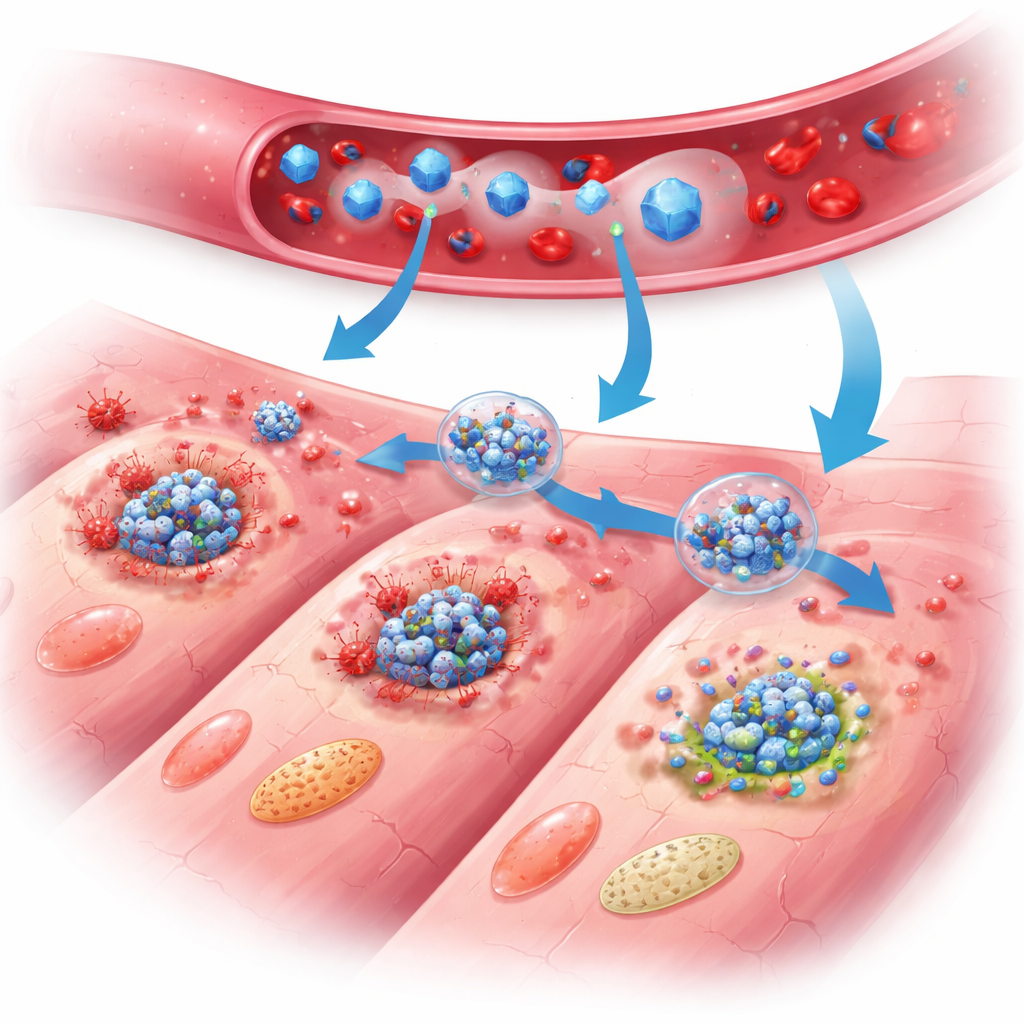
Come lo nano-scudo protegge il cuore
Nei topi trattati, i benefici di PB@PM sono diventati evidenti nel corso di giorni e settimane. La funzione di pompaggio cardiaco è migliorata, la dimensione della cicatrice si è ridotta e lo spessore della parete cardiaca è diminuito meno rispetto agli animali non trattati. Studi tissutali dettagliati hanno rivelato meno cellule cardiache in morte, cellule infiammatorie più calme e tessuto riparativo meglio strutturato con una crescita vascolare più sana e meno ingrandimento anomalo delle cellule sopravvissute. A livello molecolare, profili di espressione genica ampi e misurazioni proteiche hanno mostrato che PB@PM ha attenuato le tre principali vie di morte programmata contemporaneamente, ha interrotto l’assemblaggio dei complessi multiproteici della PANoptosi e ha ridotto i livelli di molecole di segnalazione che alimentano l’infiammazione. Le particelle hanno anche eliminato specie reattive dell’ossigeno dannose, stabilizzato i mitocondri—le centrali energetiche della cellula—e ripristinato un metabolismo energetico più normale, rimuovendo trigger chiave che altrimenti spingerebbero le cellule verso l’autodistruzione.
Cosa potrebbe significare per la cura degli infarti in futuro
In termini semplici, questo lavoro mostra che una nanoparticella ingegnosamente progettata può fungere da scudo multifrontale per il cuore, attenuando un groviglio di segnali di morte distruttivi invece di inseguire una via alla volta. Mirando al tessuto cardiaco lesionato, legandosi a proteine di controllo centrali e alleviando stress ossidativo e infiammatorio, PB@PM ha ridotto drasticamente la reazione a catena di perdita cellulare e formazione di cicatrici che spesso segue la riapertura di un’arteria ostruita. Sebbene siano necessari molti test prima che questa strategia possa raggiungere i pazienti, lo studio offre una prova di principio che prendere di mira la PANoptosi nel suo insieme—e farlo con particelle intelligenti ispirate a sistemi biologici—potrebbe aprire un nuovo capitolo nella protezione del cuore dopo un infarto.
Citazione: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Parole chiave: ischemia miocardica riperfusione, terapia con nanoparticelle, morte cellulare programmata, infiammazione cardiaca, protezione mitocondriale