Clear Sky Science · it
RPA stimola direttamente la processività dell’elicasa Mer3 per garantire la formazione normale dei crossover durante la meiosi
Come le cellule rimescolano il DNA per creare ovuli e spermatozoi sani
Ogni volta che una pianta, un animale o un essere umano produce ovuli o spermatozoi, le cellule devono rimescolare i cromosomi in modo che ogni discendente riceva una nuova combinazione di DNA parentale. Questo rimescolamento genetico dipende da scambi di DNA posizionati con precisione, o crossover, tra le coppie di cromosomi. Lo studio in primo piano rivela come due proteine chiave, Mer3 e RPA, lavorino insieme come una macchina microscopica per garantire che questi crossover si formino in modo efficiente e sicuro — un processo con implicazioni per la fertilità, l’evoluzione e forse anche per il cancro.
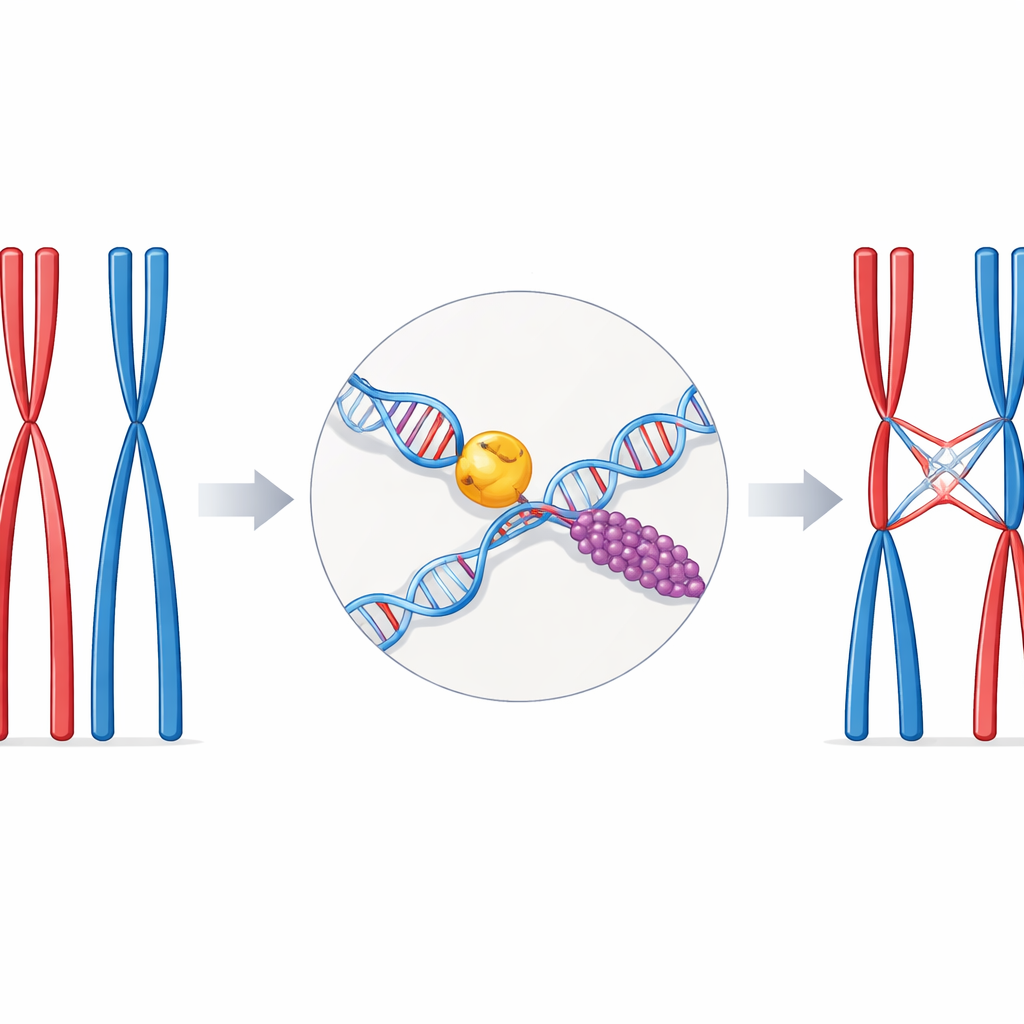
Un delicato equilibrio nella riproduzione sessuata
Durante la divisione cellulare speciale chiamata meiosi, i cromosomi si presentano in coppie corrispondenti, una proveniente da ciascun genitore. Perché queste coppie si separino correttamente, devono essere collegate fisicamente in alcuni punti ben scelti lungo la loro lunghezza. Questi legami sono i crossover — porzioni in cui i filamenti di DNA di un cromosoma vengono scambiati con quelli del partner. Avere troppo pochi crossover aumenta il rischio di mancata segregazione dei cromosomi e infertilità; averne troppi o mal posizionati può danneggiare il genoma. Le cellule si affidano quindi a vie di riparazione specializzate e a proteine ausiliarie per trasformare una pericolosa rottura del DNA in un crossover controllato e adeguato.
Incontra Mer3 e RPA, una coppia che srotola il DNA
I ricercatori si sono concentrati su Mer3, un motore molecolare che srotola il DNA e favorisce la formazione dei crossover. Il suo equivalente umano, HFM1, è noto per essere importante per la fertilità. Hanno scoperto che Mer3 si lega direttamente a RPA, un complesso proteico che normalmente riveste il DNA a singolo filamento esposto per proteggerlo e reclutare altri fattori di riparazione. Usando test biochimici, modellizzazione strutturale e saggi di interazione, il team ha mappato un sito di aggancio specifico dove una corta coda di Mer3 si inserisce in una scanalatura di una subunità di RPA. Questa interfaccia è conservata dal lievito ai mammiferi, suggerendo che si tratti di una soluzione evolutiva a lungo usata per controllare la riparazione del DNA durante la meiosi.
Osservare in azione un singolo motore del DNA
Per capire cosa fa concretamente questa collaborazione, gli scienziati hanno usato pinzette magnetiche a singola molecola — uno strumento che mantiene un singolo forcina di DNA come una piccola molla e misura come una singola molecola di Mer3 la srotola nel tempo. Hanno scoperto che Mer3 si muove lungo il DNA a velocità costante anche da sola. Ma in condizioni che imitano la relativamente bassa tensione fisica all’interno delle cellule, Mer3 tende a staccarsi dal DNA dopo aver srotolato solo un breve tratto. Quando è presente una piccola quantità di RPA, Mer3 diventa improvvisamente molto più persistente: può srotolare tratti di DNA molto più lunghi senza cadere, specialmente quando il DNA è incline a ripiegarsi su se stesso. Una versione mutante di Mer3 progettata per interrompere la coda di legame a RPA non acquisisce questa maggiore capacità di permanenza, rivelando che è il contatto diretto con RPA a potenziare la processività di Mer3.
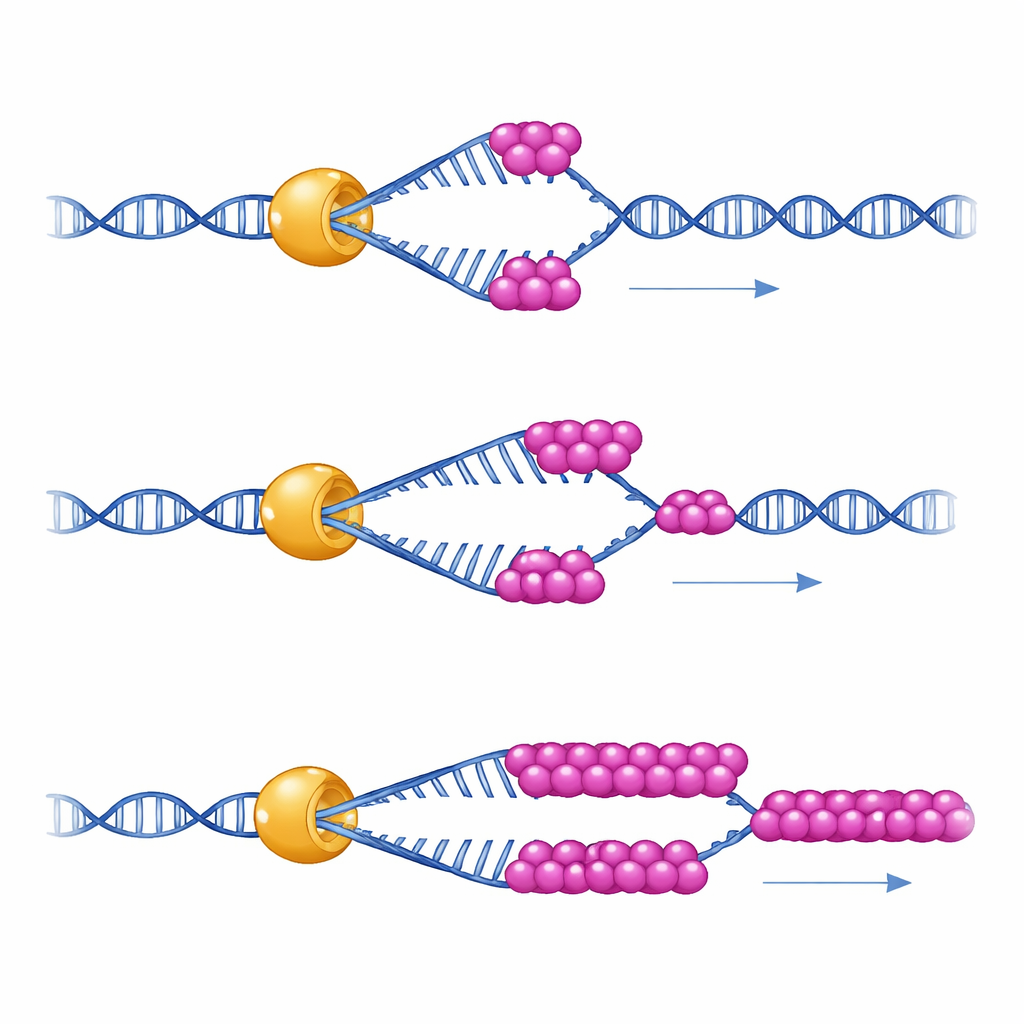
Conseguenze per i crossover nelle cellule viventi
Il team ha quindi chiesto cosa accade in cellule di lievito reali quando Mer3 non riesce ad agganciarsi correttamente a RPA. Hanno sostituito il gene MER3 normale con il mutante incapace di legare RPA e monitorato la meiosi. Queste cellule riuscivano ancora a dividersi e a formare spore, ma la loro fertilità è diminuita e il numero complessivo di crossover in alcune regioni cromosomiche è calato. Analisi dettagliate del DNA hanno mostrato un aumento degli eventi di riparazione che terminano come non‑crossover e un accumulo di intermedi di ricombinazione non risolti. La mappatura genomica della posizione di Mer3 ha rivelato che la proteina mutante veniva reclutata meno stabilmente nei siti dove avvengono rotture del DNA programmate, nonostante la sua associazione iniziale con gli assi cromosomici sembrasse normale. In altre parole, senza un forte legame con RPA, Mer3 non rimane abbastanza a lungo nei siti di rottura da guidarli in modo affidabile verso esiti di crossover.
Cosa significa per la fertilità e la stabilità del genoma
Complessivamente, lo studio mostra che RPA fa più che rivestire semplicemente il DNA libero; modula direttamente il comportamento di un’elicasa meiotica fondamentale. Agganciandosi a RPA, Mer3 diventa uno srotolatore di DNA più determinato, capace di estendere e stabilizzare le strutture congiunte del DNA che maturano in crossover. Quando questa interazione è indebolita, le cellule si orientano verso esiti di riparazione più sicuri ma meno utili e lasciano più intermedi non risolti, compromettendo sottilmente la segregazione dei cromosomi. Poiché gli stessi attori molecolari esistono negli esseri umani — e mutazioni in HFM1 sono collegate all’infertilità — questo lavoro fornisce un quadro meccanicistico di come piccole modifiche a un’interfaccia proteica possano avere ripercussioni sulla salute riproduttiva e sulla diversità genetica delle generazioni future.
Citazione: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Parole chiave: meiosi, ricombinazione genetica, elicasa del DNA, fertilità, crossover cromosomico