Clear Sky Science · it
Disregolazione della risposta al danno del DNA da parte di oligonucleotidi antisenso fosforotioati
Quando terapie geniche utili fuorviano la squadra di riparazione della cellula
Gli oligonucleotidi antisenso, o ASO, sono una classe emergente di farmaci di precisione progettati per attivare o spegnere singoli geni. Sono già impiegati per trattare alcune malattie genetiche rare e sono in sperimentazione per molte altre patologie. Questo studio mette in luce un lato inaspettato di una comune modificazione chimica usata per rendere questi farmaci più stabili: nelle condizioni giuste, può indurre la cellula a credere che il suo DNA sia danneggiato, inceppando la macchina di riparazione e mettendo a rischio la stabilità genomica a lungo termine.
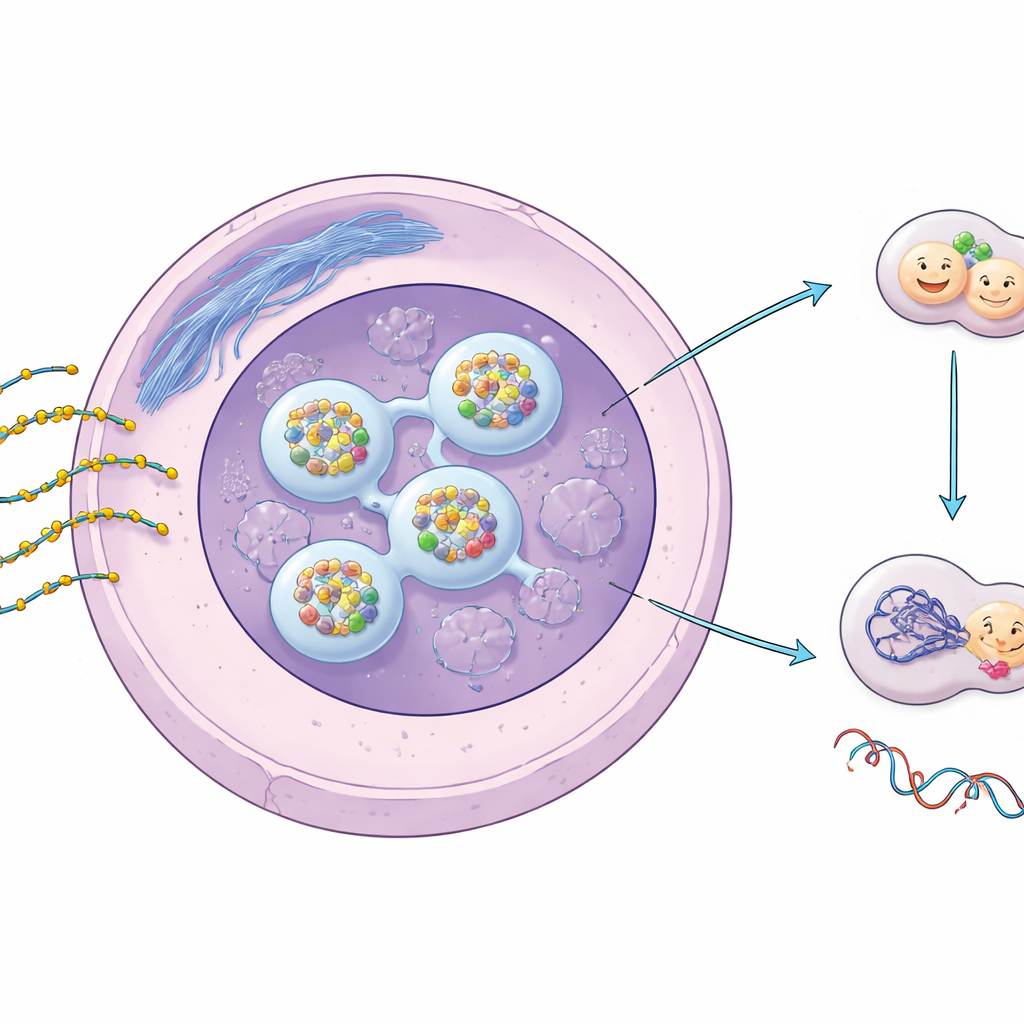
Interruttori genici progettati e il loro upgrade chimico
Gli ASO sono brevi filamenti singoli di materiale genetico costruiti per riconoscere e legare specifici messaggi di RNA all’interno delle cellule, silenziandoli o modificandoli. Per sopravvivere nell’organismo ed entrare efficacemente nelle cellule, la maggior parte degli ASO terapeutici presenta una modificazione fosforotioata (PS), in cui un atomo di zolfo sostituisce un atomo di ossigeno nello scheletro del filamento. Questo piccolo cambiamento aumenta notevolmente la loro stabilità e la tendenza a interagire con le proteine. Lavori precedenti avevano mostrato che i PS‑ASO si accumulano in punti distinti nel nucleo cellulare e possono stressare alcune strutture nucleari, ma ciò che questo comporta per la riparazione del DNA e la sicurezza a lungo termine non era chiaro.
Goccioline artificiali che imitano veri siti di riparazione del DNA
Gli autori hanno seguito PS‑ASO marcati fluorescentemente in cellule umane e hanno scoperto che, a dosi sperimentali comunemente usate, si accumulano rapidamente nel nucleo e fanno da seme per nuove strutture sferiche chiamate corpi PS. Questi corpi si formano in modo dipendente dalla concentrazione e si comportano come goccioline liquide che si fondono, si dissolvono e dipendono da forze molecolari deboli: caratteristiche tipiche della separazione di fase liquida. Crucialmente, non si trovano nei punti in cui avvengono rotture reali del DNA e non contengono i marcatori usuali del DNA spezzato. Invece, lo studio mostra che enzimi chiave della riparazione del DNA — tra cui DNA‑PKcs, ATM, ATR e PARP1 — si legano direttamente ai PS‑ASO e diventano fortemente arricchiti all’interno di queste goccioline artificiali, nonostante il DNA sottostante sia integro.
Falsi allarmi che attivano i segnali di danno della cellula
Una volta assemblate, le goccioline seminate dagli ASO fanno più che intrappolare passivamente proteine: attivano gli enzimi di riparazione. Entro un’ora dall’ingresso degli ASO, gli enzimi in queste goccioline risultano attivati e iniziano a modificare la cromatina circostante, decorando le proteine istoniche con marche chimiche tipicamente osservate dopo danni reali al DNA. Questo scatena la risposta al danno del DNA—reclutando fattori di riparazione aggiuntivi, attivando la segnalazione dei checkpoint e riducendo l’attività dei motori del ciclo cellulare chiamati CDK. Di conseguenza, le cellule rallentano o arrestano la progressione attraverso fasi chiave del ciclo cellulare, in particolare nel punto in cui normalmente verificano l’integrità del DNA prima della divisione. Nel cervello di topo esposto a una somministrazione di ASO di rilevanza clinica, i ricercatori hanno inoltre osservato un aumento della segnalazione del danno del DNA nelle aree con maggiore captazione di ASO, indicando che questi effetti non sono limitati alle colture cellulari.
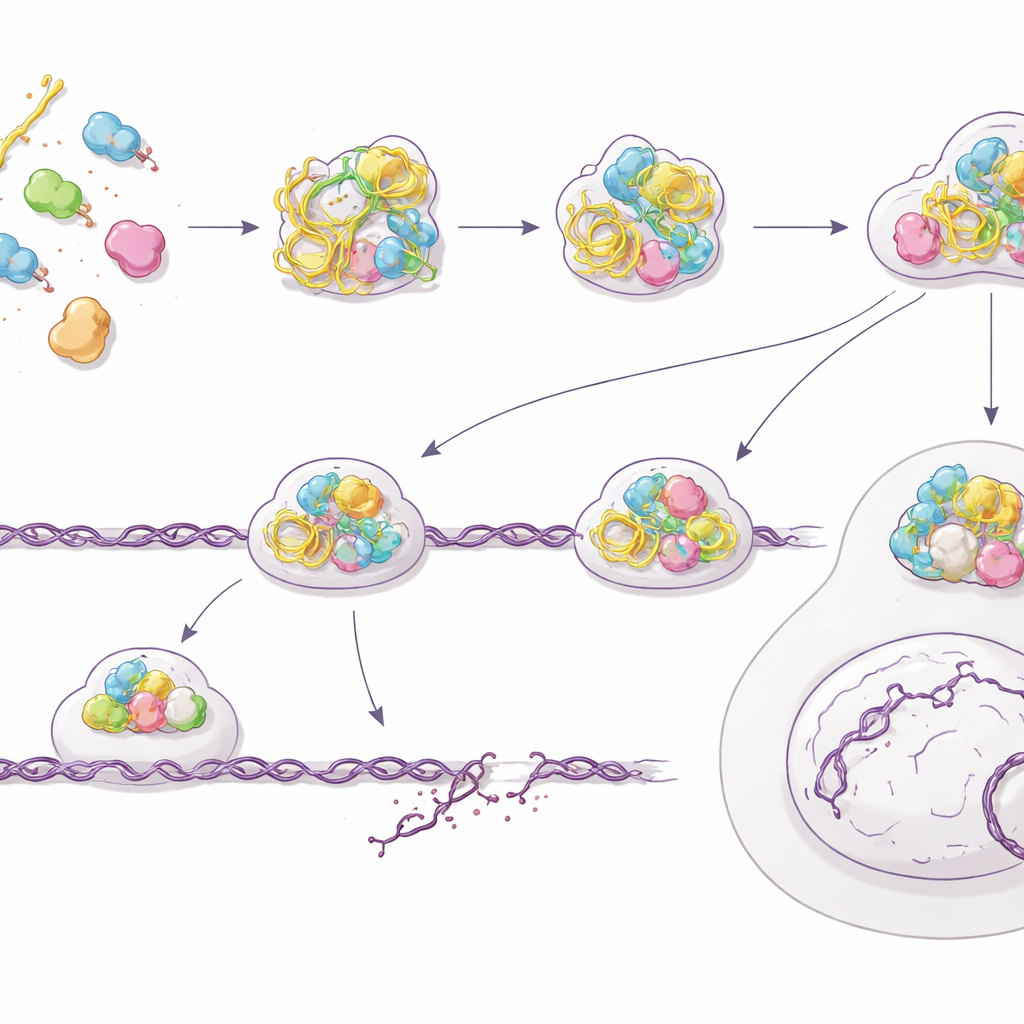
Riparazione che va male e un carico crescente di rotture del DNA
Paradossalmente, mentre il sistema d’allarme della cellula suona a tutto volume, la sua capacità reale di riparare rotture pericolose del DNA peggiora. Il gruppo ha dimostrato che le cellule pretrattate con PS‑ASO faticano a riparare i danni dopo irradiazione e accumulano persino più rotture spontanee, misurate con saggi comet e con fuochi di riparazione persistenti. Un’analisi più dettagliata di una delle vie di riparazione più accurate della cellula — la ricombinazione omologa — ha rivelato il problema: attori chiave come BRCA2 e RAD51 non riescono ad assemblarsi correttamente alle estremità del DNA rotto, mentre compaiono ancora marcatori iniziali di processamento di quelle estremità. Usando un sistema reporter genetico, gli autori hanno quantificato una riduzione di circa il 60% nell’efficienza della ricombinazione omologa dopo esposizione a PS‑ASO. Le cellule diventano meno vitali nel complesso e significativamente più sensibili alle radiazioni, coerentemente con un sistema di riparazione che viene segnalato ma non dispiegato correttamente.
Cosa significa questo per il futuro dei farmaci mirati ai geni
Nel complesso, lo studio suggerisce che gli ASO modificati con PS possono nucleare goccioline liquide artificiali nel nucleo che concentrano e attivano enzimi di riparazione del DNA anche quando non c’è danno da riparare. Questo falso allarme cronico interrompe le scelte normali di riparazione, in particolare la ricombinazione omologa accurata, portando a lesioni persistenti del DNA, attivazione dei checkpoint e morte cellulare. Pur essendo gli effetti più evidenti a livelli nucleari elevati di ASO tipici degli esperimenti di trasfezione, una sottile attivazione della segnalazione di danno è rilevabile anche a dosi inferiori, più simili a quelle farmacologiche. Per pazienti e sviluppatori di farmaci, il messaggio è chiaro: le caratteristiche chimiche che rendono gli ASO medicinali efficaci possono, in alcuni contesti, interferire con la salvaguardia più fondamentale della cellula—la sua capacità di mantenere un genoma stabile—sottolineando la necessità di progettare backbone più sicuri e di monitorare le vie di riparazione del DNA durante la terapia.
Citazione: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Parole chiave: oligonucleotidi antisenso, risposta al danno del DNA, separazione di fase liquida, ricombinazione omologa, stabilità del genoma