Clear Sky Science · it
I mitici peptidoglicani chirali prendono di mira la biosintesi della parete batterica per intervenire sui patogeni
Un nuovo modo per individuare i germi nocivi
Le infezioni resistenti agli antibiotici sono in aumento in tutto il mondo, eppure i medici continuano a disporre di pochi strumenti in grado di riconoscere e colpire con precisione i batteri pericolosi senza danneggiare le nostre cellule. Questo studio presenta un astuto “esca” molecolare che imita un componente chiave della parete batterica. Queste molecole progettate possono sia evidenziare le infezioni per l’imaging sia trasportare antibiotici direttamente ai microrganismi, offrendo una strategia nuova per combattere patogeni difficili da trattare.
Imitare l’armatura batterica
I batteri sono avvolti da una fitta rete chiamata parete cellulare, costruita con zuccheri e aminoacidi speculari insoliti che le nostre cellule utilizzano in misura molto ridotta. I ricercatori hanno sfruttato questa differenza creando lunghe catene a base di zucchero decorate con una specifica forma speculare dell’alanina, un aminoacido comune. Queste catene, chiamate mimetici peptidoglicanici chirali, sono progettate per assomigliare da vicino agli ingredienti naturali che i batteri usano per costruire le loro pareti, ma sono assenti nei tessuti dei mammiferi. Regolando con cura la quantità di alanina in forma D legata alle catene, il gruppo ha ottenuto versioni che preferiscono nettamente i batteri rispetto alle cellule umane.
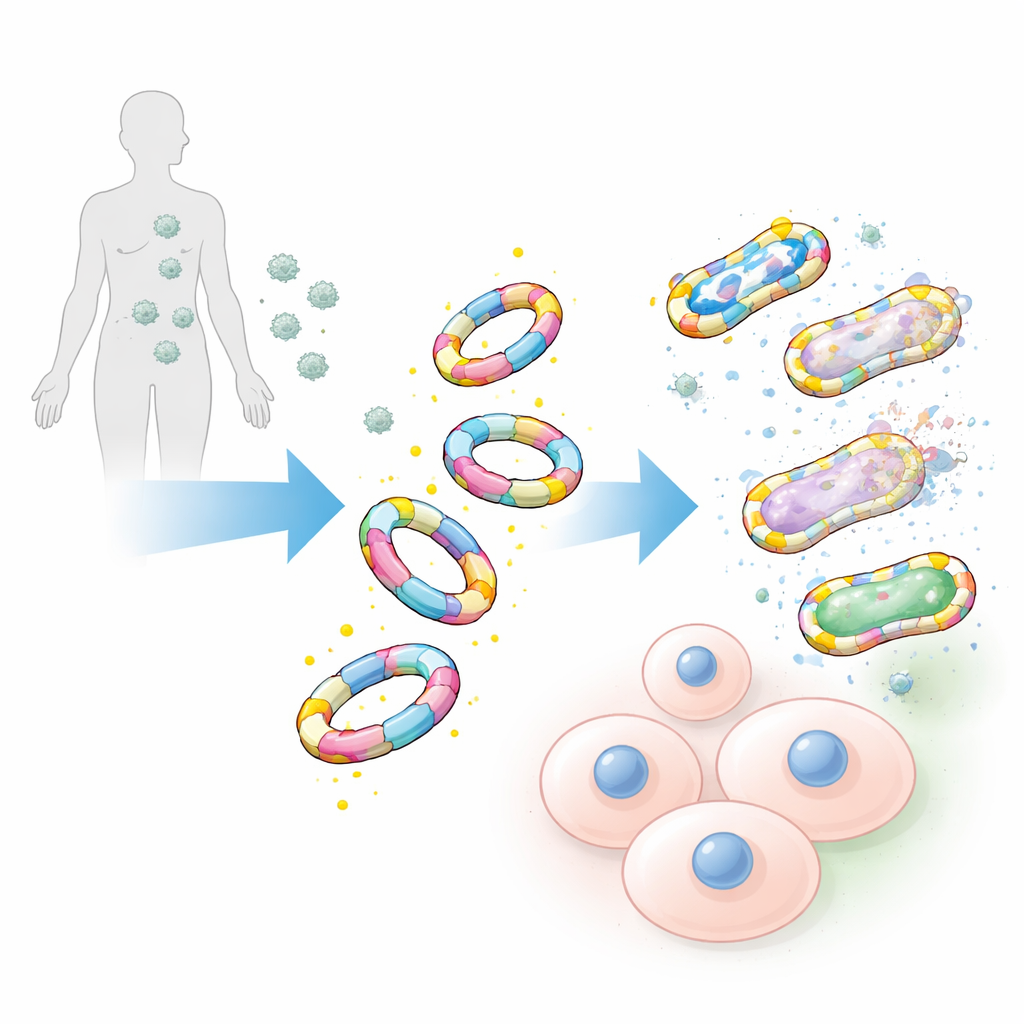
Agganciarsi ai batteri, non alle nostre cellule
Testati su un’ampia gamma di patogeni, comprese note ceppi ospedalieri come lo Staphylococcus aureus meticillino-resistente e altri batteri ESKAPE, i mimetici decorati con D-alanina si sono legati alle superfici batteriche con sorprendente efficacia. I loro omologhi speculari costruiti con la forma L dell’alanina, così come le catene zuccherine originali da sole, hanno mostrato solo un legame debole o trascurabile. Il gruppo ha anche confrontato questi grandi mimetici con sonde chimiche tradizionali, di piccola dimensione, basate su singole molecole di D-alanina. Anche quando le sonde piccole erano rese estremamente luminose, etichettavano comunque molti meno batteri e fornivano segnali più deboli, sottolineando la forza del progetto più grande e più simile all’originale.
Dirottare la linea di montaggio della parete
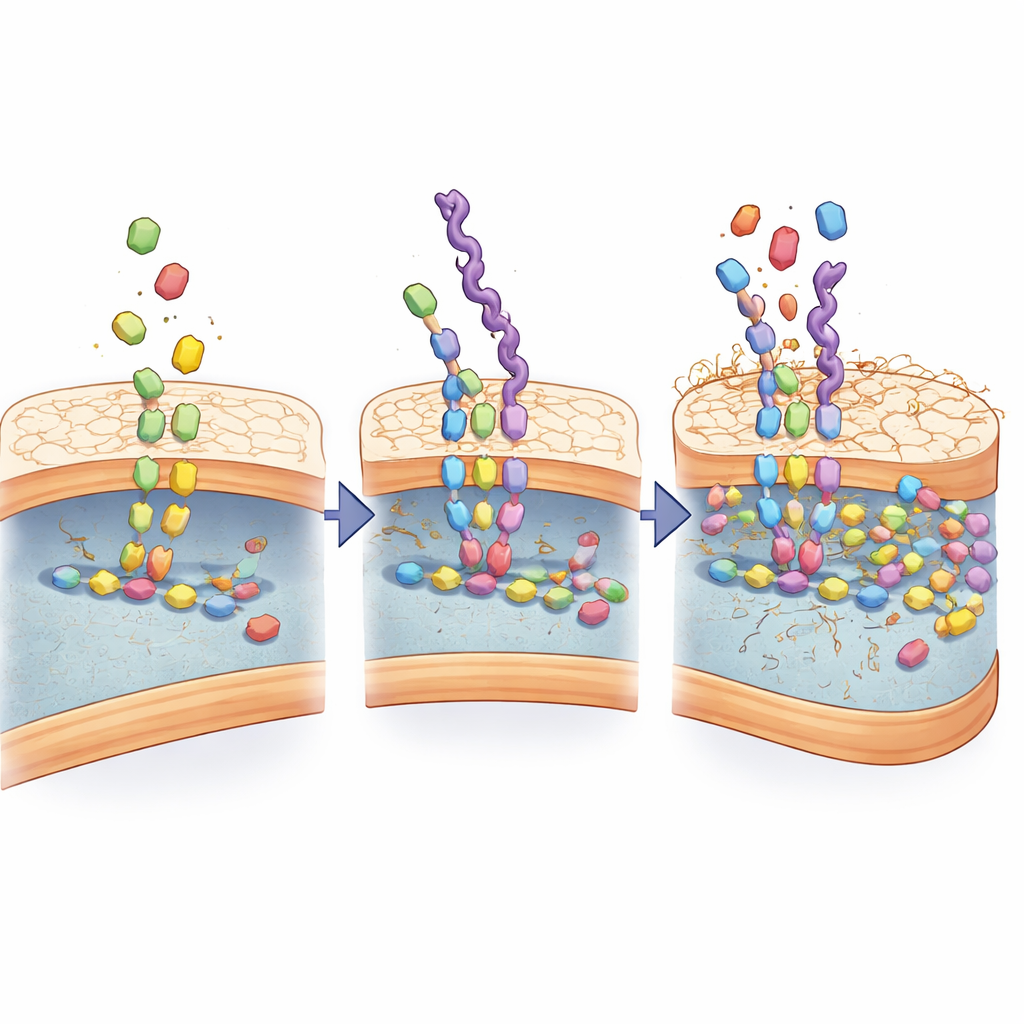
Per capire perché il riconoscimento fosse così forte, gli scienziati hanno studiato come i mimetici interagiscono con la macchina enzimatica che costruisce la parete batterica. Hanno scoperto che le catene a base di D-alanina non si limitano ad aderire all’esterno; vengono incorporate come se fossero veri elementi di costruzione e alimentate negli stessi passaggi enzimatici che normalmente uniscono i componenti della parete. L’analisi chimica ha rilevato nuovi intermedi molecolari che compaiono solo quando questi mimetici sono presenti, e le simulazioni al computer hanno mostrato che enzimi chiave per la formazione della parete afferrano i mimetici ancor più saldamente rispetto ai substrati naturali. Dopo vari cicli di crescita batterica, i mimetici si sono accumulati nella parete, deformandone gradualmente la struttura e rendendola più permeabile.
Trasformare i mimetici in vettori intelligenti di farmaci
Poiché queste catene tendono naturalmente ad assemblarsi in piccole particelle in acqua e offrono numerosi siti chimici reattivi, il gruppo le ha usate come impalcature per coloranti per imaging e per antibiotici. Versioni fluorescenti hanno delineato chiaramente i batteri nelle colture cellulari, interagendo molto poco con le cellule di mammifero coltivate nello stesso ambiente. I ricercatori hanno quindi caricato l’antibiotico tetraciclina nelle particelle a base di mimetici. Nei test in vitro, questo confezionamento ha reso la tetraciclina diverse volte più efficace, uccidendo anche ceppi resistenti a dosi molto inferiori rispetto al farmaco libero. La microscopia ha mostrato che i mimetici caricati di antibiotico si accumulavano sui batteri, penetravano i loro involucri e provocavano una morte cellulare estesa rispetto alle formulazioni non mirate.
Combattere le infezioni nell’organismo
I test più impegnativi sono stati condotti in modelli murini di ferite cutanee localizzate e di infezioni addominali potenzialmente letali. Nelle ferite infette, i mimetici fluorescenti si sono indirizzati verso i batteri profondi nei tessuti e, quando trasportavano tetraciclina, hanno quasi completamente eliminato i microrganismi. Ciò ha portato a una guarigione più rapida, a uno strato cutaneo nuovo più spesso, a una deposizione di collagene più ordinata e a una maggiore formazione di piccoli vasi sanguigni. Nei modelli di infezione sistemica, i mimetici si sono accumulati specificamente in organi infetti come la milza e i polmoni, dove hanno ridotto nettamente il carico batterico quando caricati con antibiotico. È importante che dosi elevate dei mimetici da soli abbiano mostrato una buona sicurezza, senza danni evidenti agli organi principali o alla chimica del sangue.
Cosa potrebbe significare per i trattamenti futuri
Costruendo un sosia chimico molto simile agli ingredienti naturali della parete batterica, questo lavoro dimostra un nuovo modo di “confondersi” con il metabolismo del patogeno invece di limitarsi ad attaccarlo dall’esterno. Questi mimetici chirali funzionano sia come segnali ad alta precisione per l’imaging sia come veicoli intelligenti che indirizzano gli antibiotici direttamente ai loro bersagli microbici, inclusi ceppi resistenti, risparmiando le cellule dei mammiferi. Se tradotti in strumenti clinici, tali piattaforme biomimetiche potrebbero aiutare i medici a vedere esattamente dove si nascondono le infezioni e a trattarle in modo più efficace con dosi di farmaco inferiori, offrendo un’arma promettente contro la crescente sfida della resistenza antimicrobica.
Citazione: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Parole chiave: resistenza agli antibiotici, parete cellulare batterica, consegna mirata di farmaci, imaging molecolare, nanomedicina