Clear Sky Science · it
Riprogettazione genica tra specie sfruttando le informazioni sugli ortologhi e la modellazione generativa
Perché è importante riprogettare geni tra specie
La biotecnologia moderna spesso richiede di trasferire geni da un microbo a un altro per produrre farmaci, enzimi o strumenti per la bonifica ambientale. Tuttavia, un gene che funziona bene nel suo microbo d’origine può rendere poco nel nuovo ospite, producendo scarsa quantità di proteina. Questo articolo presenta un nuovo sistema di intelligenza artificiale, OrthologTransformer, che impara dall’evoluzione stessa per riscrivere i geni in modo che risultino “nativi” in una specie diversa, migliorandone le prestazioni e aprendo nuove possibilità per tecnologie verdi e industriali.
Limiti degli attuali trucchi per la messa a punto dei geni
Per decenni gli scienziati si sono affidati a una strategia chiamata ottimizzazione dei codoni per aiutare geni estranei a funzionare in nuovi ospiti. L’idea è semplice: il codice genetico dispone di diversi “codoni” di tre basi che possono codificare lo stesso amminoacido, e specie differenti preferiscono codoni diversi. Gli strumenti tradizionali sostituiscono i codoni rari con quelli preferiti senza modificare la sequenza amminoacidica della proteina. Questo spesso aiuta, ma ignora molte altre caratteristiche che influenzano le prestazioni geniche, come il ripiegamento dell’RNA, segnali regolatori e il timing della produzione proteica. In alcuni casi, un’eccessiva ottimizzazione dei codoni può persino ridurre la resa proteica. Nel frattempo, la natura risolve l’adattamento tra specie in modo più complesso: i geni correlati in specie diverse, noti come ortologhi, mostrano comunemente cambiamenti negli amminoacidi e piccole inserzioni o delezioni oltre allo scambio di codoni, pur preservando la funzione complessiva.
Imparare il “manuale” naturale per riscrivere i geni
OrthologTransformer tratta la riprogettazione genica come una forma di traduzione linguistica: data una sequenza di DNA di un batterio, la “traduce” in come quel gene probabilmente apparirebbe in un’altra specie. Il modello è costruito sull’architettura Transformer usata negli strumenti linguistici moderni, ma qui opera sui codoni invece che sulle parole. È addestrato su milioni di geni ortologhi naturalmente abbinati provenienti da oltre duemila specie batteriche, con token speciali che indicano da quale specie si converte e verso quale. Osservando come l’evoluzione ha già bilanciato funzione e adattamento all’ospite, il sistema impara quando bastano semplici scambi di codoni e quando sono tollerati sottili cambiamenti negli amminoacidi o aggiustamenti di lunghezza. In test che hanno coinvolto 45 specie batteriche e centinaia di combinazioni sorgente–destinazione, i geni riprogettati dall’IA assomigliavano più strettamente agli ortologhi nativi della specie di destinazione rispetto sia all’ottimizzazione tradizionale dei codoni sia a un ottimizzatore neurale di codoni leader, mantenendo comunque un’elevata similarità a livello proteico. 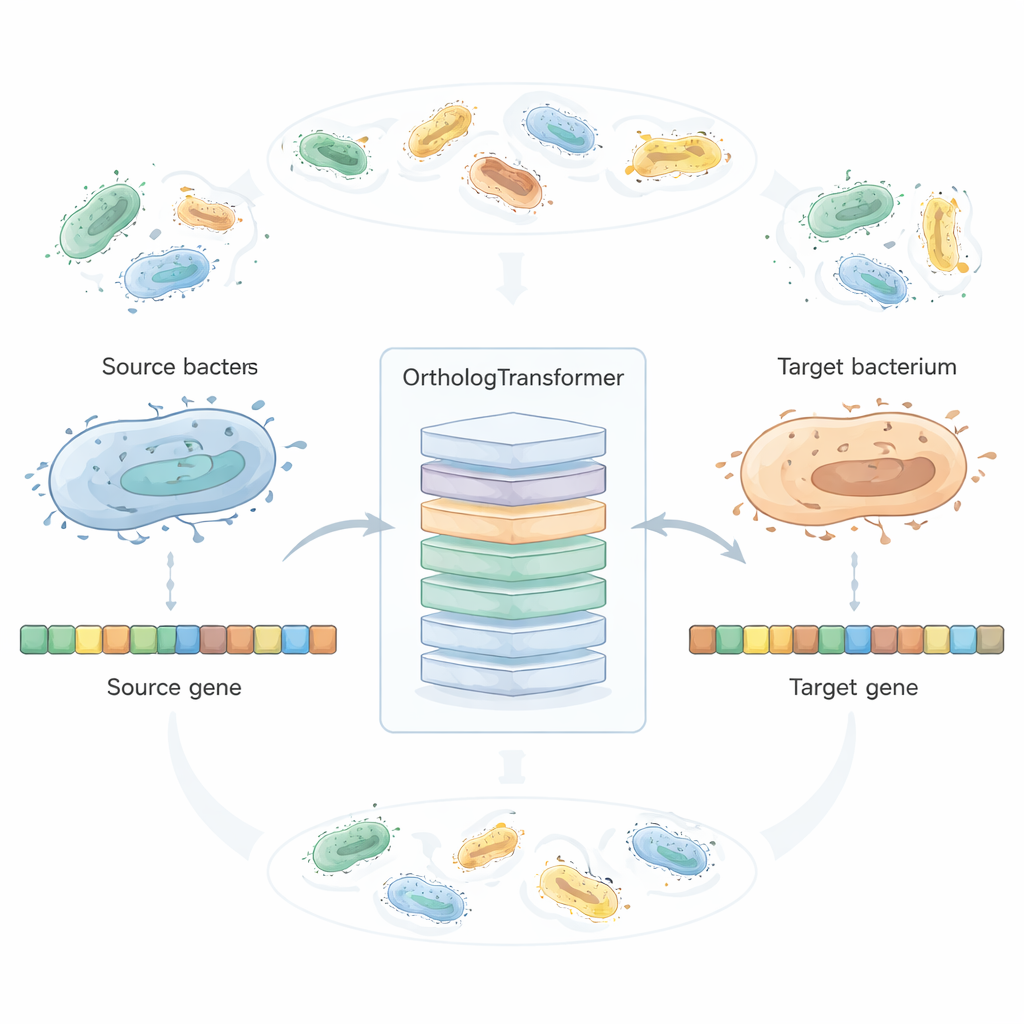
Mettere a lavoro enzimi “mangia-plastica” progettati dall’IA
Per dimostrare che non si tratta solo di un trucco computazionale, il gruppo si è concentrato su PETase, un enzima del batterio Ideonella sakaiensis capace di degradare il PET, il materiale usato nella maggior parte delle bottiglie. Ideonella cresce lentamente e non è ideale per applicazioni industriali, quindi i ricercatori hanno chiesto a OrthologTransformer di riscrivere il gene PETase per un ospite a crescita più rapida, Bacillus subtilis. Hanno generato un pannello di dodici varianti di geni riprogettati, esplorando diverse impostazioni di addestramento e una procedura di ricerca aggiuntiva che guidava le sequenze verso una composizione del DNA e strutture dell’RNA più tipiche di Bacillus. Nonostante alcune varianti contenessero molti cambiamenti del DNA e poche sostituzioni amminoacidiche, i modelli computazionali prevedevano che la forma 3D centrale dell’enzima fosse preservata. Quando questi progetti sono stati costruiti e testati in cellule viventi di Bacillus, diverse varianti hanno prodotto elevate quantità di PETase secreto e tutte hanno mostrato attività misurabile nella degradazione della plastica.
Un progetto guidato dall’IA che supera l’ottimizzazione standard
Una sequenza progettata dall’IA, chiamata AI-L2, si è distinta. Le cellule di Bacillus che esprimevano questo gene hanno secreto quantità particolarmente grandi di PETase e hanno generato circa tre volte più prodotto di degradazione della plastica rispetto a qualsiasi altro ceppo in un test di sette giorni, e circa dieci volte di più rispetto ai controlli tipicamente ottimizzati per codone se misurati dai prodotti di reazione. Immagini al microscopio dei film di PET esposti a cellule AI-L2 hanno rivelato profonde fossette e fori dove la plastica era stata consumata, molto più drammatici rispetto ad altre condizioni. Test enzimatici dettagliati hanno mostrato che la versione AI-L2 di PETase non solo veniva prodotta in modo più efficiente, ma processava anche il substrato più rapidamente, conferendole una maggiore efficienza catalitica rispetto all’enzima originale e alle versioni ottimizzate per codoni. Un esperimento parallelo in Escherichia coli ha mostrato che una versione di PETase progettata da OrthologTransformer, anche quando modificava solo l’uso dei codoni e non la sequenza amminoacidica, superava comunque un gene ottimizzato per codone basato sulle frequenze, sottolineando che il modello cattura preferenze sottili e specifiche dell’ospite che i metodi tradizionali perdono. 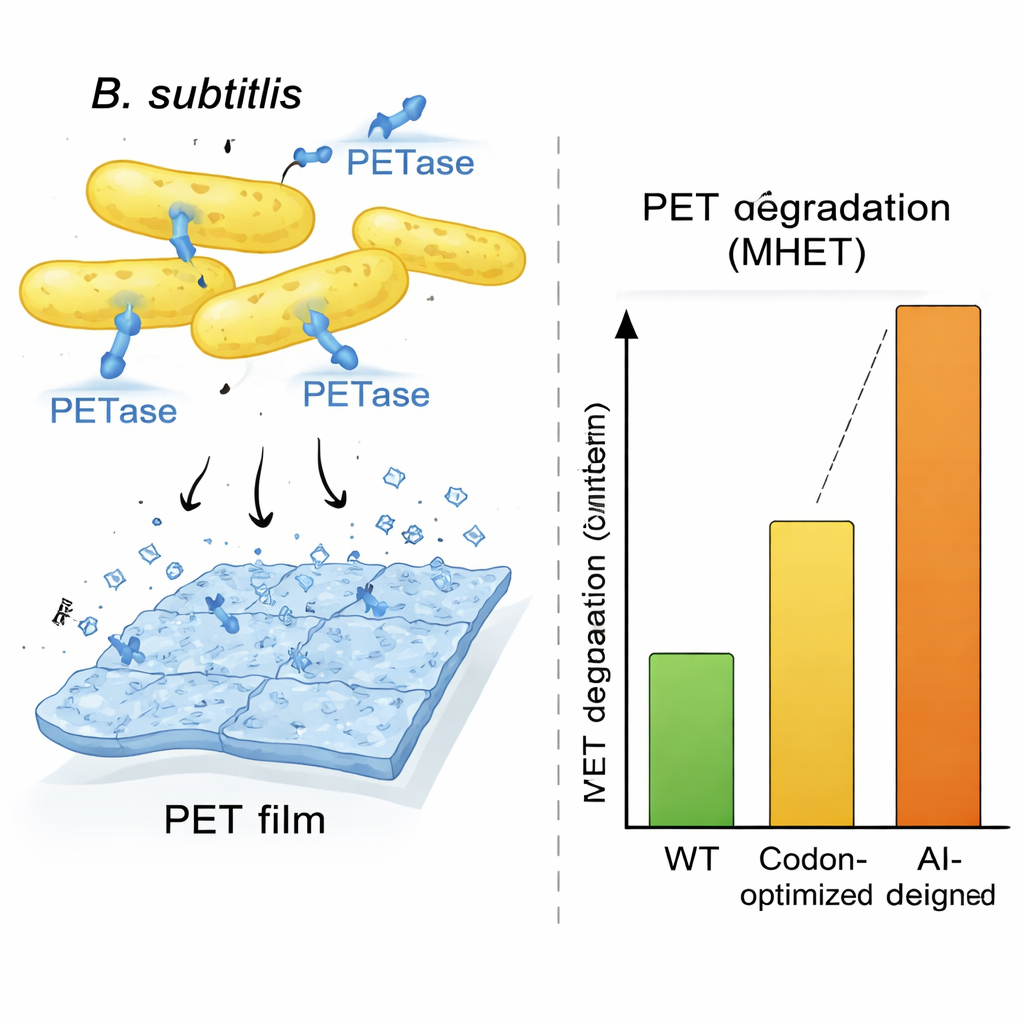
Cosa significa per la biologia e la tecnologia future
In termini quotidiani, OrthologTransformer è come un traduttore esperto che non si limita a riscrivere l’“ortografia” di un gene per un nuovo microbo, ma apporta anche piccole modifiche informate dall’evoluzione alla “frase” stessa quando sa che saranno sicure o vantaggiose. Imparando direttamente da come i geni si sono adattati naturalmente attraverso migliaia di specie batteriche, può proporre DNA riprogettato che funziona meglio in nuovi ospiti rispetto a progetti limitati allo scambio di codoni. La riuscita creazione di un enzima mangia-plastica più potente in Bacillus subtilis suggerisce che una tale riprogettazione genica guidata dall’IA potrebbe accelerare lo sviluppo di biocatalizzatori industriali, microrganismi per la bonifica ambientale e, in prospettiva, anche terapie geniche mediche, aiutando gli organismi a leggere e utilizzare geni estranei come se fossero propri.
Citazione: Akiyama, M., Tashiro, M., Huang, Y. et al. Cross-species gene redesign leveraging ortholog information and generative modeling. Nat Commun 17, 2120 (2026). https://doi.org/10.1038/s41467-026-69966-0
Parole chiave: riprogettazione genica, biologia sintetica, genei ortologhi, IA nella biotecnologia, enzimi degradanti la plastica