Clear Sky Science · it
Le cellule Th17 richiedono il sensore della riparazione del DNA xeroderma pigmentosum gruppo C per controllare il danno ossidativo al DNA in un modello murino
Custodi dei nostri difensori immunitari
Le cellule T helper 17, o Th17, sono un tipo speciale di globuli bianchi che pattugliano le barriere del nostro corpo, come intestino e pelle, per difenderci da batteri e funghi. Tuttavia partecipano anche a malattie autoimmuni quando la loro risposta sfugge al controllo. Questo studio pone una domanda apparentemente semplice: come fanno queste cellule così attive a proteggere il proprio DNA dallo stress chimico che producono mentre combattono le infezioni? La risposta si concentra su un sensore del danno al DNA chiamato XPC, noto soprattutto per proteggere le cellule della pelle dalla luce solare. Qui i ricercatori mostrano che XPC è fondamentale anche per mantenere le Th17 sane, energiche ed efficaci.
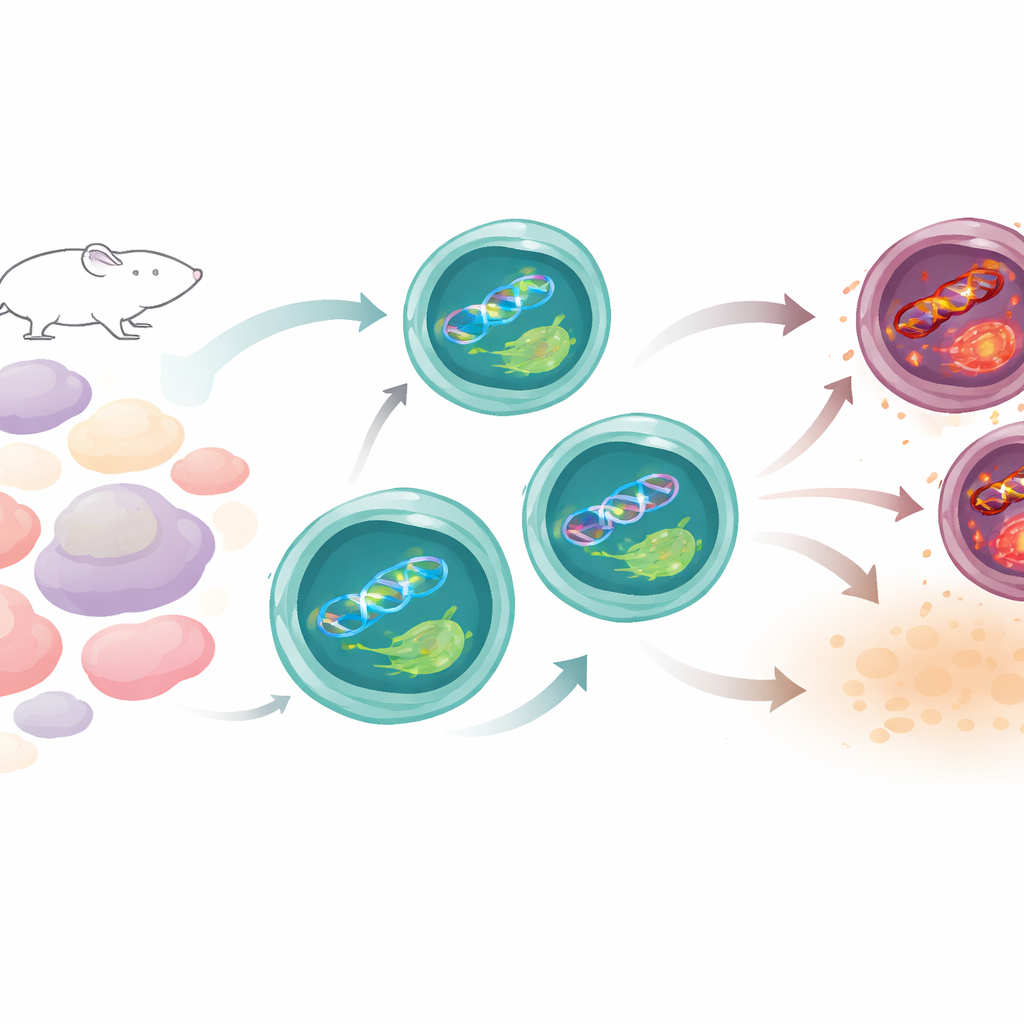
Come le Th17 mantengono normalmente l’equilibrio
Le cellule Th17 conducono una vita rischiosa. Per svolgere la loro funzione aumentano il metabolismo e producono specie reattive dell’ossigeno—molecole chimicamente reattive che possono danneggiare il DNA. Il gruppo ha confrontato le Th17 con altri tipi di cellule T nei topi e ha scoperto che, nonostante la loro intensa attività, le Th17 accumulano meno danni al DNA rispetto a molte loro «colleghe». Un indizio chiave è stato che i geni coinvolti nella riparazione del DNA, in particolare quelli di una via che normalmente corregge lesioni indotte dal sole, risultavano più attivi nelle Th17. Tra questi c’era XPC, una proteina che scandaglia il DNA alla ricerca di danni strutturali. Man mano che le Th17 maturavano, i livelli di XPC aumentavano e si localizzavano nei siti danneggiati nel nucleo, suggerendo che fosse costantemente in pattugliamento per mantenere l’integrità genetica.
Cosa succede quando manca il sensore del DNA
Per valutare l’importanza reale di XPC, i ricercatori hanno usato topi ingegnerizzati per non esprimere questa proteina. A prima vista il loro sistema immunitario sembrava per lo più normale: il numero complessivo di cellule T e molte sottopopolazioni di T non cambiavano. Ma concentrandosi sulle Th17 è emerso un difetto evidente. Senza XPC, molte meno cellule producevano la molecola caratteristica delle Th17, l’IL-17, e marcatori d’identità chiave e interruttori di segnalazione che guidano il programma Th17 risultavano ridotti. In coltura, cellule T naive provenienti da questi topi faticavano a differenziarsi in vere cellule Th17. In un modello standard in cui T trasferite scatenano infiammazione intestinale, le T prive di XPC non riuscivano a indurre colite, riflettendo una capacità infiammatoria attenuata. Contemporaneamente le cellule T regolatorie, che attenuano le risposte immunitarie, diventavano più abbondanti, suggerendo uno spostamento dell’equilibrio tra aggressività e controllo.
Danno al DNA, fabbriche di energia e stress chimico
Approfondendo, il gruppo ha trovato che le Th17 senza XPC presentavano più rotture delle catene di DNA e più basi del DNA ossidate, una firma dell’attacco da parte delle specie reattive dell’ossigeno. Anche i geni che normalmente rilevano il danno al DNA e arrestano il ciclo cellulare risultavano ridotti, suggerendo un sistema d’allarme indebolito. Il metabolismo energetico delle cellule veniva rimodellato: perdevano parte della loro capacità di usare percorsi glicolitici a pronta disponibilità e divenivano più dipendenti dai mitocondri, i piccoli impianti energetici intracellulari. Eppure questi mitocondri rilasciavano più specie reattive dell’ossigeno e mostravano segni di stress, creando un circolo vizioso di crescente stress chimico e danno al DNA. È notevole che il trattamento delle cellule con un antiossidante abbia ripristinato la produzione di IL-17 e ridotto il danno al DNA, collegando direttamente lo stress ossidativo al difetto funzionale osservato.
Un lavoro di squadra nella riparazione del DNA danneggiato
Oltre al suo ruolo classico, XPC cooperava anche con un’altra proteina di riparazione chiamata OGG1, che riconosce una base del DNA frequentemente ossidata. I ricercatori hanno mostrato che queste due proteine si associano fisicamente nelle Th17, aiutando a coordinare la rimozione delle basi danneggiate. Quando XPC mancava, l’attività di taglio di OGG1 aumentava, come se cercasse di compensare il danno in eccesso. Ma questa iperattività avveniva in un contesto di elevato stress ossidativo e reti di riparazione disturbate, e non bastava a riportare la funzione Th17 alla normalità. Analisi genetiche e strutturali suggerivano che XPC agisca da nodo che mette in collegamento diverse vie di riparazione e il controllo redox, garantendo che il danno venga non solo rilevato ma anche elaborato in modo da permettere alla cellula di continuare a dividersi e a produrre molecole protettive.
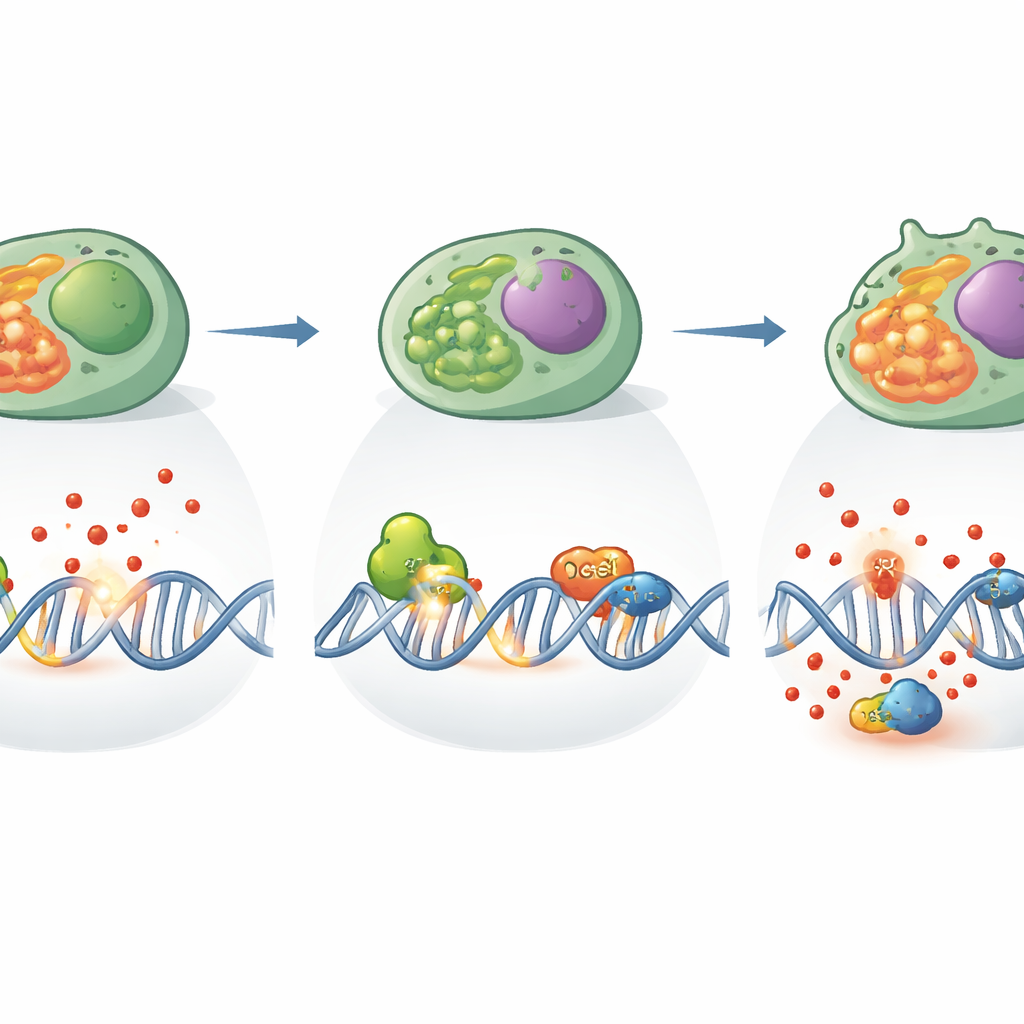
Perché questo è importante per malattie e terapie
Per il lettore non specialista, il messaggio chiave è che le cellule immunitarie hanno bisogno dei propri guardiani interni per restare in forma mentre ci proteggono. Questo studio rivela che XPC, precedentemente famoso per proteggere le cellule cutanee dai raggi UV, è anche un guardiano vitale delle Th17, mantenendo intatto il loro DNA e bilanciati i loro sistemi energetici sotto stress ossidativo. Quando XPC manca, le Th17 diventano geneticamente e metabolicamente fragili, producono meno output infiammatorio e possono spostare l’equilibrio immunitario verso la regolazione invece che l’attacco. Poiché le Th17 sono centrali in condizioni come la malattia infiammatoria intestinale, la psoriasi e la sclerosi multipla, le vie controllate da XPC potrebbero diventare nuovi bersagli per modulare le risposte immunitarie—calmando l’infiammazione dannosa o potenziando la difesa dove è troppo debole—agendo su come queste cellule riparano il DNA e gestiscono lo stress ossidativo.
Citazione: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Parole chiave: Cellule Th17, Riparazione del DNA, Stress ossidativo, Proteina XPC, Malattia autoimmune