Clear Sky Science · it
Secrezione tardiva endosomiale dipendente da VAMP7 di proteine del RE e dei mitocondri influenza il microambiente tumorale e il coinvolgimento dei macrofagi
Come le cellule sotto stress chiedono aiuto
Le cellule tumorali vivono vite difficili. Private di ossigeno e nutrienti, accumulano danni nei piccoli impianti energetici (mitocondri) e nelle fabbriche proteiche (reticolo endoplasmatico, o RE) al loro interno. Questo studio scopre un modo inaspettato con cui le cellule sotto pressione espellono pezzi danneggiati di queste strutture interne verso l’esterno. Nei tumori cerebrali detti glioblastomi, questo sistema cellulare di “esportazione dei rifiuti”, guidato da una proteina chiamata VAMP7, risulta influenzare il modo in cui le cellule immunitarie percepiscono e penetrano nel tumore.
Rotte di spedizione nascoste dentro la cellula
La maggior parte delle proteine che escono da una cellula segue una via classica: entrano nel RE, passano attraverso una stazione di smistamento centrale chiamata apparato del Golgi e vengono poi imballate in piccole bolle che si fondono con la membrana cellulare. Ma le cellule si affidano anche a rotte non convenzionali che bypassano il Golgi. Una di queste utilizza endosomi tardivi—sacche interne che possono fondersi con la superficie e rilasciare il loro contenuto all’esterno. Gli autori si concentrano su una proteina “cerniera” molecolare, VAMP7, già nota per aiutare gli endosomi tardivi a fondersi con la membrana esterna e rilasciare piccole vescicole extracellulari, minuscoli pacchetti che trasportano carico tra le cellule.
Portare le parti usurate verso l’uscita
Usando cellule renali e di glioma di ratto modificate e prive di VAMP7, i ricercatori hanno tracciato cosa accade alle proteine normalmente presenti nel RE e nei mitocondri. Hanno dimostrato che in assenza di VAMP7 le cellule rilasciavano molto meno una forma corta di una proteina che modella il RE chiamata RTN3 e di VDAC, un canale sulla superficie mitocondriale. Allo stesso tempo, gli endosomi tardivi risultavano mal posizionati e le piccole vescicole ricche del marcatore CD63 venivano poco secrete. Immagini ad alta risoluzione e saggi di prossimità hanno rivelato che RTN3 e materiale mitocondriale si associano fisicamente con endosomi tardivi CD63-positivi prima di essere rilasciati, e che questo passaggio dipende da VAMP7 e dalle sue proteine di fusione partner. Questi risultati supportano un modello in cui RE e mitocondri sotto stress formano piccole vescicole che si fondono con gli endosomi tardivi, i quali poi esportano il loro carico fuori dalla cellula. 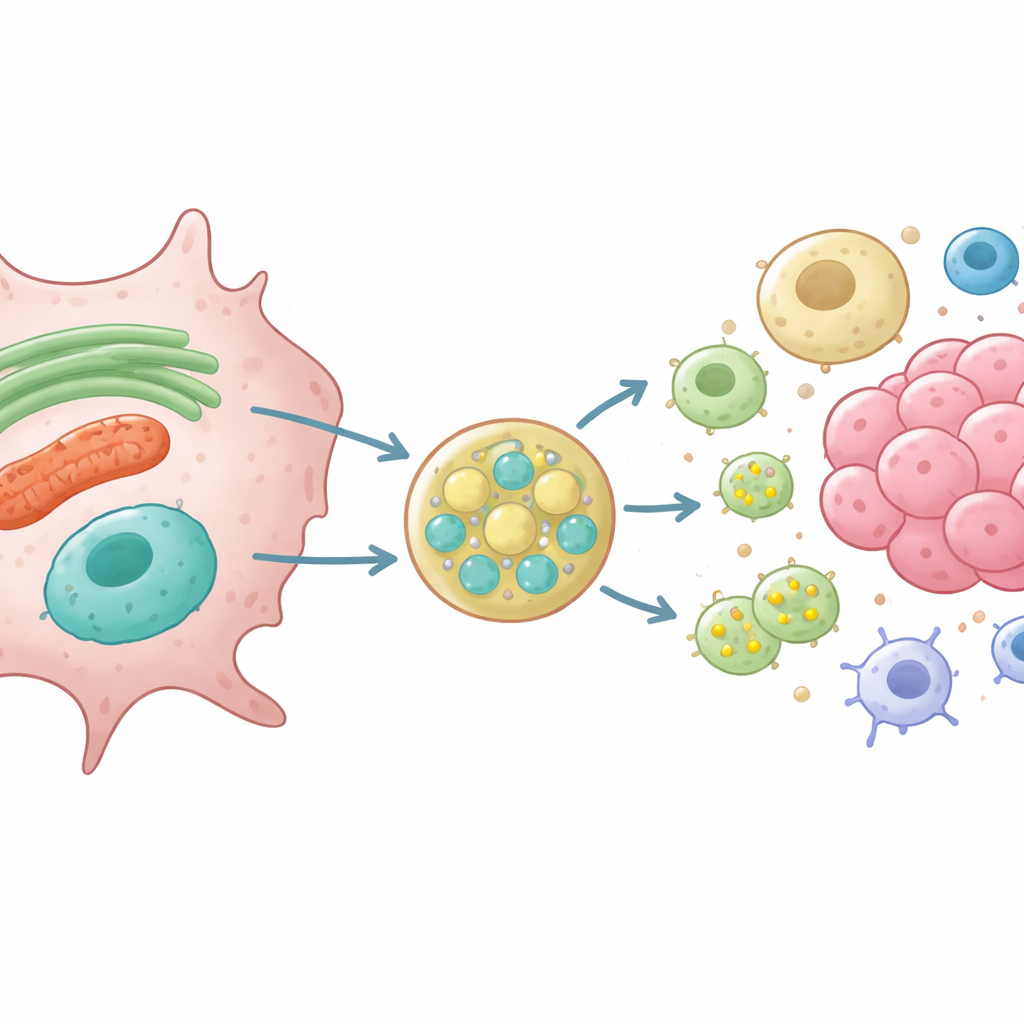
Scarico dello stress e controllo qualità
Le cellule prive di VAMP7 non perdevano la via generale di riciclo nota come autofagia, ma mostravano chiari segni di sofferenza. I profili di espressione genica indicavano l’attivazione di risposte di stress nel RE e alterazioni di geni legati ai mitocondri. La microscopia ha rivelato anomali “giri” di membrana del RE e mitocondri eccessivamente fusi ed elongati, entrambi segni distintivi di organelli in difficoltà nel mantenere l’equilibrio. Le misurazioni del consumo di ossigeno hanno mostrato che, pur avendo una maggiore massa mitocondriale, le cellule senza VAMP7 o prive di una proteina chiave dell’autofagia (ATG5) producevano meno energia. Quando gli scienziati provocarono deliberatamente stress al RE o ai mitocondri con farmaci, le cellule con VAMP7 intatto aumentarono la secrezione di RTN3 o VDAC, rispettivamente. Questo aumento veniva perso quando VAMP7 era rimosso, suggerendo che la secrezione mediata dagli endosomi tardivi funge da valvola di sfogo per eliminare componenti danneggiati e comunicare lo stato interno della cellula.
Modellare il quartiere tumorale
Per testare l’importanza di questa via nella malattia, il team ha usato un modello di glioblastoma nel ratto, un tumore cerebrale altamente aggressivo. Hanno impiantato nel cervello di ratto cellule di glioma normali, prive di VAMP7 o prive di ATG5. I tumori derivati da cellule senza VAMP7 crescevano molto e contenevano molto più tessuto necrotico, ma erano infiltrati da meno macrofagi—le cellule immunitarie che fagocitano i detriti e possono influenzare se un tumore cresce o si arresta. Al contrario, i tumori privi di ATG5 erano complessivamente più piccoli ma non mostrarono la stessa riduzione selettiva nell’ingresso dei macrofagi nel nucleo tumorale. Analisi di dataset di tumori cerebrali umani hanno inoltre rivelato che un’espressione più bassa di VAMP7 (e RTN3) è associata a una sopravvivenza peggiore dei pazienti, suggerendo che questa via di secrezione legata allo stress possa agire naturalmente per frenare la progressione tumorale modellando il paesaggio immunitario. 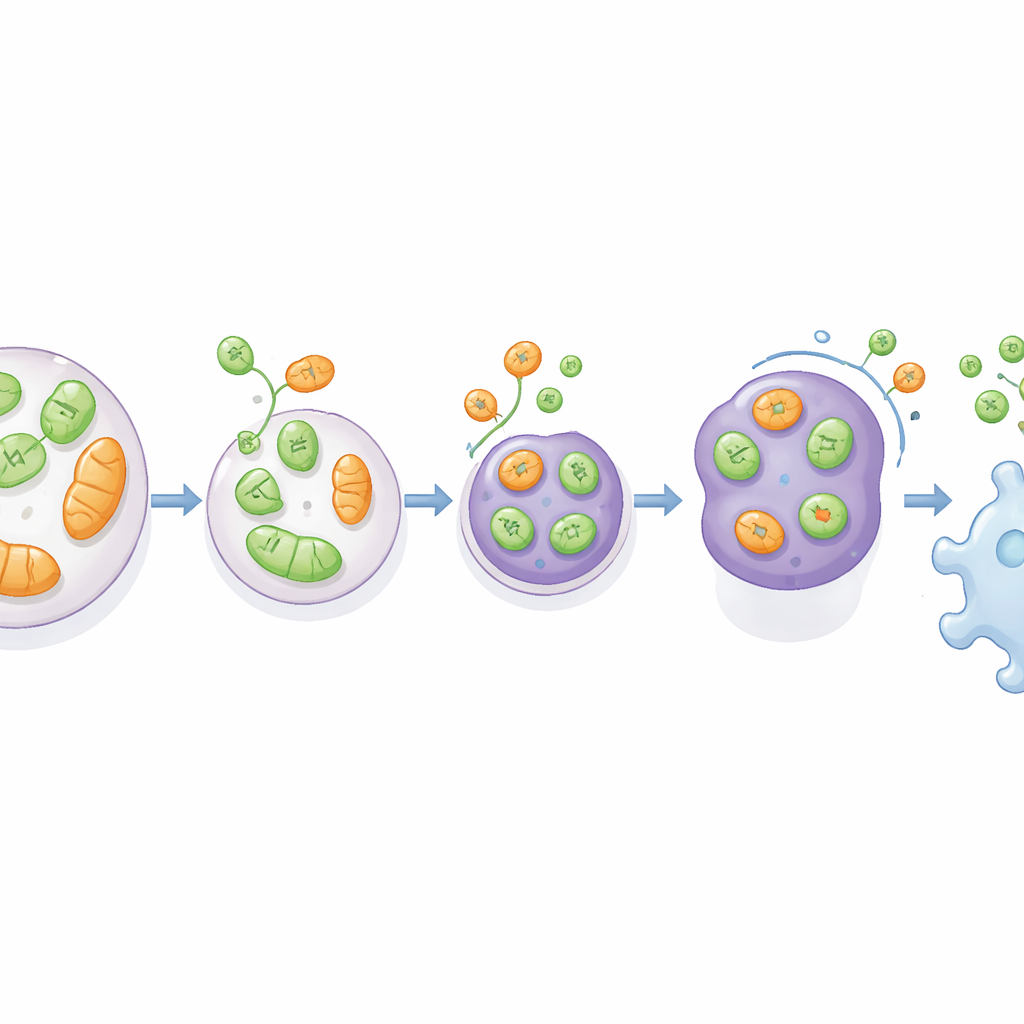
Perché è importante per cancro e immunità
In parole semplici, lo studio propone che VAMP7 aiuti le cellule a impacchettare ed esportare pezzi danneggiati della loro macchina interna tramite endosomi tardivi, soprattutto sotto stress. Nel glioblastoma, questo flusso verso l’esterno di materiale derivato dal RE e dai mitocondri sembra funzionare come un segnale di soccorso che incoraggia i macrofagi a entrare nel tumore e a rimuovere i detriti, contribuendo a un ambiente più soppressivo per il tumore. Quando VAMP7 manca, il segnale si indebolisce, il danno agli organelli si accumula, i tumori diventano più necrotici e il coinvolgimento dei macrofagi diminuisce. Comprendere e, potenzialmente, modulare questo sistema secretorio di controllo qualità potrebbe aprire nuove strade per rendere i tumori resistenti più visibili e reattivi al sistema immunitario.
Citazione: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Parole chiave: secrezione proteica non convenzionale, VAMP7, glioblastoma, microambiente tumorale, vescicole extracellulari