Clear Sky Science · it
Il fattore d’iniziazione degli eucarioti 6 modula la plasticità del carcinoma polmonare a piccole cellule tramite l’asse di segnalazione integrina-FAK
Perché questa ricerca sul cancro polmonare è importante
Il carcinoma polmonare a piccole cellule (SCLC) è una delle forme più letali di cancro ai polmoni. Di solito risponde bene alla chemioterapia all’inizio, ma quasi sempre recidiva, in modo rapido e aggressivo. Questo studio si pone una domanda centrale: cosa permette alle cellule SCLC di “cambiare personalità” e diventare resistenti ai farmaci, e si può rallentare o bloccare questo trasformarsi?
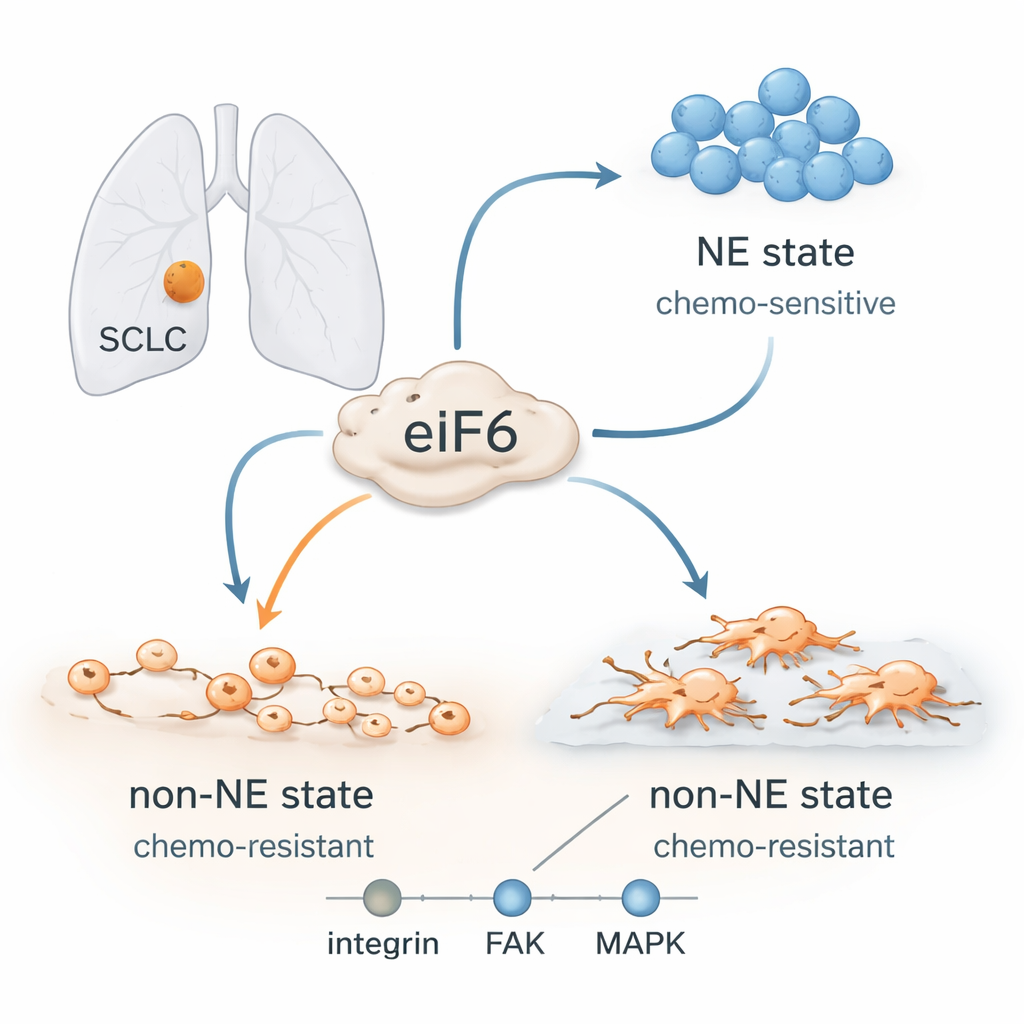
Cellule tumorali che cambiano forma
I medici pensavano che l’SCLC fosse una malattia uniforme, ma è ormai chiaro che questi tumori contengono tipi cellulari diversi. Alcune cellule hanno una forte identità “neuroendocrina”: crescono in gruppi compatti fluttuanti, rispondono bene alla chemioterapia a base di platino e tendono a essere ricche di certe proteine di tipo nervoso. Altre perdono questa identità e adottano uno stato “non neuroendocrino”: si diffondono, si attaccano ai tessuti circostanti, mostrano caratteristiche di cellule più mobili e invasive, e sono molto più difficili da eliminare con i farmaci. I tumori dei pazienti spesso evolvono dallo stato sensibile a quello resistente durante o dopo il trattamento, anche se il loro DNA non cambia molto. Questo suggerisce che a guidare la recidiva siano programmi cellulari plastici piuttosto che nuove mutazioni.
Un fattore della traduzione con una doppia vita
Gli autori si sono concentrati su una proteina chiamata eIF6, nota principalmente per il suo ruolo nell’assemblaggio dei ribosomi, le fabbriche proteiche della cellula. Studiando campioni di pazienti, modelli murini e diverse linee cellulari umane di SCLC, hanno scoperto che i livelli di eIF6 aumentavano costantemente quando le cellule passavano allo stato non neuroendocrino resistente ai farmaci. Sorprendentemente, questo aumento coesisteva con una diminuzione complessiva della produzione proteica di massa, insinuando che eIF6 possa svolgere ruoli oltre il suo compito classico. Analisi dettagliate di come gli mRNA si legano ai ribosomi hanno mostrato che le parti fondamentali del ribosoma non cambiavano molto. Al contrario, veniva rimodellato il modo in cui i messaggi venivano selezionati e processati per la traduzione quando le cellule cambiavano identità.
Distaccarsi per collegarsi ai segnali di sopravvivenza
Approfondendo, il gruppo ha scoperto che nelle cellule resistenti una parte di eIF6 si stacca dai ribosomi e si associa a un hub di segnalazione di superficie costruito intorno alle integrine e a una proteina chiamata focal adhesion kinase (FAK). Le integrine aiutano le cellule a percepire e aderire all’ambiente circostante; FAK trasmette quei segnali all’interno, spesso attivando percorsi che favoriscono movimento, sopravvivenza e tolleranza ai farmaci. Pull-down biochimici e saggi di prossimità in cellula hanno mostrato che eIF6 interagisce fisicamente con il partner integrinico CD104 e con FAK, e che questi complessi sono più abbondanti nelle cellule non neuroendocrine. Questo assemblaggio eIF6–integrina–FAK a sua volta potenzia l’attività della via di segnalazione MAPK, un noto motore della crescita e della resistenza allo stress.
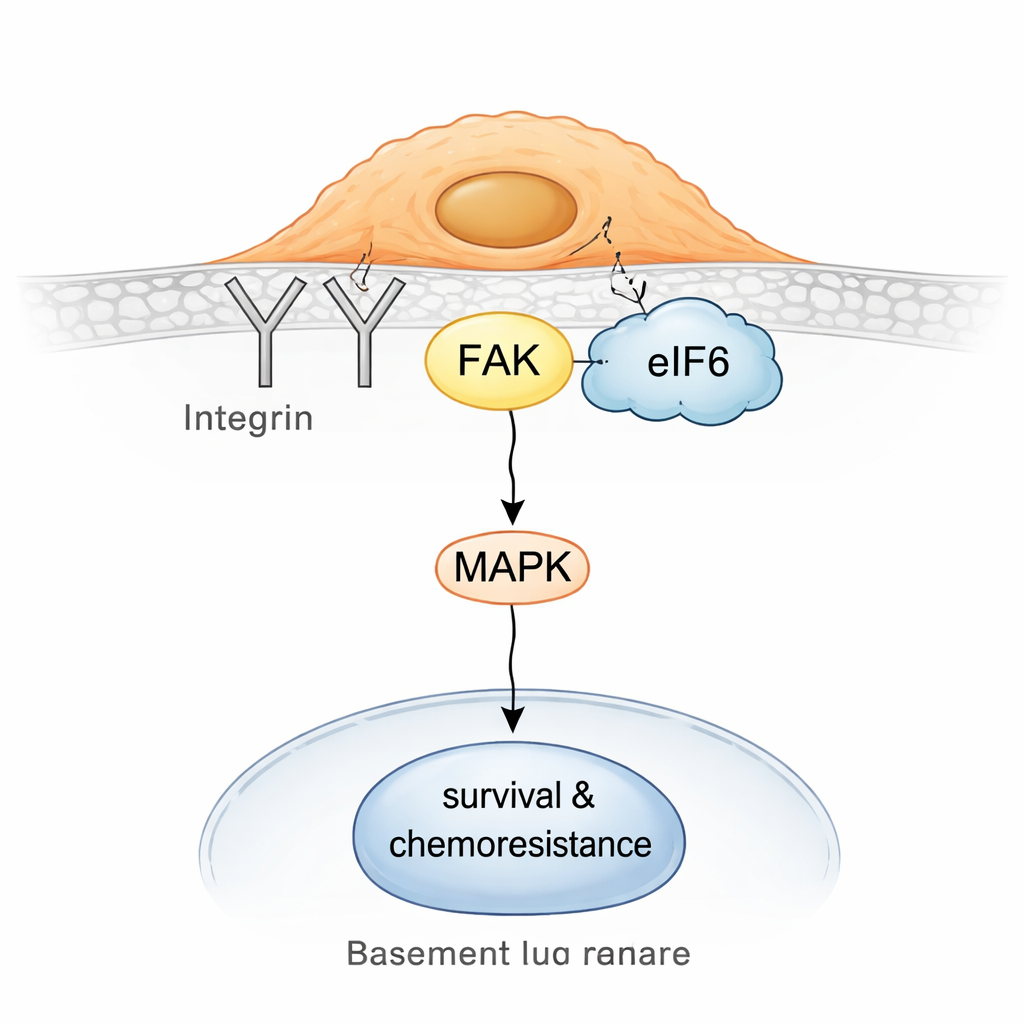
Rendere nuovamente vulnerabili i tumori resistenti
I ricercatori si sono quindi chiesti se manipolare eIF6 potesse modificare il comportamento dell’SCLC. Riducendo i livelli di eIF6 nelle cellule resistenti, i geni associati a un programma mobile e di formazione di cicatrici (epitelio–mesenchimale) venivano soppressi, mentre i classici geni neuroendocrini venivano parzialmente ripristinati. Questi cambiamenti non riportavano completamente le cellule allo stato precedente, ma rallentavano la transizione verso lo stato resistente. In modo cruciale, le cellule con meno eIF6 diventavano più sensibili alla chemioterapia standard con carboplatino–etoposide in coltura e nei tumori murini, lasciando meno colonie sopravvissute e un rimpicciolimento più duraturo. Poiché al momento eIF6 non è bersaglio di farmaci specifici, il gruppo ha testato inibitori di FAK già in sviluppo clinico. Bloccare la segnalazione FAK ha ri-sensibilizzato le cellule resistenti alla chemioterapia e, nei topi, la terapia combinata ha prodotto il controllo tumorale più efficace.
Dall’intuizione di laboratorio agli strumenti futuri per i pazienti
Infine, gli autori hanno esaminato campioni tumorali di pazienti con SCLC in stadio limitato sottoposti a intervento chirurgico. Usando un metodo di colorazione sensibile che evidenzia le proteine solo quando sono vicine tra loro, hanno misurato quanto spesso eIF6 si trovi in complesso con CD104 o con FAK all’interno delle cellule tumorali. Alti livelli di questi complessi—più che di eIF6 da solo—erano associati a recidive più precoci e a una sopravvivenza più breve, indicandoli come promettenti marker prognostici. Nel complesso, questo lavoro rivela che eIF6 può “lavorare di notte” lontano dai ribosomi per aiutare a collegare le cellule tumorali a circuiti di sopravvivenza potenti. Mappando questo asse eIF6–integrina–FAK, lo studio suggerisce modi per identificare i pazienti a rischio più elevato di recidiva e supporta l’uso combinato di inibitori di FAK con la chemioterapia per contrastare la pericolosa plasticità dell’SCLC.
Citazione: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Parole chiave: carcinoma polmonare a piccole cellule, resistenza ai farmaci, plasticità cellulare, eIF6, segnalazione integrina FAK