Clear Sky Science · it
Inibizione della traduzione dipendente dal contesto come modalità terapeutica contro il cancro
Usare le fabbriche di proteine contro il cancro
Le cellule tumorali sopravvivono producendo continuamente grandi quantità di proteine “driver” a breve emivita che ne mantengono la crescita e la divisione. Questo studio esplora un nuovo modo di combattere il cancro inceppando in modo sottile le macchine cellulari per la sintesi proteica — i ribosomi — solo quando cercano di costruire sequenze proteiche particolari, in particolare quelle presenti in oncogeni difficili da colpire farmacologicamente come MYC. Questa interferenza selettiva potrebbe eliminare le cellule tumorali risparmiando gran parte della produzione proteica normale.
Come le cellule costruiscono le proteine — e dove le cose possono andare storte
Ogni cellula dipende dai ribosomi, minuscole fabbriche molecolari che leggono i messaggi genetici (mRNA) e collegano gli amminoacidi in proteine. La maggior parte dei farmaci che prendono di mira i ribosomi, come gli antibiotici o alcuni vecchi farmaci oncologici, agisce come un attrezzo rozzo: sopprimono in modo ampio la sintesi proteica, danneggiando le cellule sane e provocando effetti collaterali gravi. Gli autori hanno ipotizzato che poiché ogni catena proteica nascente ha una sequenza e una caratteristica chimica uniche, fosse possibile progettare piccole molecole che bloccano il ribosoma solo quando una specifica sequenza si trova nella macchina, lasciando per lo più intatta la restante produzione proteica cellulare.
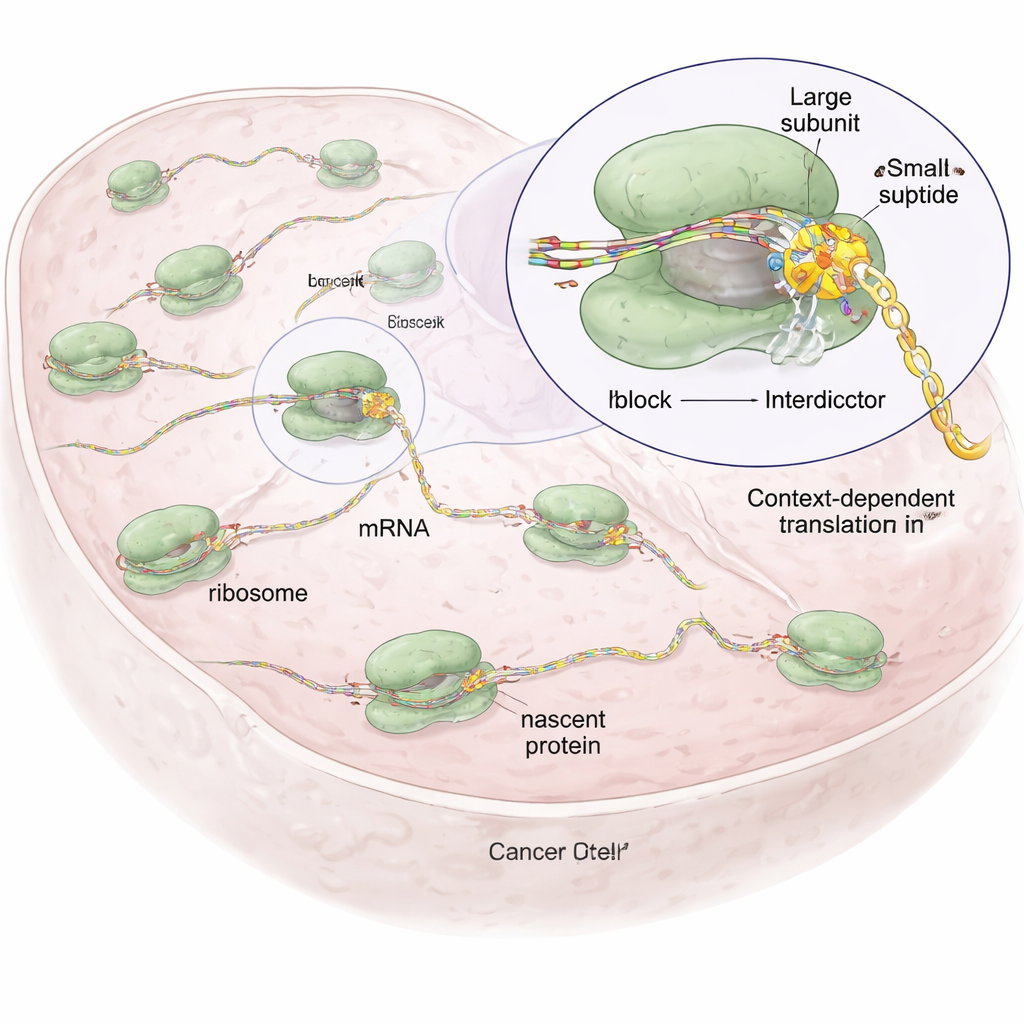
Molecole progettate che arrestano solo certe sequenze proteiche
Partendo da un composto naturale chiamato anisomicina, che si lega al cuore catalitico del ribosoma dove si formano i legami peptidici, i ricercatori hanno creato una famiglia di molecole sintetiche che chiamano “interdittori”. Tutte condividono uno scheletro centrale che le ancora all’interno del ribosoma, ma differiscono per gruppi laterali che puntano verso la catena proteica in crescita. Questi gruppi laterali sono sintonizzati per favorire particolari tipi di amminoacidi — per esempio, un interdittore (IDB-001) è attratto da residui carichi negativamente, mentre un altro (IDB-002) preferisce residui piccoli e idrofobici. Usando una tecnica chiamata ribosome profiling, che mappa globalmente dove i ribosomi fanno pause sugli mRNA all’interno delle cellule, il gruppo ha dimostrato che ciascun composto provoca arresti in brevi motivi distinti nella catena nascente, spesso al penultimo amminoacido (−1), dimostrando un’azione dipendente dalla sequenza piuttosto che un blocco indiscriminato.
Osservare l’incontro tra farmaco e ribosoma atomo per atomo
Per capire in dettaglio fisico come funziona questa selettività, gli autori hanno congelato ribosomi umani nell’atto di tradurre sequenze peptidiche progettate e li hanno immaginati mediante microscopia elettronica criogenica a risoluzione quasi atomica. Hanno osservato l’interdittore incastonato nel sito attivo del ribosoma che stabilisce contatti precisi con gli ultimi amminoacidi della catena nascente. In una struttura, un gruppo laterale idrofobico di IDB-002 è accolto da residui piccoli e non ingombranti nel peptide, spiegando perché catene laterali più grandi sono sfavorite. In un’altra, il gruppo laterale acido di un residuo derivato da MYC si avvicina per formare un ponte salino con un gruppo carico positivamente su IDB-001. La presenza del farmaco spinge anche basi di rRNA vicine in nuove posizioni che restringono il sito attivo e ostacolano parzialmente l’ingresso del tRNA successivo, contribuendo a congelare l’allungamento in quelle sequenze preferite.
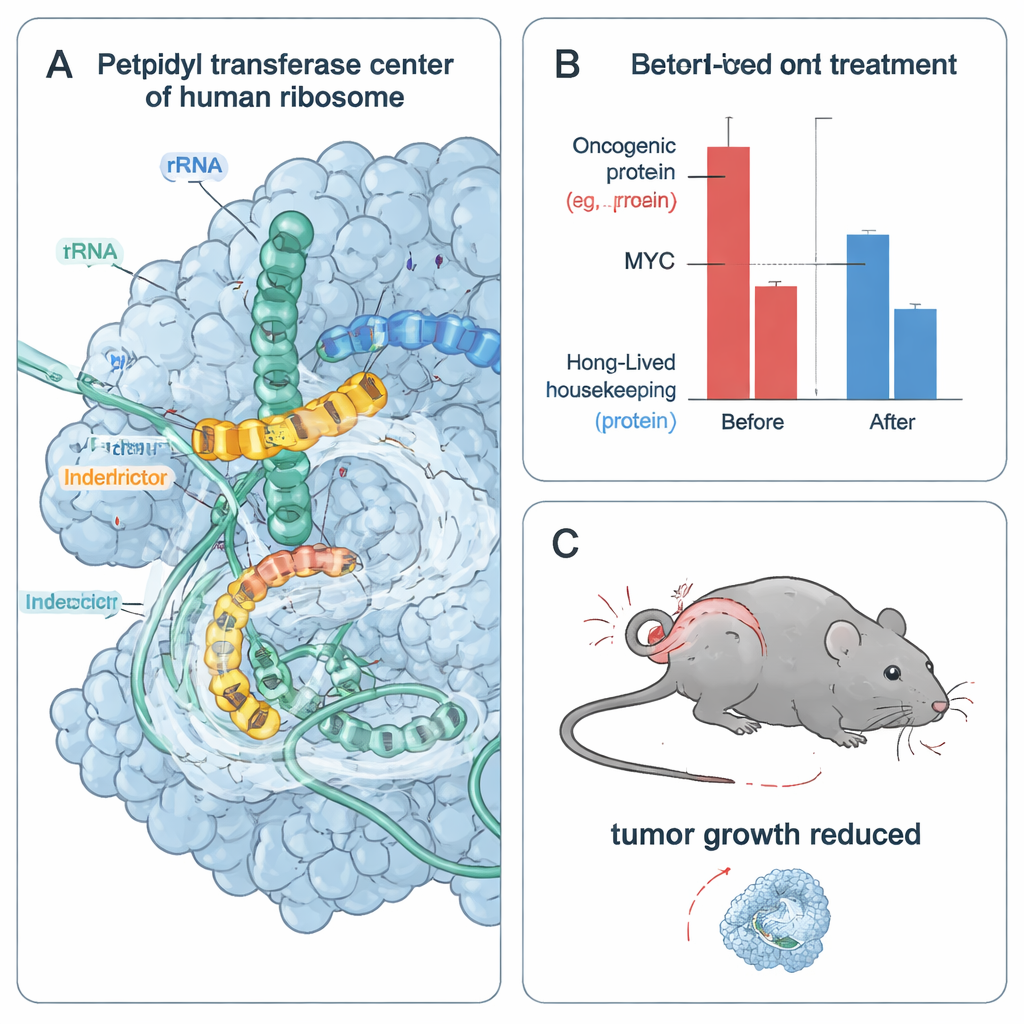
Dai ribosomi bloccati a cellule tumorali stressate e morenti
Poiché le cellule tumorali in rapida divisione dipendono fortemente da proteine oncogeniche a rapida degradazione come MYC e CCND1, il gruppo ha testato come gli interdittori influenzano la sopravvivenza delle cellule tumorali. In multiple linee cellulari tumorali dipendenti da MYC, IDB-001 e IDB-002 hanno ridotto la vitalità cellulare a concentrazioni nanomolari fino ai bassi micromolari. Un analogo ulteriormente ottimizzato, IDB-003, è risultato ancora più potente e adatto alla somministrazione orale. Nelle cellule, questi composti hanno rapidamente esaurito MYC e altre oncoproteine a rapido turnover lasciando relativamente stabili, nel medesimo intervallo temporale, proteine di base più longeve. I farmaci hanno anche indotto risposte di stress cellulare associate a collisioni tra ribosomi, ma il blocco di quelle vie di segnalazione dello stress non ha eliminato la perdita di vitalità, suggerendo che la privazione diretta di proteine oncogeniche essenziali è un fattore chiave nella morte delle cellule tumorali.
Prova di principio in un modello difficile di cancro al seno
Per verificare se questo approccio funziona negli animali, gli autori hanno trattato topi portatori di tumori umani di carcinoma mammario triplo negativo con IDB-003 somministrato per via orale. In 28 giorni, i tumori trattati sono cresciuti molto più lentamente rispetto a quelli dei controlli, con un’inibizione della crescita tumorale fino all’80% a dosi più elevate e senza tossicità severa riportata in questo studio. L’analisi dell’espressione genica dei tumori ha mostrato una forte downregulation dei programmi genici bersaglio di MYC, coerente con una ridotta attività di MYC in vivo. Nel complesso, questi risultati indicano che l’arresto selettivo dei ribosomi su specifiche sequenze proteiche può indebolire i tumori dipendenti da driver oncogenici instabili, evitando potenzialmente la tossicità diffusa dei classici bloccanti della traduzione.
Perché questo è importante per le future terapie oncologiche
Questo lavoro introduce un nuovo tipo di piccola molecola: una che non agisce legandosi a una proteina finita, ma intercettandola mentre viene sintetizzata e solo quando è presente un breve “tag di indirizzo”. Poiché molte proteine che promuovono il cancro sono flessibili, a breve emivita o prive di tasche evidenti per farmaci convenzionali, mirare la loro sintesi direttamente al ribosoma potrebbe aprire la strada al trattamento di tumori guidati da geni attualmente “non druggable” come MYC. Lo studio suggerisce inoltre che, sintonizzando la chimica degli interdittori, in futuro si potrebbero progettare medicinali focalizzati su diversi motivi di sequenza e bersagli patologici, estendendo questa strategia oltre l’oncologia ad altre condizioni in cui ridurre specifiche proteine potrebbe ripristinare la salute.
Citazione: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Parole chiave: terapia antitumorale mirata al ribosoma, inibizione della traduzione, tumori guidati da MYC, piccole molecole dipendenti dal contesto, carcinoma mammario triplo negativo