Clear Sky Science · it
L’ingegneria in situ di TRIM13 potenzia la capacità anti-infiammatoria dei CAR-M per la terapia della fibrosi epatica
Riprogrammare la squadra di pulizia del fegato
La fibrosi epatica, un processo di cicatrizzazione che può evolvere in cirrosi e insufficienza epatica, colpisce milioni di persone e attualmente dispone di poche terapie efficaci. Questo studio esplora un modo per sfruttare e riprogrammare le cellule immunitarie del fegato in modo che non solo rimuovano le cellule che formano la cicatrice, ma attenuino anche l’infiammazione dannosa, offrendo potenzialmente una terapia più sicura e potente per le malattie croniche del fegato.
Perché la cicatrizzazione del fegato è così difficile da fermare
Quando il fegato viene danneggiato ripetutamente — da virus, alcol o malattie metaboliche — tenta di ripararsi depositando tessuto cicatriziale. Cellule specializzate chiamate cellule stellate epatiche si attivano e producono fibre robuste, come operai che gettano cemento. Col tempo questa cicatrizzazione, nota come fibrosi, deforma l’organo e ne compromette la funzione. Al centro di questo processo ci sono i macrofagi, cellule del sistema immunitario. In un fegato danneggiato possono comportarsi come una lama a doppio taglio: in una modalità promuovono infiammazione e attivano le cellule stellate, mentre in un’altra, più riparativa, aiutano a degradare il tessuto cicatriziale e a ristabilire l’equilibrio.
Trasformare segnali dannosi in segnali utili
I ricercatori si sono concentrati su un segnale di pericolo chiave nei fegati danneggiati: il DNA mitocondriale che fuoriesce dalle cellule lesionate. I macrofagi rilevano questo DNA attraverso la via cGAS‑STING, che li spinge verso uno stato pro‑infiammatorio e pro‑fibrotico. Una proteina chiamata TRIM13 normalmente contribuisce a limitare STING marcandola per la degradazione. Il gruppo ha ipotizzato che aumentare TRIM13 all’interno dei macrofagi epatici potesse rimodularli verso uno stato più calmo e riparativo. Allo stesso tempo, volevano che queste cellule cercassero e rimuovessero direttamente le cellule stellate che formano la cicatrice. Per farlo hanno adottato il concetto del recettore chimerico per antigeni (CAR), preso in prestito dalla terapia oncologica: un recettore sintetico che permette alle cellule immunitarie di riconoscere un bersaglio scelto — in questo caso una proteina chiamata FAP, abbondante sulle cellule stellate attivate.
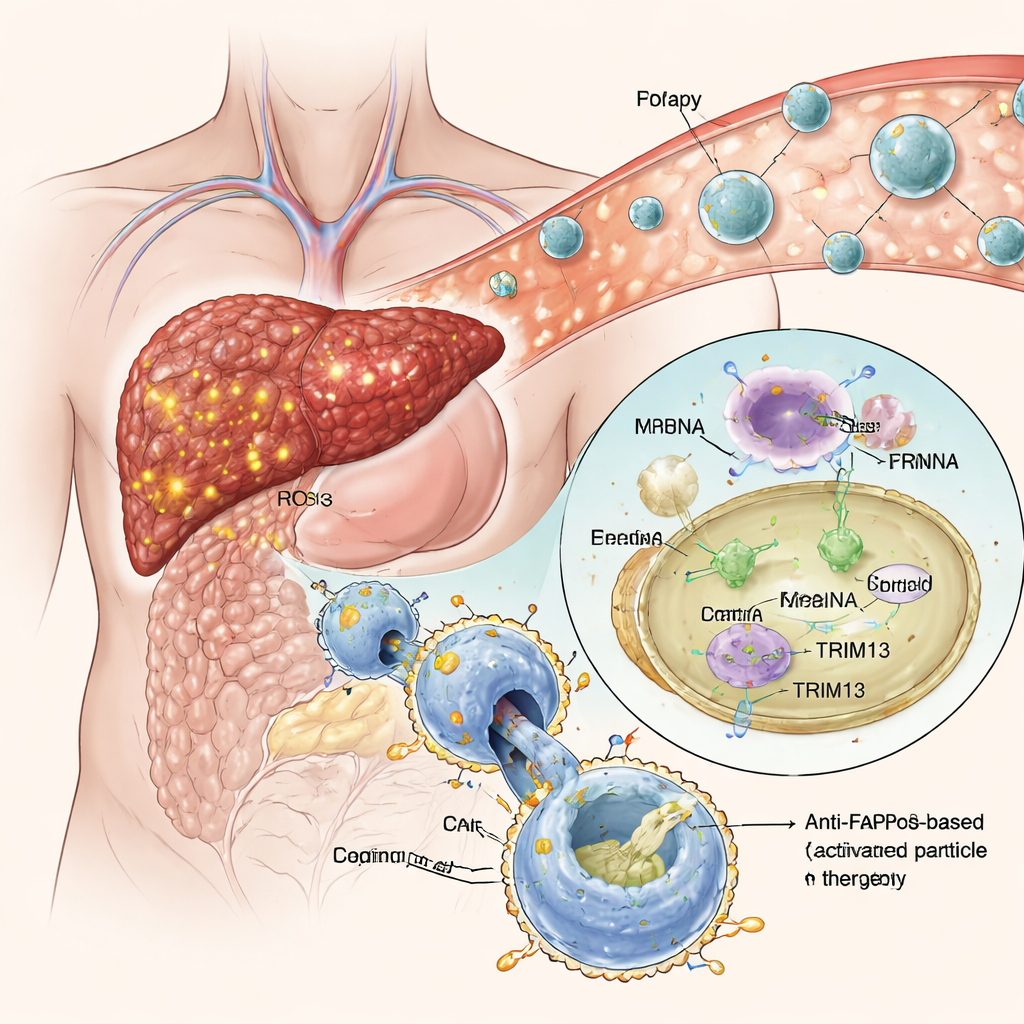
Nanoparticelle intelligenti che si dirigono al tessuto malato
Invece di modificare i macrofagi fuori dal corpo, il gruppo ha costruito nanoparticelle lipidiche «scatenate dall’efferocitosi» — piccole sfere lipidiche che trasportano istruzioni genetiche sotto forma di RNA messaggero (mRNA). Queste particelle sono rivestite con una forma mascherata di fosfatidilserina, un segnale naturale di «mangiami» che le cellule morenti espongono per attrarre i macrofagi. Nell’ambiente altamente ossidativo dei tessuti epatici fibrotici, la maschera viene rimossa e il segnale si rivela, inducendo i macrofagi vicini a inglobare le nanoparticelle. Una volta all’interno, l’mRNA viene rilasciato e tradotto dalla cellula, portando alla produzione sia di TRIM13 sia del CAR anti‑FAP. In colture cellulari questo approccio ha spinto con successo i macrofagi verso uno stato anti‑infiammatorio conferendo loro una forte e selettiva appetenza per le cellule FAP‑positive che formano la cicatrice, senza alterare la loro normale capacità di eliminare altri detriti.
Da fegati malati a fegati rigeneranti nei topi
Il team ha poi testato la strategia in modelli murini di fibrosi epatica indotta sia da una sostanza chimica tossica sia da una dieta povera di nutrienti e ricca di grassi. Le nanoparticelle somministrate sistemicamente hanno raggiunto efficacemente il fegato e, soprattutto negli animali fibrotici, sono state assorbite principalmente dai macrofagi. Là, le cellule ingegnerizzate hanno mostrato una ridotta attività della via STING e una minore produzione di molecole infiammatorie, insieme a una maggiore capacità di eliminare le cellule stellate attivate. Le analisi tissutali hanno rivelato cali marcati di collagene e altri marcatori di cicatrice, una struttura della matrice extracellulare più fine e più normale e miglioramenti negli esami ematici della funzione epatica. I fegati dei topi trattati hanno mostrato più cellule in proliferazione e un’architettura più sana, suggerendo una riparazione dell’organo reale piuttosto che una semplice attenuazione temporanea dell’infiammazione.
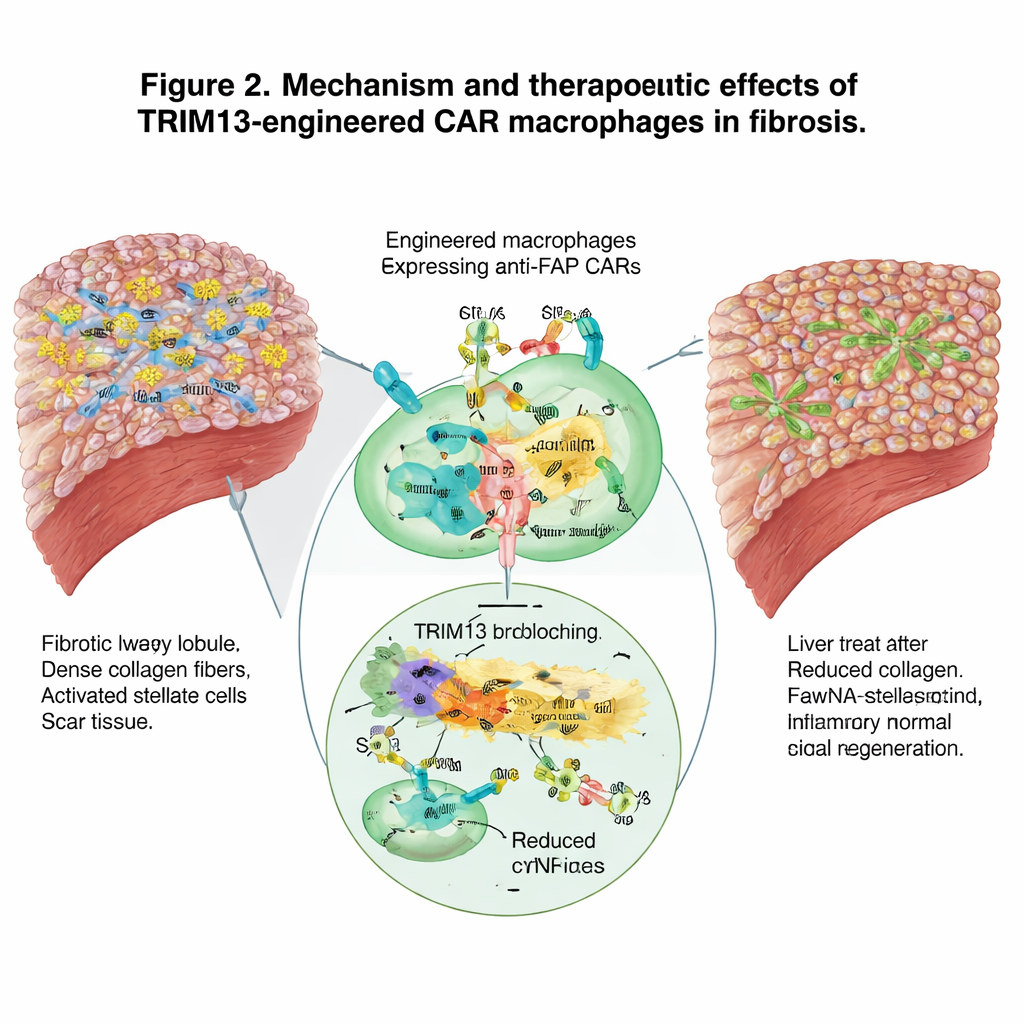
Coinvolgere l’intero sistema immunitario
Oltre alla rimozione diretta della cicatrice, i macrofagi ingegnerizzati hanno rimodellato il panorama immunitario più ampio. Si sono spostati da un profilo aggressivo e promotore di danno a uno più risolutivo e riparativo, riducendo i segnali infiammatori nel sangue. Allo stesso tempo, divorando le cellule che formano la cicatrice, sono apparsi come «insegnanti» per il sistema immunitario adattativo, attirando neutrofili, cellule dendritiche e linfociti T e favorendo una risposta coordinata contro il tessuto fibrotico. Il sequenziamento dell’RNA a singola cellula delle cellule immunitarie del fegato ha confermato lo spostamento da programmi genici pro‑infiammatori verso una maggiore capacità di fagocitare ed eliminare cellule e detriti dannosi.
Cosa potrebbe significare per i pazienti
Per un lettore non specialista, la conclusione è che questo lavoro indica un modo per «rieducare» le cellule spazzine del fegato in modo che smantellino il tessuto cicatriziale e spengano i segnali d’allarme cronici che perpetuano il danno. Usando istruzioni mRNA a vita breve confezionate in nanoparticelle intelligenti, la terapia evita di alterare permanentemente le cellule e limita l’attività alle regioni malate, il che potrebbe ridurre gli effetti collaterali. Pur richiedendo molte ulteriori verifiche prima di poter essere sperimentata sull’uomo, questa strategia delinea uno schema promettente per trattare la fibrosi epatica — e potenzialmente altre malattie fibrotiche — trasformando il sistema immunitario dell’organismo da motore della cicatrizzazione a partner attivo nella guarigione.
Citazione: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Parole chiave: fibrosi epatica, terapia con macrofagi, consegna di mRNA con nanoparticelle, recettore chimerico per antigeni, via TRIM13 STING