Clear Sky Science · it
Radiomarcatura di oligopeptidi mediante scambio selettivo di isotopi dell’idrogeno con deuterio e trizio in buffer acquosi
Tracciare i farmaci a livello atomico
I farmaci moderni includono sempre più spesso molecole biologiche complesse come peptidi e piccole proteine. Per capire dove questi farmaci si distribuiscono nell’organismo e quanto a lungo persistono, gli scienziati spesso sostituiscono alcuni atomi ordinari con atomi rari o radioattivi che possono essere rilevati. Questo articolo presenta un modo per “etichettare” i farmaci peptidici con tali atomi tracciabili direttamente in soluzioni acquose, molto più vicino alle condizioni biologiche reali rispetto alla maggior parte dei metodi precedenti.
Perché contano i piccoli scambi atomici
Sostituire l’idrogeno normale con forme più pesanti come il deuterio o il trizio trasforma molecole comuni in potenti traccianti scientifici. Queste versioni etichettate si comportano quasi allo stesso modo del farmaco originale ma possono essere seguite da strumenti sensibili che rilevano massa o radiazione. Per piccole molecole farmacologiche, i chimici hanno messo a punto un ampio repertorio di tecniche per ottenere composti etichettati. Al contrario, i metodi per marcare biologici più grandi e fragili — come peptidi e proteine — sono scarsi, spesso complessi e poco adatti ad ambienti acquosi simili al sangue o ai fluidi cellulari. Gli autori si sono posti l’obiettivo di colmare questa lacuna: una via semplice e selettiva per inserire deuterio o trizio nei mattoni peptidici direttamente in buffer acquosi.
Una strategia di marcatura in un unico passaggio in acqua
Il gruppo ha puntato su un tipo di reazione chiamata scambio di isotopi dell’idrogeno, in cui un atomo di idrogeno su una molecola viene sostituito dal suo cugino più pesante proveniente da un gas come il deuterio (D2) o il trizio (T2). Hanno allestito un catalizzatore in situ a base di iridio e di un opportuno fosfina coadiuvante. Mescolato in un buffer debolmente basico e riscaldato, questo sistema attiva legami carbonio–idrogeno specifici su amminoacidi e piccoli peptidi e sostituisce quegli idrogeni con deuterio o trizio provenienti dal gas. Fondamentale è che ciò avviene in un unico passaggio, in un mezzo ricco d’acqua e con quantità di metallo molto basse — condizioni più compatibili con peptidi delicati e con flussi di lavoro di laboratorio pratici. 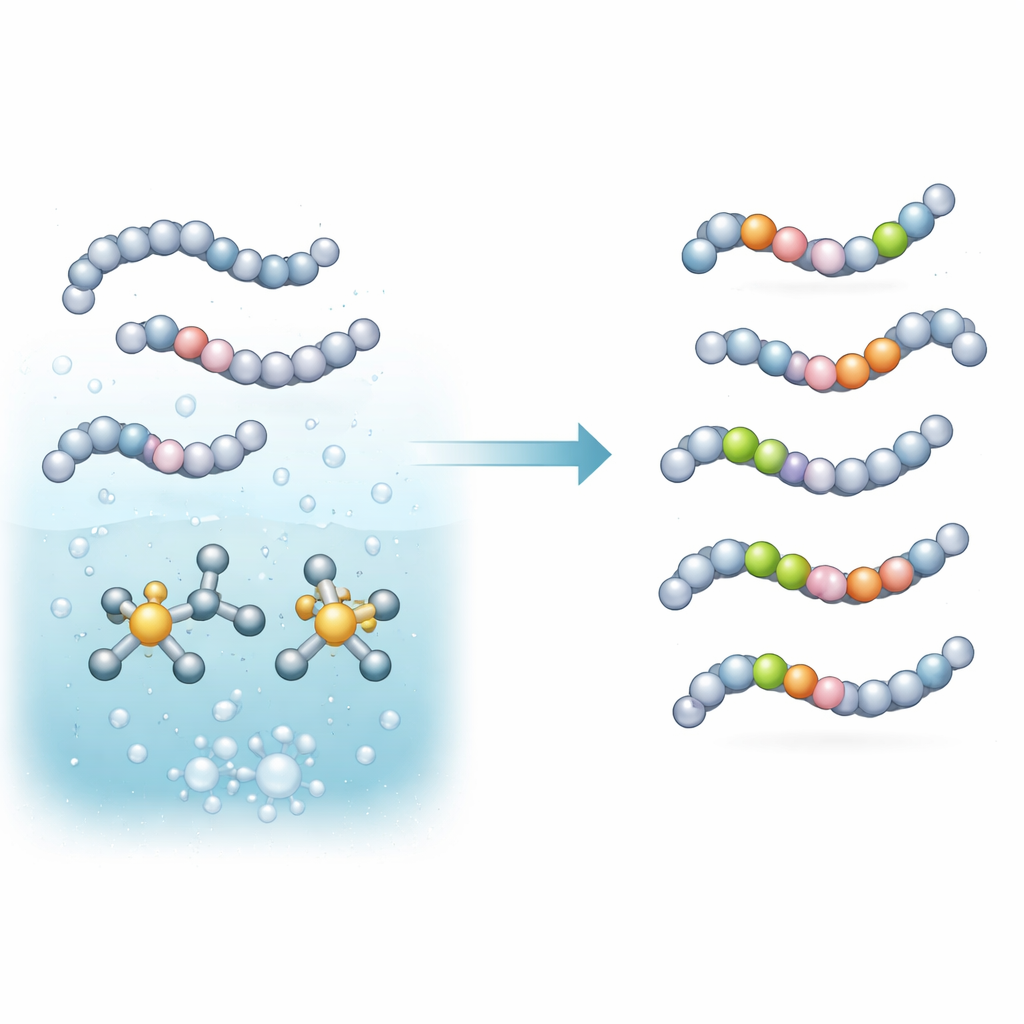
Scegliere i punti giusti sui peptidi
Non tutti gli atomi di idrogeno in un peptide sono ugualmente utili come etichetta. Alcuni vengono facilmente persi durante il metabolismo, il che cancellerebbe il marcatore radioattivo. Gli autori hanno esplorato con cura dove il loro catalizzatore preferisce agire. Hanno scoperto che amminoacidi non protetti come lisina e arginina sono particolarmente adatti. Nella lisina, il metodo etichetta selettivamente un carbonio nella catena laterale (la cosiddetta posizione gamma), un sito considerato “non attivato” e più probabile che resti stabile nell’organismo. Anche l’arginina mostra comportamenti simili in posizioni vicine della sua catena laterale. Testando una serie di molecole correlate, incluse catene corte con due gruppi amminici, il team ha osservato che la presenza di due siti azotati posizionati in modo appropriato aiuta il catalizzatore metallico ad agganciarsi alla molecola e raggiungere il legame carbonio–idrogeno mirato.
Uno sguardo al funzionamento interno del catalizzatore
Per capire perché sorge questa selettività, i ricercatori hanno combinato esperimenti con dettagliate simulazioni computazionali basate sulla teoria del funzionale della densità. Questi calcoli tracciano il paesaggio energetico mentre il complesso di iridio si forma partendo da un dimero, si lega all’acqua, poi all’amminoacido e infine inserisce in uno specifico legame carbonio–idrogeno. I modelli mostrano che la rottura del dimero di iridio originale è energeticamente fattibile in acqua per un certo tipo di precursore ma non per uno strettamente correlato, spiegando perché solo alcuni complessi di partenza sono efficaci. Rivelano inoltre che il substrato stesso contribuisce a stabilizzare il centro metallico attivo e a impedirne l’aggregazione in particelle inattive. Il percorso più favorevole coinvolge il legame dell’amminoacido tramite due atomi di azoto, formando una presa a “pinza” che posiziona un singolo legame carbonio–idrogeno per lo scambio con deuterio o trizio.
Dai semplici mattoni ai veri farmaci peptidici
Con il meccanismo in mano, il team ha esteso il metodo dai singoli amminoacidi a brevi peptidi contenenti fino a sette residui e poi a sequenze terapeutiche più complesse con fino a 13 amminoacidi. In tutti i casi, la marcatura avveniva sulle catene laterali di lisina o arginina poste all’estremità del peptide, e i peptidi restavano sostanzialmente intatti nelle condizioni di reazione. Per il trizio hanno ottimizzato la procedura a basse pressioni di gas per ottenere in sicurezza elevate attività specifiche, cioè una grande frazione di molecole che porta almeno un atomo di trizio. Questi peptidi marcati con trizio sono stati prodotti in un’unica soluzione e sono pronti per l’uso come traccianti in studi in vitro e potenzialmente in vivo. 
Cosa significa per i farmaci del futuro
Questo lavoro dimostra che è possibile attaccare selettivamente deuterio o trizio a farmaci peptidici realistici in un semplice passaggio acquoso, mirando a posizioni metaboliche robuste su amminoacidi chiave. Per gli sviluppatori di farmaci, ciò significa un accesso più agevole a versioni traccianti dei peptidi terapeutici, essenziali per misurare assorbimento, distribuzione e metabolismo. Oltre alla produzione di traccianti, le intuizioni meccanicistiche su come il catalizzatore al iridio interagisce con gli amminoacidi potrebbero ispirare nuovi modi per modulare dove e come le biomolecole complesse vengono modificate, aprendo la strada a un controllo chimico più preciso sui futuri medicinali biologici.
Citazione: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Parole chiave: peptidi radiomarcati, scambio di isotopi dell’idrogeno, marcatura con deuterio e trizio, terapeutici peptidici, catalisi al iridio