Clear Sky Science · it
ERCC6L2 garantisce fedeltà di riparazione per rotture a doppio filamento del DNA con estremità sfalsate
Perché questa scoperta è importante per il nostro DNA
Ogni cellula del corpo subisce continuamente danni al DNA, in particolare il tipo più pericoloso: rotture che recidono entrambi i filamenti della doppia elica. Se non vengono riparate correttamente, queste rotture possono causare cancro, malattie ereditarie o il fallimento di interventi di editing genomico terapeutico. Questo studio rivela una proteina «guardiana» finora poco considerata, ERCC6L2, che protegge in modo specifico un tipo insidioso di rottura dall’evolvere in ampi vuoti e cromosomi disordinati. Capire il ruolo di questa guardiana aiuta a spiegare una rara malattia del midollo osseo umano e mette in guardia su come alcuni strumenti di editing genico possano avere effetti avversi in pazienti vulnerabili.
Tipi diversi di rotture del DNA, rischi diversi
Non tutte le rotture del DNA sono uguali. Alcune incisioni sono nette, con entrambi i filamenti recisi nello stesso punto, come tagliare una corda alla perfezione. Altre sono sfalsate, lasciando brevi estremità sporgenti che non si allineano perfettamente. Gli attuali editor genomici come Cas9 generano di solito tagli netti e piatti, mentre strumenti come Cas12a, TALEN e alcuni sistemi di nickase accoppiati creano rotture sfalsate con estremità a sbalzo. I ricercatori hanno confrontato sistematicamente come le cellule umane affrontano questi due tipi di rottura abbattendo migliaia di geni e identificando quali fossero particolarmente importanti per riparare ciascun tipo di taglio.
Una guardiana nascosta per le rotture sfalsate
Dagli schermi genomici su larga scala è emersa ERCC6L2 come protettrice cruciale per le rotture sfalsate, ma in gran parte non necessaria per quelle piatte. Le cellule prive di ERCC6L2 riuscivano comunque a riparare i tagli netti indotti da Cas9 con soltanto piccole inserzioni o delezioni, le tipiche impronte della riparazione quotidiana del DNA. In netto contrasto, quando le rotture sfalsate venivano indotte da Cas12a, TALEN o Cas9 a due nickase, le cellule carenti di ERCC6L2 mostravano molte più delezioni ampie che raggiungevano migliaia di basi e riarrangiamenti cromosomici distanti tra loro, detti traslocazioni. Questi effetti sono stati osservati non solo in linee cellulari ingegnerizzate, ma anche in cellule del midollo osseo di pazienti portatori di mutazioni ereditarie in ERCC6L2, sottolineando la rilevanza clinica della scoperta. 
Quando molte rotture si accumulano, le cellule iniziano a cedere
I pericoli della perdita di ERCC6L2 sono diventati ancora più evidenti quando il gruppo ha indotto molteplici rotture sfalsate attraverso il genoma contemporaneamente. In questi esperimenti, le cellule senza ERCC6L2 faticavano a sopravvivere e formavano frequentemente micronuclei—piccoli corpi contenenti DNA mal posizionati che segnalano che i cromosomi si sono frantumati o sono stati segregati in modo errato. La stessa vulnerabilità è apparsa quando i ricercatori hanno considerato una fonte naturale di rotture sfalsate: l’enzima TOP2, che taglia temporaneamente il DNA per alleviare torsioni durante l’attività cellulare normale. Un farmaco chemioterapico, l’etoposide, intrappola TOP2 nello stato rotto, trasformando questi nick temporanei in rotture sfalsate durature. Le cellule prive di ERCC6L2 risultavano dramaticamente più sensibili all’etoposide e mostravano un’eccessiva erosione delle estremità del DNA, rispecchiando quanto osservato con rotture indotte da Cas12a.
Come ERCC6L2 controlla la macchina della riparazione
Per comprendere il funzionamento molecolare di ERCC6L2, il gruppo ha ricostituito il processo in provetta con proteine e DNA purificati. Hanno scoperto che ERCC6L2 si lega a molte forme di DNA ma possiede un talento particolare: può attivamente «fondere» o srotolare brevi estremità sporgenti sulle rotture sfalsate, e ciò richiede la sua attività motoria che consuma energia. Nelle cellule, ERCC6L2 bilancia un’altra macchina di riparazione, il complesso MRN, che normalmente smussa le estremità del DNA per creare tratti a singolo filamento. Questa escissione è utile in alcune vie di riparazione ma diventa pericolosa se eccessiva, portando a grandi delezioni e cromosomi spezzati. Nelle cellule carenti di ERCC6L2, l’escissione guidata da MRN procede senza controllo sulle rotture sfalsate. Bloccare MRN o il suo regolatore ATM ha invertito il consumo eccessivo del DNA e ridotto la frequenza di grandi delezioni, dimostrando che ERCC6L2 normalmente mantiene sotto controllo questa via.
Cosa significa per i pazienti e per l’editing genomico
Mettendo insieme questi pezzi, gli autori propongono che ERCC6L2 agisca come una guardiana specialistica per le rotture sfalsate del DNA. Fonde le estremità a sbalzo e favorisce una rapida e ordinata ricongiunzione, prevenendo lunghe perdite di DNA e giunzioni errate tra cromosomi distanti. Nelle persone nate con mutazioni in ERCC6L2, le fonti quotidiane di rotture sfalsate—in particolare quelle create da TOP2—probabilmente si accumulano non riparate o riparate in modo scorretto, guidando l’insufficienza del midollo osseo, la leucemia e possibilmente alcuni problemi neurologici. Per la terapia genica, lo studio manda un messaggio chiaro: gli strumenti di editing che creano intenzionalmente tagli a sbalzo, come Cas12a, TALEN o alcuni disegni di nickase, potrebbero essere particolarmente rischiosi in questi pazienti. Scegliere strategie di editing che evitino rotture sfalsate potrebbe essere essenziale per garantire che correggere un gene non destabilizzi accidentalmente il resto del genoma. 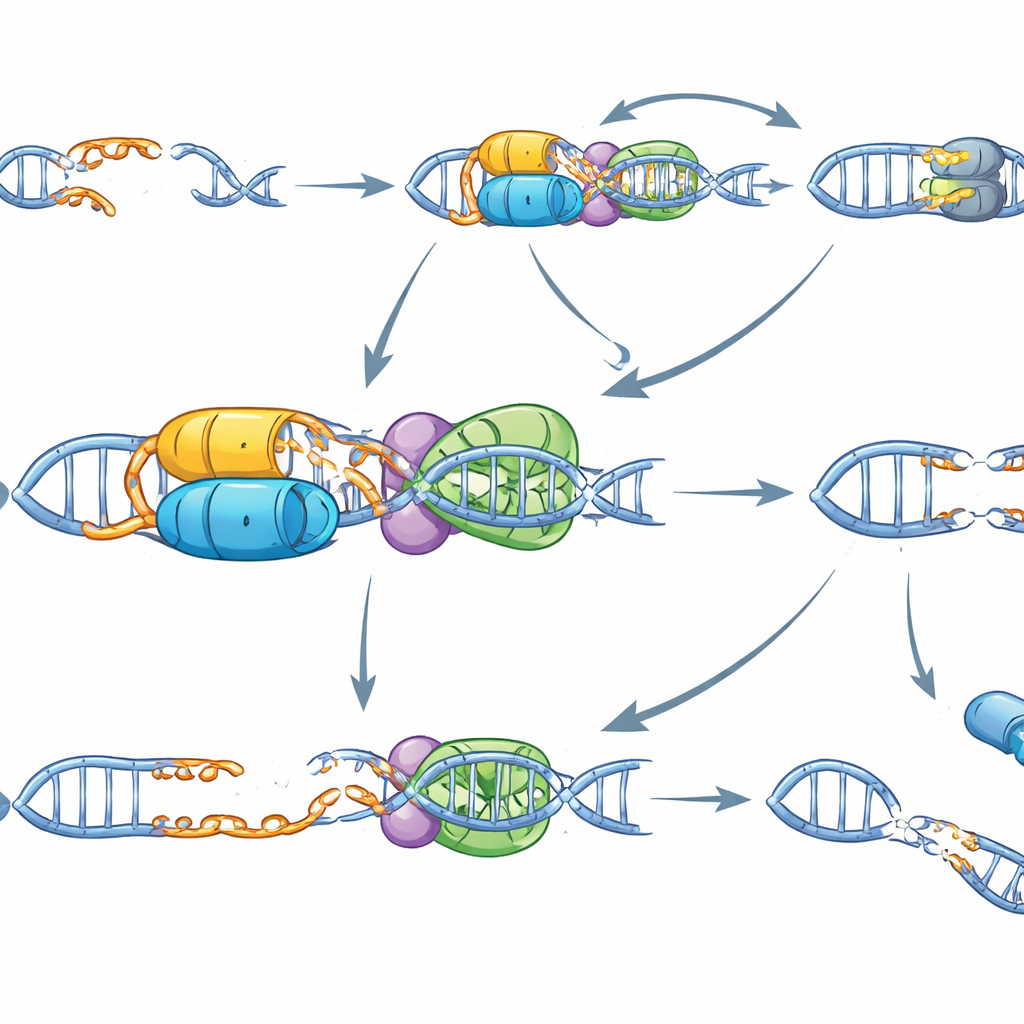
Citazione: Aird, E.J., Serrano-Benitez, A., Siegner, S.M. et al. ERCC6L2 ensures repair fidelity for staggered-end DNA double-strand breaks. Nat Commun 17, 2743 (2026). https://doi.org/10.1038/s41467-026-69843-w
Parole chiave: Riparazione del DNA, editing del genoma, rotture a doppio filamento, ERCC6L2, instabilità cromosomica