Clear Sky Science · it
Massimizzare l’utilizzo di energia e l’efficienza di lisciviazione del litio tramite doppia ossidazione elettrochimica sequenziale e immersione-rilassamento
Perché le vecchie batterie per auto contano ancora
Le batterie agli ioni di litio alimentano i nostri telefoni, laptop e, sempre più, le nostre auto. Ma quando milioni di pacchi di veicoli elettrici giungono al termine della loro vita utile, generano un nuovo tipo di rifiuto — e una nuova opportunità. Il litio e gli altri metalli racchiusi nelle batterie esauste sono preziosi ma costosi in termini energetici da recuperare. Questo studio esplora un modo più intelligente per estrarre il litio usando elettricità in modo più efficiente, riducendo costi e impatto ambientale pur rispondendo alla crescente domanda mondiale di materiali per batterie.
Trasformare le batterie esauste in una risorsa
Oggi la maggior parte del riciclo industriale delle batterie agli ioni di litio si basa su sostanze chimiche aggressive o forni ad alta temperatura. Questi metodi possono recuperare i metalli, ma spesso sprecano energia e rendono difficile separare il litio da nichel, cobalto e manganese nelle cosiddette batterie NCM. I ricercatori si sono concentrati su una via più recente e pulita: usare una corrente elettrica in acqua salina per estrarre il litio dal materiale catodico usato. Si sono posti una domanda semplice ma cruciale: possiamo riorganizzare quando e come utilizziamo l’elettricità in modo che quasi ogni watt contribuisca a rimuovere il litio anziché perdersi in reazioni laterali?
Un ballo in due fasi: potenza, poi quiete
Il team ha progettato un processo in due stadi che combina una spinta attiva con un “bagno” tranquillo. Nella prima fase, chiamata doppia ossidazione elettrochimica, viene applicata una tensione costante attraverso una cella contenente un catodo NCM esausto e una soluzione di cloruro di sodio. La corrente estrae ioni litio dal solido verso il liquido e al contempo genera specie ossidanti potenti nella soluzione. Gli scienziati hanno scoperto che la maggior parte del lavoro utile avviene nella prima ora: il litio lascia rapidamente la struttura cristallina all’inizio, mentre più tardi gran parte dell’energia viene sprecata in reazioni laterali come la formazione di bolle di ossigeno.
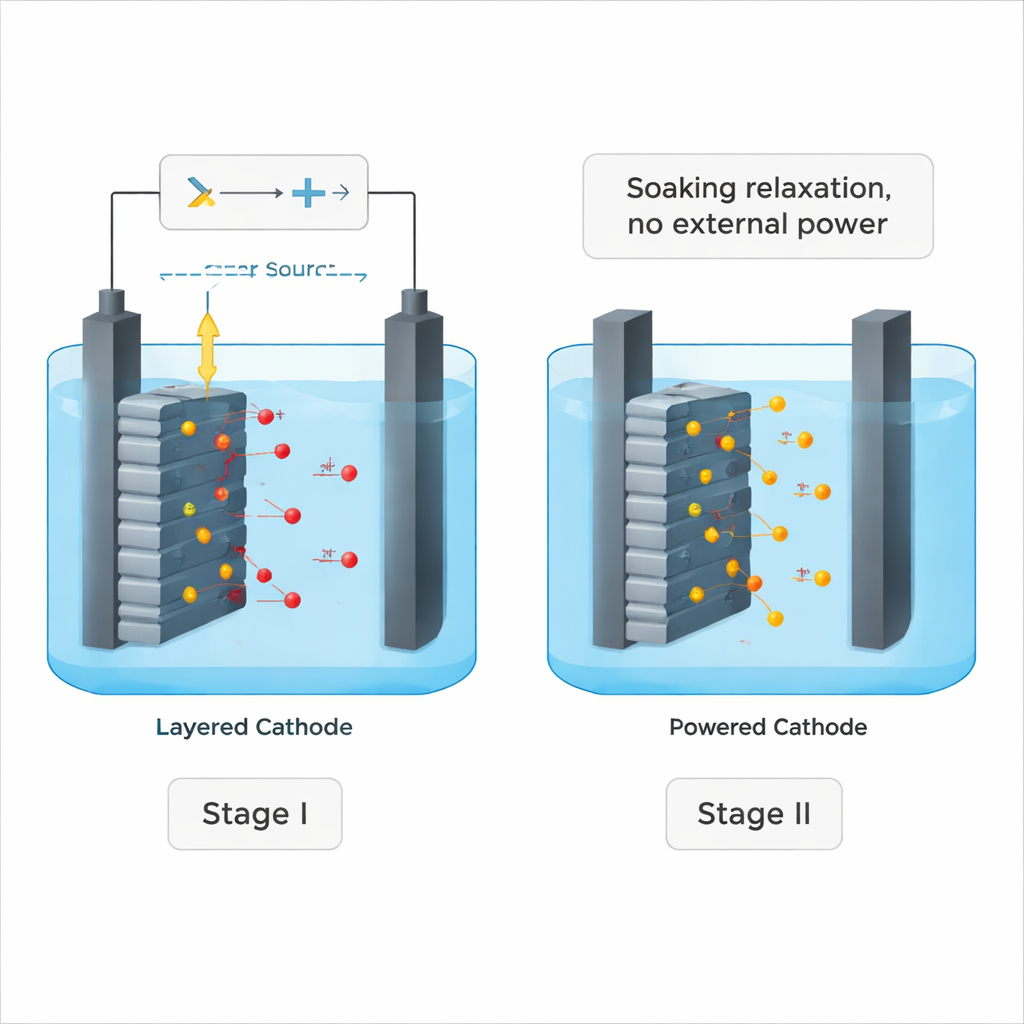
Lasciare che la chimica finisca il lavoro
Invece di continuare ad applicare corrente sempre più a lungo, i ricercatori hanno semplicemente spento l’alimentazione e lasciato l’elettrodo in immersione nella soluzione salina ora ossidante. Sorprendentemente, il litio ha continuato a lisciviare finché quasi tutto non è stato rimosso — raggiungendo circa il 99% di recupero per materiale NCM fresco e circa il 98% per catodi esausti reali. Misurazioni dettagliate hanno mostrato che atomi di ossigeno all’interno del cristallo, temporaneamente portati a uno stato più reattivo durante la fase alimentata, sono diventati il motore nascosto di questa seconda fase silenziosa. Queste specie di ossigeno “attivate” hanno favorito uno scambio lento: ioni litio sono diffusi nel liquido mentre ioni sodio (o potassio) dalla soluzione si infilavano negli spazi vuoti, il tutto senza ulteriore apporto elettrico.
Come si riarrangia la struttura cristallina
Usando microscopi elettronici, diffrazione a raggi X e spettroscopia, il team ha osservato le particelle del catodo fessurarsi, assottigliarsi e modificare il loro impilamento interno man mano che il litio partiva. Il materiale ha attraversato diversi arrangiamenti stratificati conosciuti passando da uno stato ricco di litio a uno povero, fino a una forma ricca di sodio che ha mantenuto la struttura ma non conteneva più molto litio. Durante questo processo, atomi di nichel e cobalto hanno cambiato i loro stati di carica per mantenere l’equilibrio elettrico complessivo del materiale, mentre il manganese è rimasto per lo più invariato, contribuendo a stabilizzare il reticolo. I ricercatori hanno anche mostrato che gli ioni potassio, che perdono più facilmente le loro molecole d’acqua rispetto al sodio, possono accelerare ulteriormente il passaggio di scambio ionico.
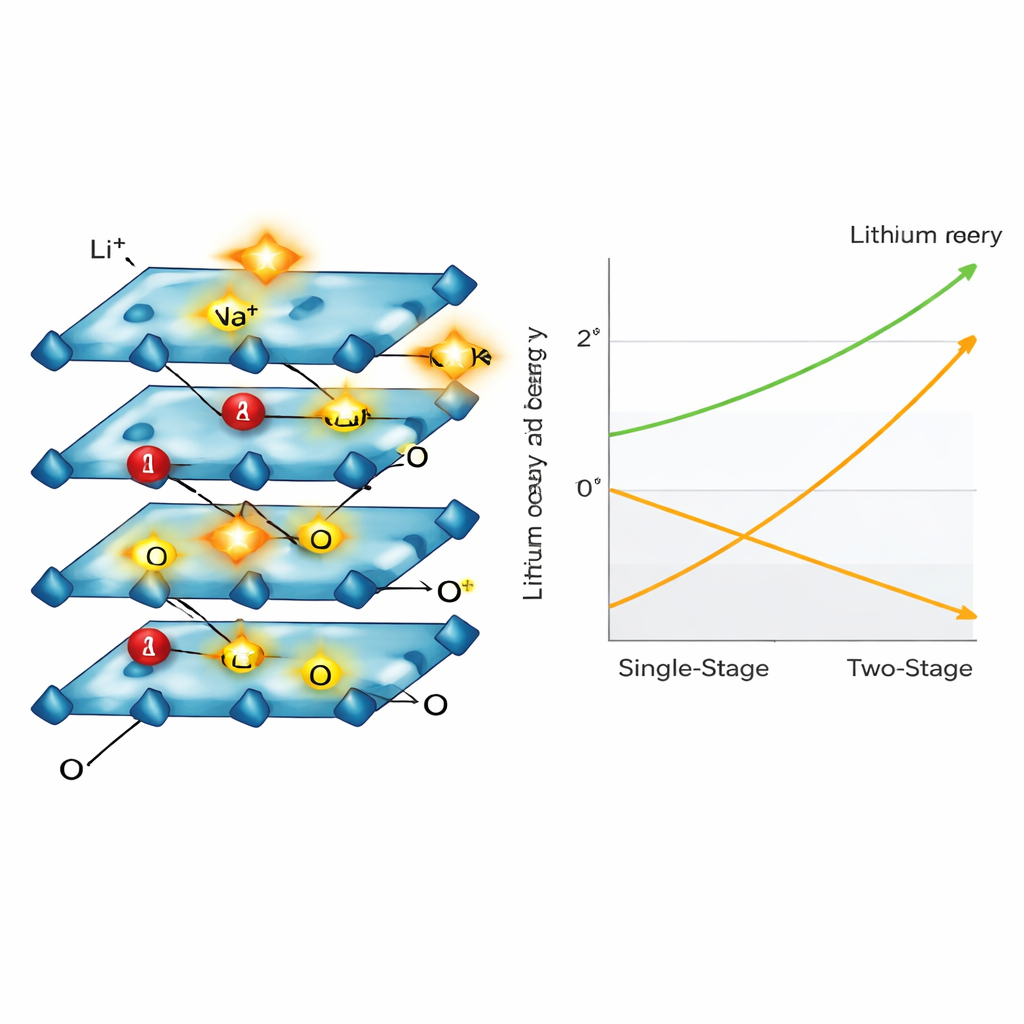
Dal banco di laboratorio al piano industriale
Per verificare se l’idea potesse funzionare fuori dal laboratorio, il team ha costruito un impianto pilota capace di trattare mezzo chilogrammo di rifiuto di batterie reale per lotto. Usando il loro metodo in due fasi, hanno recuperato oltre il 98% del litio come carbonato di litio ad alta purezza, idoneo per la produzione di nuove batterie. Fondamentale è che, poiché la corrente viene spenta una volta che la “chimica intelligente” è stata messa in moto, il processo ha utilizzato circa la metà dell’energia elettrica rispetto a un metodo elettrochimico monostadio standard, risparmiando più di un quinto del profitto operativo totale per tonnellata di materiale catodico riciclato.
Cosa significa per le batterie del futuro
In parole semplici, lo studio dimostra che non è sempre necessario continuare a immettere elettricità per recuperare materiali preziosi dalle vecchie batterie. Un impulso di potenza ben temporizzato può preparare il materiale e la soluzione in modo che il resto del lavoro avvenga da solo, guidato da forze chimiche interne. Se adottato su scala, questo approccio in due fasi potrebbe rendere il riciclo del litio da batterie NCM esaurite più economico, più pulito e più attraente per l’industria, contribuendo a chiudere il ciclo di vita delle batterie e ad alleviare la pressione sull’estrazione di nuovo litio.
Citazione: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Parole chiave: riciclo del litio, rifiuti di batterie, lisciviazione a basso consumo energetico, catodi NCM, recupero elettrochimico