Clear Sky Science · it
Sopravvivenza delle cianobatteri e mitigazione degli effetti tossici del Fe(II) in un oceano arcaico ricco di silice
Mari antichi e l'aria che respiriamo
Miliardi di anni prima che esistessero animali o piante, minuscoli microbi fotosintetici chiamati cianobatteri iniziarono a rilasciare ossigeno negli oceani della Terra. Eppure passarono centinaia di milioni di anni prima che l'ossigeno si accumulasse nell'atmosfera. Questo studio indaga perché quel ritardo fu così lungo e se la chimica dei mari primordiali — ricca di ferro e silice disciolti — abbia favorito o ostacolato quei microbi che alla fine resero il nostro pianeta respirabile.

Oceani ricchi di ferro e un effetto collaterale tossico
I mari antichi contenevano grandi quantità di ferro disciolto, specialmente nelle regioni costiere dove acque profonde risalivano verso la superficie. Quando questo ferro incontrava l'ossigeno rilasciato dai cianobatteri, si ossidava formando minerali ferrici che in seguito diventarono le formazioni di ferro a strati — rocce a bande che sono alcuni dei nostri archivi geologici più antichi. Ma le stesse reazioni possono anche generare “specie reattive dell'ossigeno”, forme altamente aggressive di ossigeno che possono danneggiare DNA, proteine e membrane cellulari. Lavori precedenti avevano suggerito che questa reazione chimica indotta dal ferro potesse avvelenare i cianobatteri, rallentandone la diffusione e ritardando l'aumento di ossigeno nell'atmosfera.
La silice come guardia inaspettata
Gli autori si sono concentrati su un altro ingrediente abbondante dell'acqua marina primitiva: la silice disciolta, lo stesso materiale di base del vetro. Le evidenze geologiche suggeriscono che gli oceani antichi contenevano concentrazioni di silice ben più alte rispetto a oggi. In esperimenti di laboratorio hanno coltivato un cianobatterio marino (Synechococcus sp. PCC 7002) in condizioni controllate con diverse quantità di ferro e silice disciolti. Hanno monitorato la velocità di crescita delle cellule, la quantità di ossigeno prodotta, la rapidità con cui il ferro veniva ossidato e la formazione di specie reattive dell'ossigeno. A bassi livelli di ferro le cellule prosperavano indipendentemente dalla silice. Ma quando il ferro era molto elevato — simile a condizioni attese in alcune acque costiere dell'Archeano — le colture senza silice aggiunta vacillavano, mentre quelle con alta silice restavano attive, producevano più ossigeno e raggiungevano numeri cellulari maggiori.
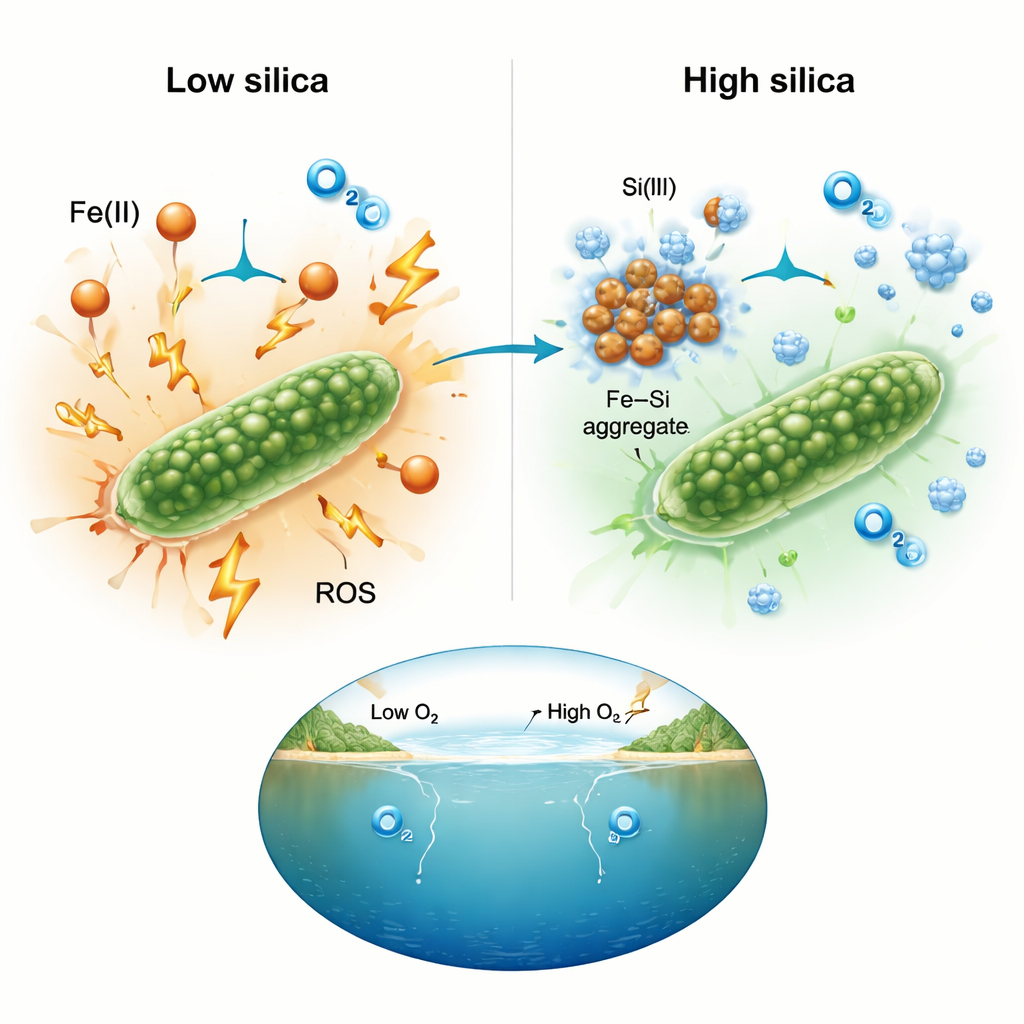
Cooperazione chimica che attenua reazioni dannose
Per capire perché la silice facesse la differenza, il gruppo ha misurato direttamente le specie reattive dell'ossigeno usando sonde fluorescenti. A livelli elevati di ferro, le colture prive di silice mostravano forti segnali di specie reattive dell'ossigeno, coerenti con una chimica stressante intorno alle cellule. Negli allestimenti ricchi di silice, quei segnali restavano vicini ai livelli di fondo anche quando le concentrazioni di ferro erano estreme. I ricercatori interpretano questo come effetto della legatura della silice al ferro disciolto e della formazione di aggregati ferro‑silice. Una volta intrappolato in questi agglomerati, il ferro è meno disponibile a alimentare le reazioni a catena che generano ossidanti dannosi. L'effetto netto è un ambiente chimico più mite in cui i cianobatteri possono continuare a fotosintetizzare invece di essere compromessi dallo stress ossidativo.
Ritmi giorno‑notte e impatti a scala oceanica
Gli esperimenti sono stati condotti anche con cicli luce‑buio realistici anziché con illuminazione costante. In queste condizioni alternate, i cianobatteri ossidavano il ferro più rapidamente e tolleravano meglio acque ad alto contenuto di ferro, suggerendo che i periodi di “riposo” notturno riducono lo stress a lungo termine. Utilizzando i tassi di produzione di ossigeno misurati in laboratorio, gli autori hanno costruito un semplice modello numerico di una colonna d'acqua oceanica primitiva. Per abbondanze plausibili di cianobatteri e tassi realistici di risalita di acque profonde, hanno trovato che le acque superficiali potevano diventare ricche di ossigeno mentre gli strati più profondi rimanevano ricchi di ferro. In molti scenari, le concentrazioni di ossigeno nella zona illuminata dal sole raggiungevano o superavano i livelli di saturazione tipici del mare moderno, con la conseguenza che “oasi” locali di ossigeno sopra profondità ricche di ferro potrebbero essere state comuni.
Riconsiderare perché l'ossigeno impiegò tanto
Nel complesso i risultati suggeriscono che le specie reattive dell'ossigeno formate da ferro e ossigeno probabilmente non furono un ostacolo insormontabile per i cianobatteri primitivi, a condizione che la silice fosse abbondante e che prevalessero cicli naturali giorno‑notte. Invece di essere cronicamente avvelenati, questi microbi probabilmente trovarono molti ambienti costieri in cui la silice attenuava gli effetti collaterali dannosi del ferro, permettendo loro di crescere, ossidare grandi quantità di ferro e rilasciare ossigeno in eccesso nell'atmosfera. Il mistero persistente sul perché l'atmosfera terrestre si ossigenò così tardi deve quindi risiedere più in fattori su larga scala — come la velocità con cui l'ossigeno veniva consumato da gas vulcanici e rocce — che nella chimica locale attorno a singole cellule microbiche.
Citazione: Dreher, C.L., Cirpka, O.A., Schad, M. et al. Survival of cyanobacteria and mitigation of Fe(II) toxicity effects in a silica-rich Archean ocean. Nat Commun 17, 1987 (2026). https://doi.org/10.1038/s41467-026-69826-x
Parole chiave: ossigeno della Terra primordiale, cianobatteri, formazioni di ferro a strati, specie reattive dell'ossigeno, oceani ricchi di silice