Clear Sky Science · it
La colecistochinina derivata dalle cellule beta guida lo sviluppo dell'adenocarcinoma pancreatico associato all'obesità
Quando il peso in eccesso parla al pancreas
È noto che l'obesità aumenta il rischio di cancro del pancreas, uno dei tumori più letali, ma la "conversazione" biologica che collega il grasso corporeo in eccesso ai tumori è stata a lungo sfuggente. Questo studio svela un messaggero inaspettato: un ormone digestivo chiamato colecistochinina, o CCK, prodotto all'interno delle cellule che sintetizzano insulina nel pancreas. Tracciando come queste cellule cambiano sotto stress metabolico, gli autori mostrano in che modo un ormone pensato per aiutare l'organismo a far fronte alla situazione possa invece alimentare il cancro, suggerendo nuove modalità per intercettare la malattia prima che prenda piede.
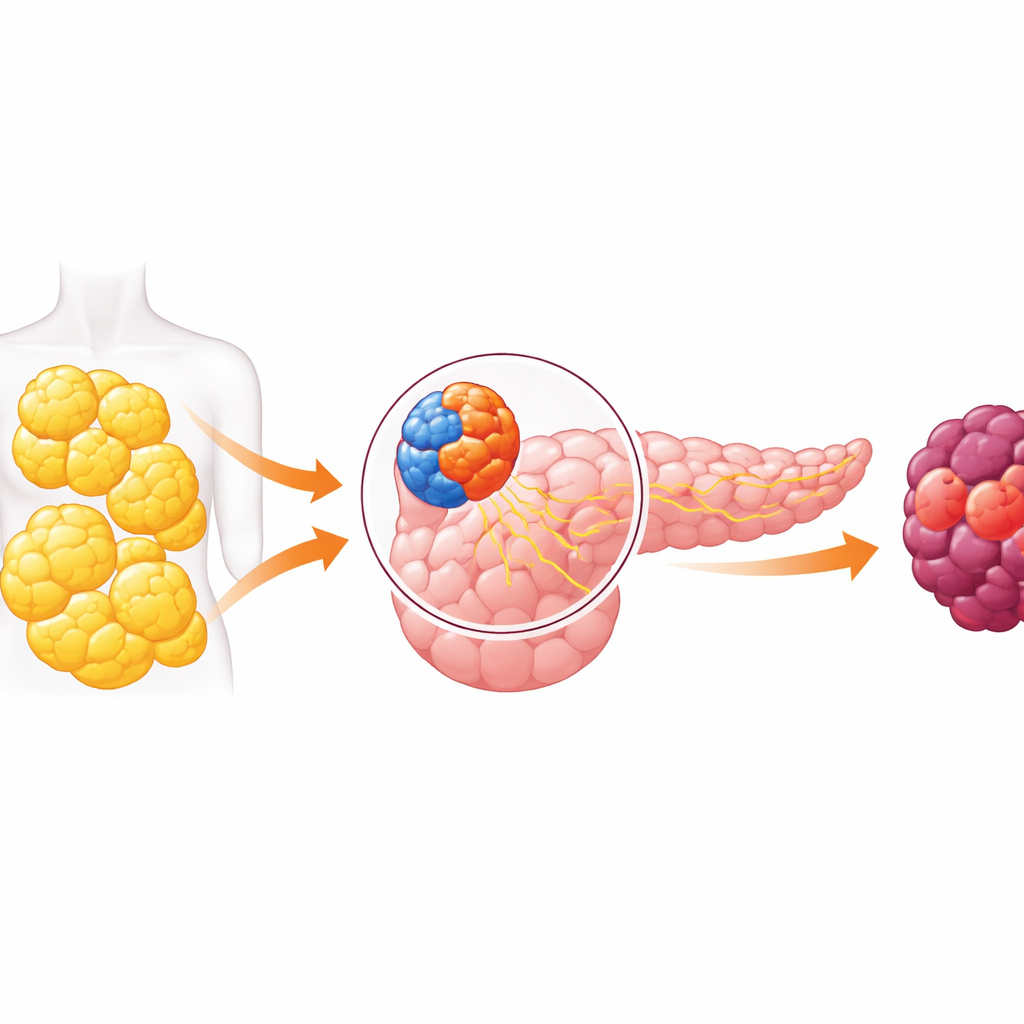
Un organo a due facce e un dialogo pericoloso
Il pancreas ha due funzioni principali. Da un lato, la porzione endocrina contiene minuscole isole di cellule che rilasciano ormoni come l'insulina per controllare la glicemia. Dall'altro, la parte esocrina produce succhi digestivi e include le cellule che più spesso danno origine al cancro pancreatico. Per anni i ricercatori hanno assunto che questi compartimenti operassero in gran parte in isolamento. Lavori recenti hanno ribaltato questa idea, mostrando che i segnali provenienti dalle cellule produttrici di ormoni possono influenzare le cellule digestive vicine. Questo articolo esplora quel dialogo trasversale e scopre che, nell'obesità, può spingere il lato esocrino del pancreas verso il cancro.
Lo stress nelle cellule endocrine accende un nuovo segnale
Nell'obesità, le cellule beta produttrici di insulina sono sottoposte a pressione costante per far fronte alla crescente richiesta di insulina. Utilizzando sequenziamento dell'RNA a singola cellula e strumenti computazionali avanzati, i ricercatori hanno seguito singole cellule beta mentre i topi passavano da snelli a sovrappeso fino a gravemente obesi. Hanno osservato che una sotto-popolazione di cellule beta immature si espandeva e progressivamente perdeva la propria identità specializzata di produttrici di insulina. Con l'aumentare dello stress in queste cellule, sono cresciuti i marcatori di problemi nel ripiegamento delle proteine e di danno cellulare, mentre la produzione di insulina calava. Allo stesso tempo, queste cellule cominciavano a produrre alti livelli di CCK, un ormone solitamente associato all'intestino che può stimolare le cellule digestive a proliferare e trasformarsi.
Da ormone utile a combustibile per il cancro
Per verificare se la CCK neo-prodotta fosse solo un sottoprodotto dello stress o un vero motore della malattia, il gruppo ha ingegnerizzato topi le cui cellule beta producevano quantità extra di CCK, anche in assenza di obesità. Questi animali hanno sviluppato lesioni precancerose pancreatiche e tumori invasivi in misura simile ai topi obesi, pur avendo peso e glicemia normali. Al contrario, quando la CCK è stata rimossa specificamente dal pancreas di topi obesi, il carico tumorale è diminuito sensibilmente, nonostante gli animali restassero pesanti e con alti livelli di insulina. In diversi modelli murini, i livelli di CCK nel pancreas correlavano strettamente con la quantità di tumore, mentre i livelli di insulina tendevano ad andare nella direzione opposta. Ciò indica che, in questi sistemi, è la CCK — non l'insulina — l'ormone dominante che collega obesità e cancro pancreatico.
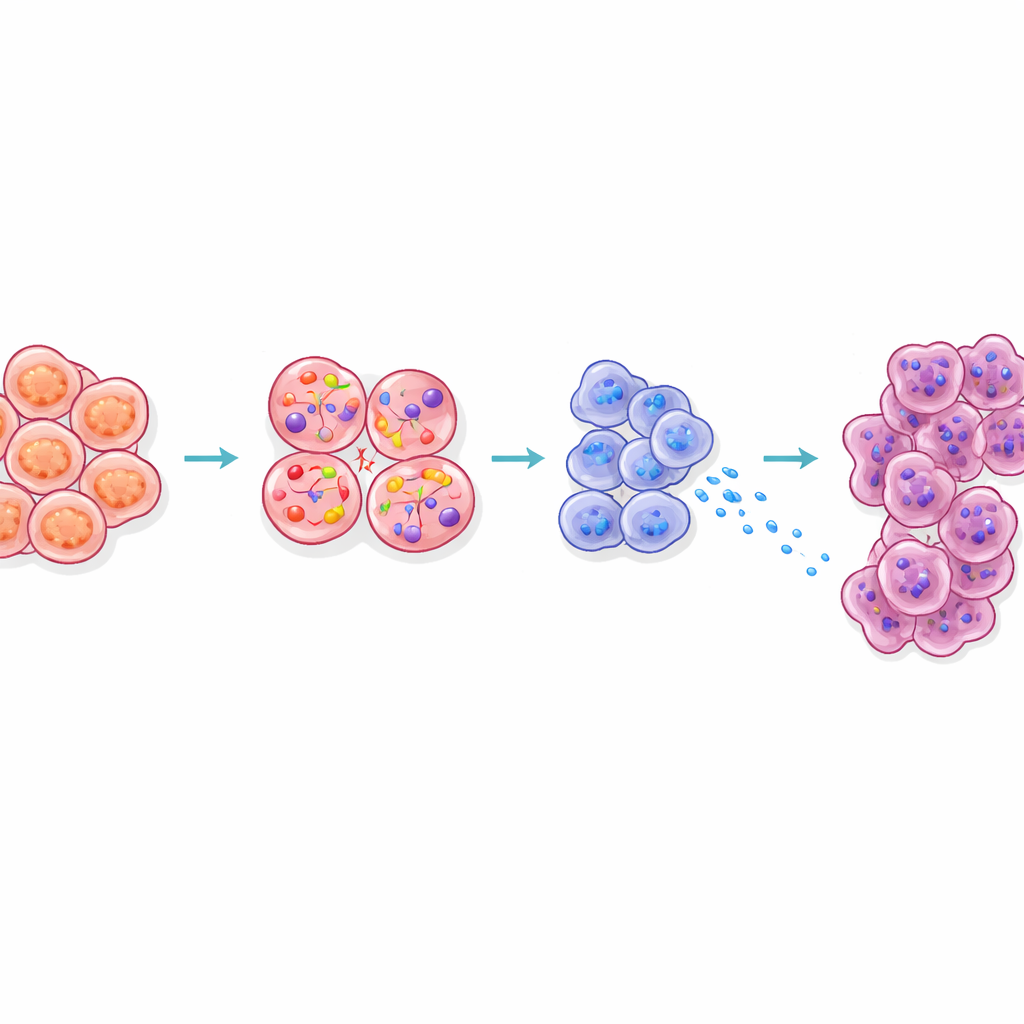
Come il segnale raggiunge e prepara le cellule vicine
Lo studio ha anche esaminato come la CCK proveniente dalle cellule beta rimodelli il tessuto circostante. Le cellule acinari, che normalmente secernono enzimi digestivi, si trovano a stretto contatto con le isole pancreatiche. Nei topi obesi, le cellule acinari vicine alle isole mostravano un profilo di stress, producevano più enzimi digestivi e proteine appartenenti alla famiglia Reg, e mutavano in stati noti per essere più facilmente trasformabili in cellule tumorali. Il blocco della segnalazione della CCK nei topi obesi riduceva questi segnali Reg. L'imaging tridimensionale ha inoltre rivelato che le lesioni precancerose precoci tendevano a sorgere in modo anomalo vicino alle isole negli animali obesi. Nel loro insieme, questi risultati suggeriscono che la diffusione di CCK da cellule beta stressate crea una "zona calda" attorno alle isole dove le cellule digestive sono predisposte a diventare tumori.
Pattern condivisi con il diabete umano e un interruttore chiave
Confrontando i dati murini con tessuto pancreatico umano proveniente da persone con e senza diabete di tipo 2, gli autori hanno trovato paralleli notevoli: le cellule beta dei donatori diabetici si collocavano negli stessi stati stressati e meno maturi osservati nei topi obesi. Hanno quindi utilizzato un'analisi regolatoria per chiedersi cosa attivi la CCK nelle cellule beta e hanno identificato una via sensibile allo stress centrata sulla proteina cJun. Quando hanno bloccato la via JNK–cJun a monte nei topi obesi o in cellule simili alle beta in coltura, i livelli di CCK sono diminuiti, e cJun è stato osservato legarsi vicino a una regione regolatoria del gene CCK. Ciò suggerisce che lo stress cronico attiva JNK–cJun, che a sua volta fa sì che le cellule beta si convertano in uno stato produttore di CCK.
Cosa significa per le persone a rischio
Per un lettore non specialista, il messaggio centrale è che, sotto la pressione dell'obesità e del diabete, le cellule insuliniche del pancreas non si limitano a guastarsi: si adattano in modo che involontariamente incoraggia le cellule vicine a formare il cancro. Lo fanno accendendo la produzione di CCK, un ormone che funziona come segnale di crescita e di stress per le cellule digestive circostanti, contribuendo a creare un terreno fertile per i tumori. Poiché la CCK pancreatica non è essenziale per il controllo della glicemia, mirare a questa fonte ormonale specifica o al suo interruttore attivato dallo stress potrebbe, in linea di principio, ridurre il rischio di cancro del pancreas nelle persone con obesità o diabete di tipo 2 senza compromettere l'equilibrio ormonale complessivo. Il lavoro rimette in gioco il cancro pancreatico come una malattia di comunicazione deviata tra le due componenti dell'organo e indica nuove strade per la prevenzione precoce.
Citazione: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Parole chiave: cancro del pancreas, obesità, cellule beta, colecistochinina, diabete di tipo 2