Clear Sky Science · it
Interazioni metal-supporto modulati per un'elettroreduction del nitrato efficiente a potenziali positivi
Trasformare l'acqua inquinata in una risorsa utile
L'inquinamento da nitrati in fiumi, laghi e acque reflue industriali è una preoccupazione crescente per gli ecosistemi e la salute umana, ma rappresenta anche una risorsa sprecata. Lo stesso azoto che danneggia i corsi d'acqua può essere riconvertito in ammoniaca, pilastro di concimi, combustibili e prodotti chimici. Questo studio esplora un nuovo modo per depurare l'acqua contaminata da nitrati recuperando ammoniaca mediante elettricità in modo più efficiente rispetto al passato, indicando strade verso un'agricoltura più pulita, un trattamento dei rifiuti più intelligente e nuove forme di accumulo energetico.
Perché l'azoto in eccesso è un problema
L'agricoltura e l'industria moderne dipendono fortemente dall'ammoniaca, prodotta principalmente dal dispendioso processo Haber–Bosch. Durante l'uso e lo smaltimento, gran parte di questa ammoniaca finisce come nitrato nelle acque reflue, alterando il ciclo naturale dell'azoto e contribuendo a problemi ambientali come fioriture algali e contaminazione delle acque potabili. I metodi esistenti per rimuovere i nitrati possono essere costosi e spesso si limitano a seppellire o diluire il problema. La conversione elettrochimica dei nitrati in ammoniaca offre un modo per depurare l'acqua riciclando l'azoto, ma la maggior parte dei sistemi attuali richiede un elevato apporto energetico perché deve funzionare a potenziali fortemente negativi.
Progettare una superficie catalitica più intelligente
Per affrontare questa sfida, i ricercatori hanno progettato un nuovo catalizzatore costituito da piccolissimi agglomerati di rutenio ancorati su sottili fogli di idrossido di cobalto. Hanno usato un metodo semplice di «autocorrosione»: una schiuma metallica si dissolve lentamente in presenza di un sale di rutenio e ossigeno, formando uno strato fresco di idrossido mentre agglomerati di rutenio si depositano direttamente su di esso. Questo processo può essere applicato a metalli diversi, ma il team si è concentrato sui supporti a base di cobalto, nichel e ferro per valutare come ciascuno influenzi le prestazioni. Microscopia e spettroscopia hanno confermato che gli agglomerati di rutenio sono ultrafini e distribuiti in modo uniforme sui fogli di idrossido, e che avvengono spostamenti di elettroni tra il metallo e il suo supporto, modulando sottilmente l'interazione della superficie con nitrato e acqua.

Equilibrare presa e flusso per una conversione migliore
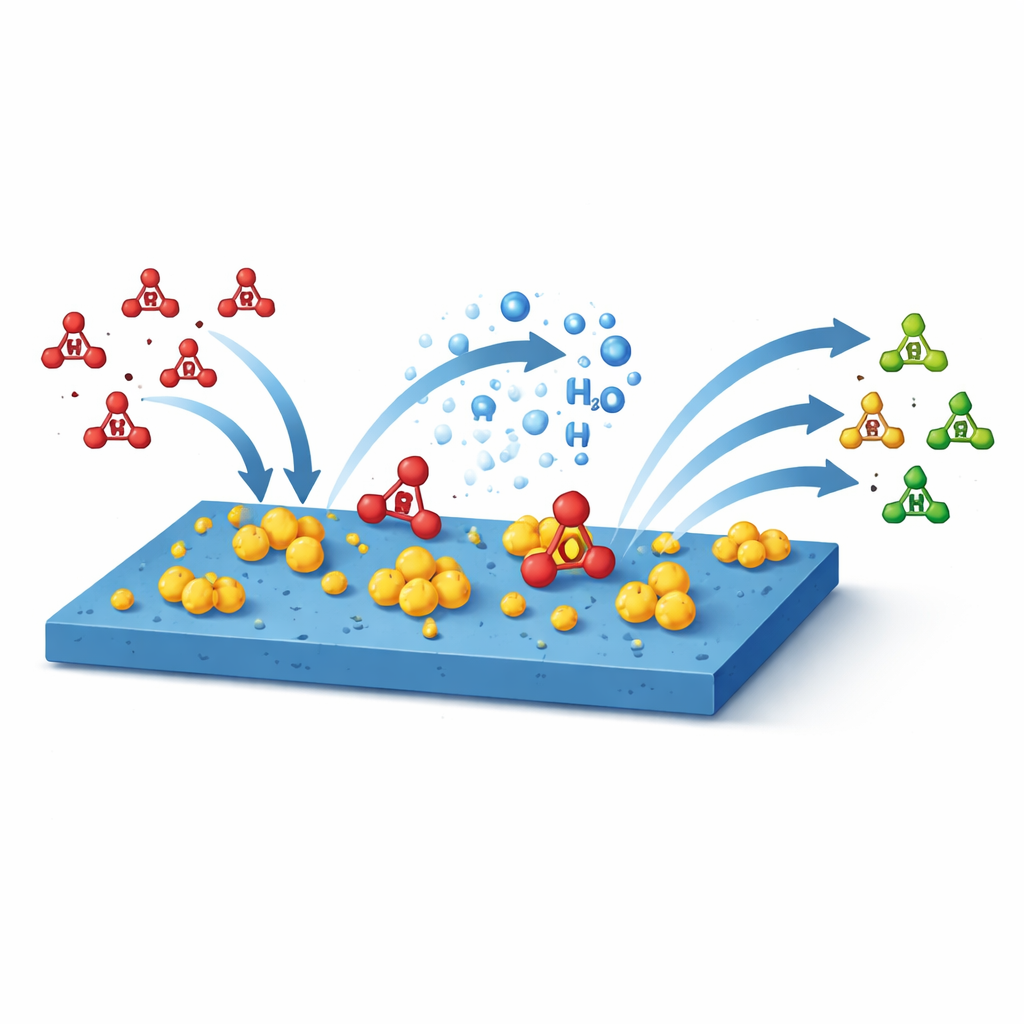
Perché la reazione proceda in modo efficiente, devono verificarsi in armonia due condizioni: il nitrato deve aderire alla superficie catalitica con sufficiente forza per reagire, e l'acqua all'interfaccia deve scindersi per fornire gli atomi di idrogeno «attivi» che gradualmente trasformano il nitrato in ammoniaca. Se il nitrato si lega troppo saldamente, la superficie si intasa; se troppo debolmente, scivola via senza essere usato. Allo stesso modo, una lenta dissociazione dell'acqua priva la reazione di idrogeno. I test hanno mostrato che il catalizzatore a base di cobalto trova questo punto di equilibrio. Rispetto alle versioni su nichel e ferro, avvia la reazione a un potenziale più vicino all'ideale, raggiunge quasi il 100% di selettività per l'ammoniaca e ottiene un'efficienza energetica di circa il 50% a un potenziale operativo positivo — richiesta energetica insolitamente bassa per questa chimica. Mantiene inoltre alta attività per oltre 1.200 ore a densità di corrente rilevanti per l'industria, riducendo i nitrati in acque reflue simulate al di sotto dei limiti per le acque potabili.
Scrutare i passaggi nascosti
Per capire perché il cobalto funzioni meglio, il team ha monitorato la reazione in tempo reale con sonde ottiche ed elettrochimiche e ha corroborato le osservazioni con modellizzazione al calcolatore. Hanno scoperto che il supporto in idrossido di cobalto rimodella il sottile strato d'acqua sulla superficie, indebolendo la sua rete di legami a idrogeno in modo che le molecole d'acqua si scindano più facilmente in frammenti reattivi. Allo stesso tempo, l'interazione elettronica tra idrossido di cobalto e rutenio regola la forza con cui il nitrato e i suoi intermedi si legano. I calcoli mostrano che su questa superficie il passaggio più difficile — la conversione di un frammento di tipo nitrosile in una specie più ricca di idrogeno — richiede molta meno energia rispetto alle versioni supportate su nichel o ferro. Di fatto, il supporto in cobalto fornisce il giusto equilibrio: il nitrato è trattenuto saldamente ma non intrappolato, e l'acqua fornisce idrogeno rapidamente, permettendo alla sequenza di passaggi dal nitrato all'ammoniaca di procedere senza intoppi.
Dal trattamento dei rifiuti alla produzione di energia e al riciclo della plastica
Sfruttando il catalizzatore efficiente, gli autori hanno assemblato una batteria ricaricabile che abbina il metallo zinco con la riduzione dei nitrati al catodo cobalto–rutenio. Durante la scarica, il nitrato viene convertito in ammoniaca mentre lo zinco si ossida, fornendo energia elettrica. Durante la carica, sostituiscono la consueta reazione di formazione di ossigeno con l'ossidazione più dolce del glicole etilenico, un mattoncino chimico che può essere recuperato dalla plastica di scarto. Questa variazione riduce l'energia necessaria per ricaricare la batteria e valorizza le molecole derivate dalla plastica in prodotti di maggior pregio, mentre l'ammoniaca prodotta può formare sali ammonici. Il dispositivo ibrido funziona in modo stabile su molti cicli, illustrando come controllo dell'inquinamento, recupero di risorse e stoccaggio energetico possano essere integrati in un unico sistema.
Una nuova leva per una chimica più pulita
In termini accessibili, questo lavoro mostra che una messa a punto fine dell'interazione tra un catalizzatore metallico e il materiale di supporto può migliorare drasticamente l'efficienza della conversione di nitrati dannosi in acqua in ammoniaca utile. Scegliendo un supporto che non afferri i nitrati troppo forte né li lasci andare, e che aiuti l'acqua a frammentarsi per alimentare la reazione, i ricercatori raggiungono alta efficienza a potenziali più miti e mantengono le prestazioni per lunghi periodi. Lo stesso principio di progetto — regolare con cura le interazioni metallo-supporto — potrebbe guidare lo sviluppo di futuri catalizzatori per molti altri processi chimici sostenibili.
Citazione: Tang, Y., Wan, Y., Yan, W. et al. Modulated metal-support interactions for efficient nitrate electroreduction at positive potentials. Nat Commun 17, 3006 (2026). https://doi.org/10.1038/s41467-026-69802-5
Parole chiave: inquinamento da nitrati, produzione di ammoniaca, elettrocatalisi, trattamento delle acque reflue, stoccaggio di energia