Clear Sky Science · it
Analoghi non idrolizzabili dell'acetillisina per studiare l'acetilazione proteica in vitro e nelle cellule
Perché piccoli marchi chimici sulle proteine contano
All'interno di ogni cellula, le proteine vengono continuamente modificate con piccoli marchi chimici che funzionano come interruttori on/off o come dimmer della loro attività. Uno dei più importanti di questi marchi è l'acetilazione, che può cambiare il comportamento di una proteina senza alterare il codice genetico sottostante. Capire esattamente cosa fa l'acetilazione in un sito specifico su una proteina specifica è sorprendentemente difficile, perché le cellule possono rimuovere questi marchi con la stessa rapidità con cui li aggiungono. Questo studio introduce un intelligente «sostituto» chimico dell'acetilazione che non può essere rimosso, fornendo agli scienziati un modo per fissare questi interruttori e osservare cosa succede.
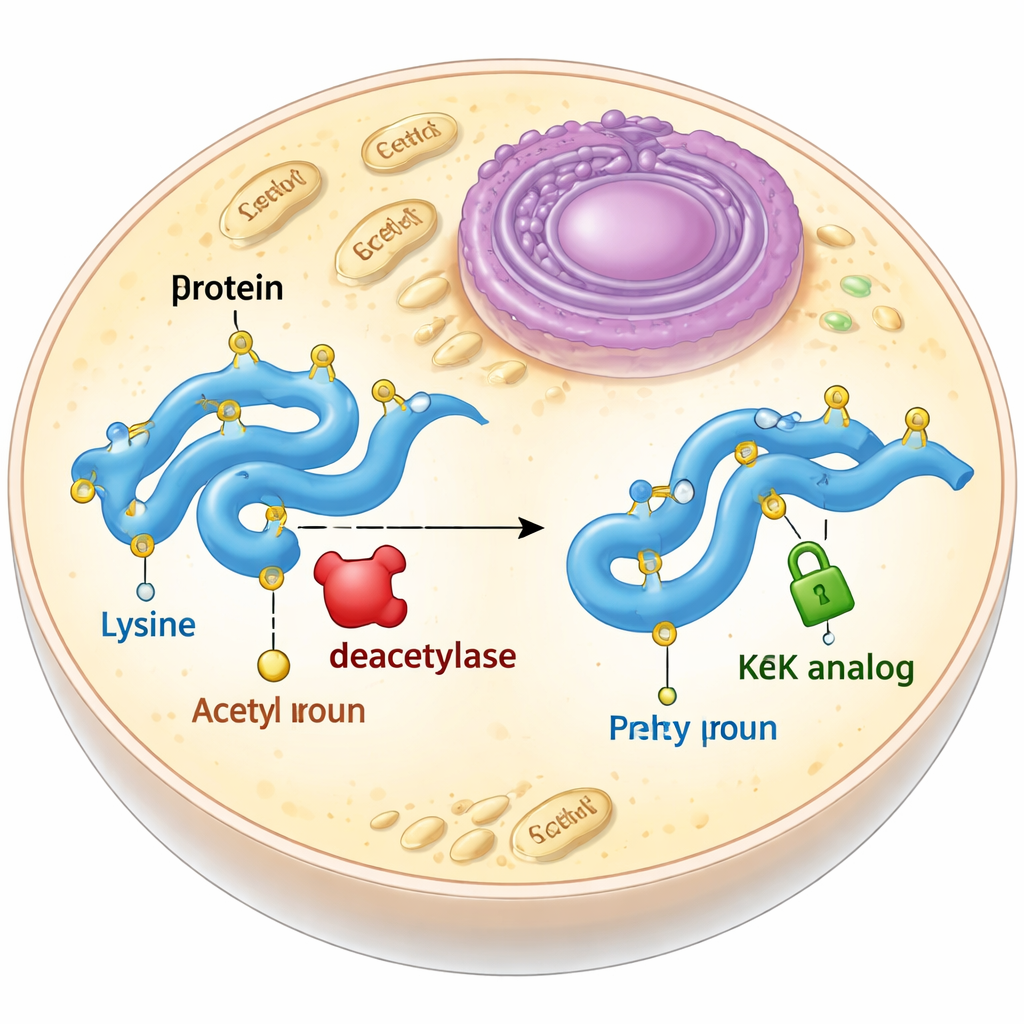
Un sostituto stabile per un marchio effimero
L'acetilazione avviene di solito su un componente delle proteine chiamato lisina. Quando una lisina è acetilata, perde la carica positiva e la sua catena laterale diventa leggermente più lunga. I biologi cercano spesso di mimare questo effetto mutando la lisina in un altro amminoacido, la glutammina, che è neutra ma più corta, o inserendo vera acetillisina tramite l'espansione del codice genetico. Entrambi gli approcci hanno limiti: la glutammina non riproduce completamente i cambiamenti conformazionali indotti dall'acetilazione, e la vera acetillisina viene rapidamente rimossa da enzimi detti deacetilasi all'interno delle cellule. Gli autori si sono dunque posti l'obiettivo di progettare e testare analoghi dell'acetillisina che mantengano la giusta dimensione e forma ma non possano essere rimossi.
Testare nuovi mimetici chimici su una proteina modello
Il gruppo ha concentrato l'attenzione inizialmente sull'ubiquitina, una piccola proteina ben studiata che essa stessa viene decorata con diversi marchi. Usando avanzate tecniche di ingegneria genetica, hanno inserito varianti di lisina in una posizione di ubiquitina: acetillisina naturale, due analoghi non rimovibili chiamati TFAcK e ketolysina (KeK), e sostituti comuni come glutammina, alanina e arginina. Hanno quindi esaminato come questi cambiamenti influenzassero la struttura e la funzione dell'ubiquitina. Misurazioni NMR ad alta risoluzione hanno mostrato che acetillisina, TFAcK e KeK producono cambiamenti strutturali quasi identici, specialmente attorno a un'elica centrale, mentre la glutammina e altre mutazioni semplici non lo fanno. Test funzionali con un enzima chiamato HDM2 hanno rivelato che l'ubiquitina contenente acetillisina, TFAcK o KeK si comportava in modo simile fra loro e distinto dalla versione con glutammina, sottolineando che la lunghezza e l'ingombro della catena laterale — non solo la carica — sono cruciali.
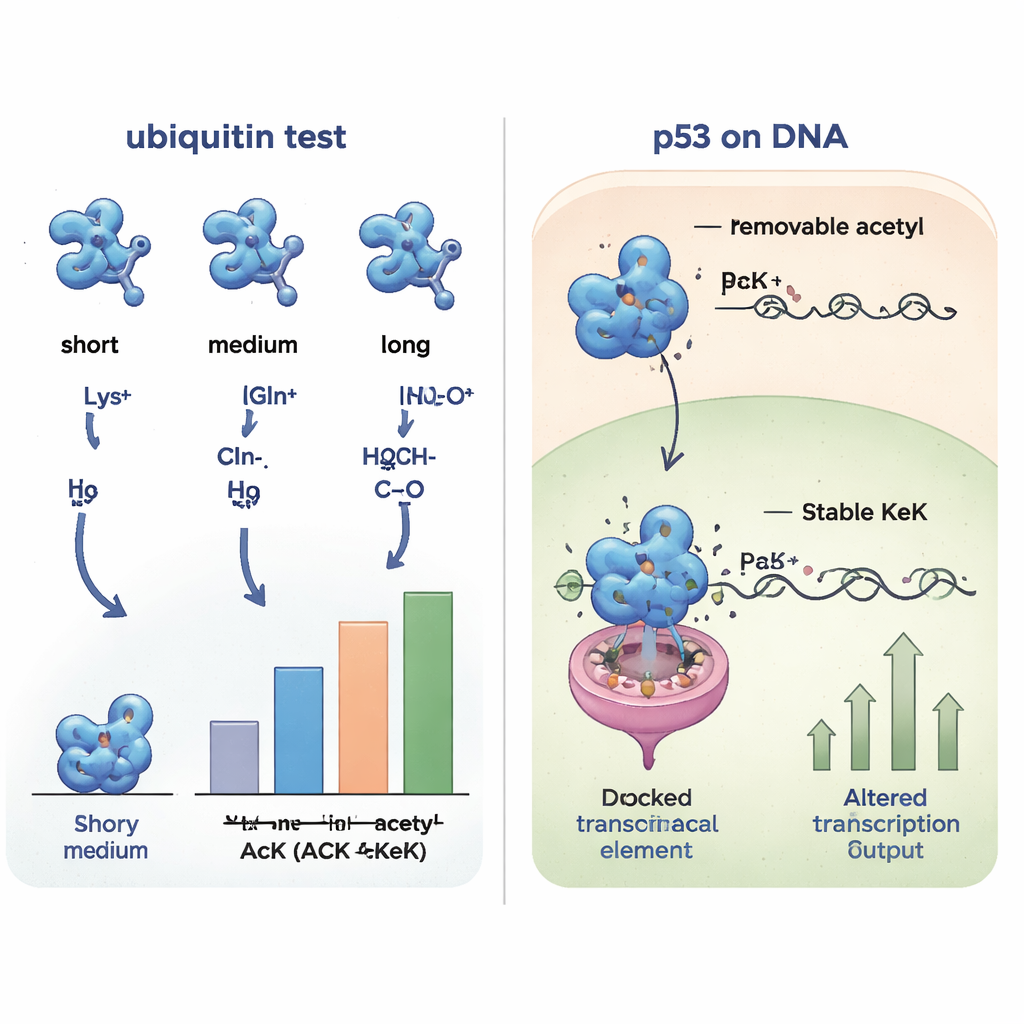
Esplorare le interazioni proteiche nella cellula
Poiché piccoli cambiamenti strutturali possono alterare i partner con cui una proteina interagisce, i ricercatori hanno quindi confrontato come le varie versioni di ubiquitina si legassero ad altre proteine da estratti di cellule umane. Mediante il recupero dei partner di legame e la loro identificazione con spettrometria di massa, hanno osservato che l'ubiquitina contenente acetillisina, TFAcK o KeK mostrava pattern di interazione molto simili, mentre le forme con glutammina o alanina si raggruppavano insieme e apparivano diverse. Le varianti cariche positivamente (lisina o arginina) costituivano un altro gruppo distinto. Questo confronto sistematico ha mostrato che gli analoghi non rimovibili TFAcK e in particolare KeK imitano sia la struttura sia il comportamento di legame della vera acetilazione molto meglio della tradizionale sostituzione con glutammina.
Bloccare l'acetilazione sul soppressore tumorale p53
Per verificare se questi strumenti funzionano all'interno di cellule vive, gli autori si sono concentrati su p53, un importante soppressore tumorale spesso definito il «guardiano del genoma». Specifiche lisine nella regione di legame al DNA di p53 possono essere acetilate, modificando i geni che vengono attivati, come quelli che arrestano il ciclo cellulare o inducono la morte cellulare. Il team ha ingegnerizzato cellule umane affinché p53 incorporasse acetillisina, TFAcK o KeK in due posizioni di lisina importanti (120 e 164) solo quando l'amminoacido non standard corrispondente veniva fornito. Tutti e tre potevano essere inseriti in p53, ma misurazioni dettagliate hanno mostrato che, nelle cellule, i gruppi acetile e TFAcK venivano in gran parte rimossi dalle deacetilasi, mentre KeK rimaneva intatto. Nei test sull'abilità di p53 di attivare un gene reporter e il gene naturale p21, le varianti contenenti KeK in quei siti risultavano molto meno attive, coerentemente con quanto ci si aspetta quando l'acetilazione in quelle posizioni è bloccata, mentre acetillisina e TFAcK si comportavano più simili al p53 normale perché erano state deacetilate.
Cosa significa per lo studio delle decisioni cellulari
Complessivamente, lo studio mostra che KeK è un sostituto fedele e non rimovibile dell'acetillisina: riproduce da vicino i cambiamenti strutturali, le preferenze di legame e le conseguenze funzionali dell'acetilazione, ma non può essere cancellato dagli enzimi cellulari. Per i non specialisti, questo significa che i ricercatori hanno ora un modo per «congelare» un interruttore chimico normalmente reversibile in un singolo sito di una proteina e poi osservare come ciò influisce su processi quali la regolazione genica e le decisioni sul destino cellulare. Questo dovrebbe rendere molto più semplice districare i ruoli specifici dell'acetilazione rispetto ad altre modifiche sovrapposte e potrebbe, in ultima analisi, chiarire come la disregolazione dell'acetilazione proteica contribuisca a malattie come il cancro.
Citazione: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Parole chiave: acetilazione proteica, modificazione post‑traduzionale, ubiquitina, p53, espansione del codice genetico