Clear Sky Science · it
Rimodellamento dinamico del trascrittoma in cellule progenitrici neurali umane trapiantate svela meccanismi per la preservazione della vista in un modello di ratto della retinite pigmentosa
Perché è importante proteggere una vista che svanisce
La retinite pigmentosa è un gruppo di malattie ereditarie che privano progressivamente le persone della vista, spesso iniziando con la cecità notturna e procedendo verso la cecità legale. Poiché centinaia di mutazioni genetiche differenti possono causare questa condizione, trattare ciascuna singolarmente con terapie geniche è complicato. Questo studio esplora un approccio più universale: trapiantare cellule progenitrici neurali umane—cellule nervose immature coltivate in laboratorio—nell’occhio per proteggere le cellule fotosensibili rimaste. Capire esattamente come queste cellule trapiantate si comportano e contribuiscono a preservare la vista potrebbe guidare trattamenti futuri non solo per la retinite pigmentosa ma anche per altri disturbi che causano cecità.
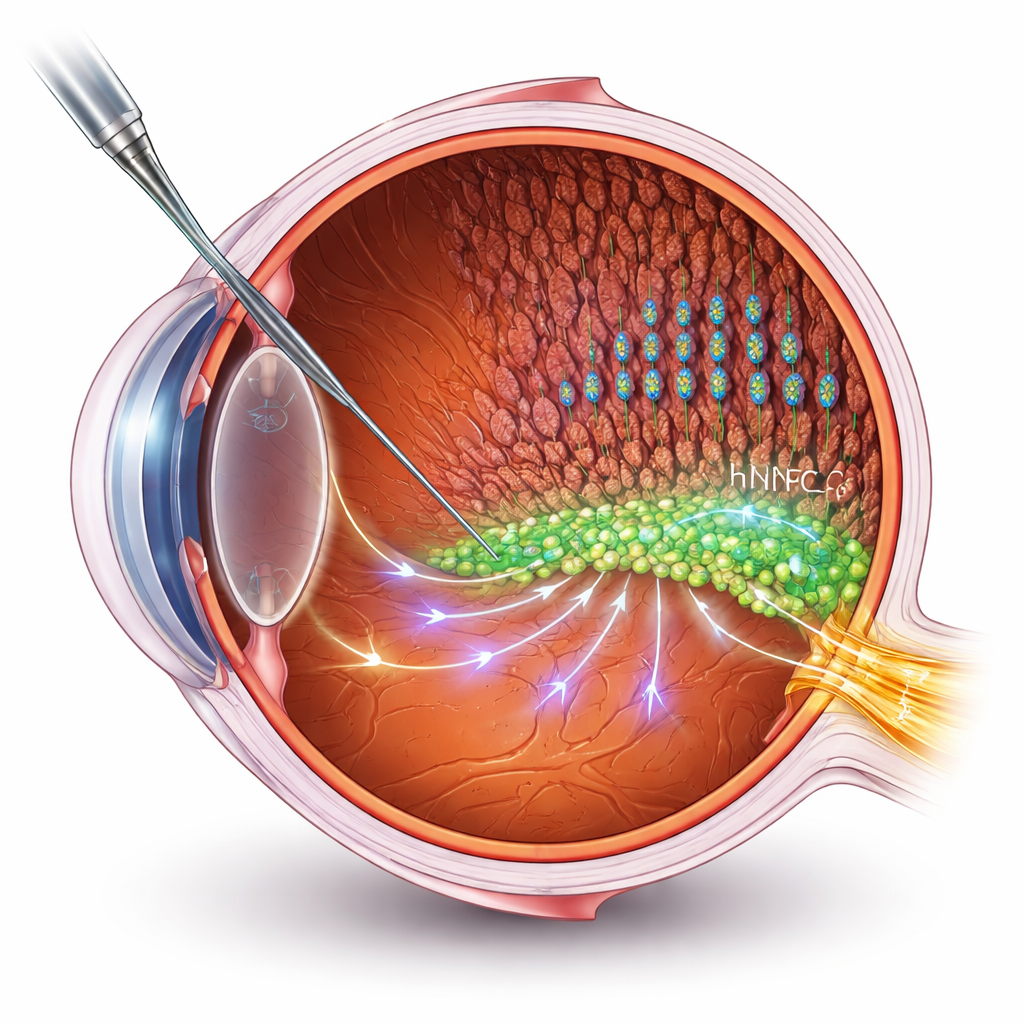
Aiutare le cellule invece di sostituirle
Molte terapie con cellule staminali puntano a sostituire cellule morte o danneggiate. Ma nelle malattie retiniche avanzate, ricostruire nuove connessioni con il cervello è un ostacolo tecnico rilevante. Qui i ricercatori seguono una strada diversa: usare cellule progenitrici neurali umane (hNPC) come “aiutanti” che supportano le cellule retiniche del paziente. Hanno trapiantato hNPC nello spazio sottomaculare di un noto modello di ratto della retinite pigmentosa, quindi hanno misurato la vista mediante registrazioni elettriche e test comportamentali. I ratti trattati hanno mantenuto una funzione visiva migliore e strati di fotorecettori—i bastoncelli e i coni che captano la luce—più intatti rispetto agli animali non trattati, anche se la degenerazione è comunque progredita lentamente.
Come cambiano le cellule trapiantate nell’occhio malato
Per osservare cosa accade a livello molecolare, il gruppo ha usato il sequenziamento dell’RNA a singola cellula, una tecnica che profila quali geni sono attivi in migliaia di singole cellule. Hanno seguito le hNPC trapiantate in due momenti temporali, corrispondenti più o meno a stadi iniziali e successivi dopo il trapianto. Piuttosto che trasformarsi in nuovi fotorecettori, la maggior parte delle cellule trapiantate si è differenziata in cellule di supporto simili agli astrociti, con una frazione minore che esprimeva marcatori di oligodendrociti o di neuroni immaturi. Col tempo queste cellule si sono stabilizzate, assumendo caratteristiche che suggeriscono una maggiore adattamento per sopravvivere in un ambiente stressante e degenerativo e per interagire strettamente con le cellule retiniche vicine.
Segnali protettivi, metabolismo e pulizia
Le hNPC hanno prodotto un ricco assortimento di proteine protettive note come fattori trofici. Tra queste figuravano MANF e MYDGF, collegate alla sopravvivenza cellulare, alla riduzione dello stress ossidativo e all’attenuazione dell’infiammazione, oltre ad altri fattori come midkine e pleiotrofina che supportano la crescita e il movimento delle cellule neurali. Queste molecole sembravano agire sia sul trapianto stesso sia sulla retina circostante. Nei ratti trattati, bastoncelli e coni mostravano profili di espressione genica più vicini ai controlli sani, con un migliore supporto per la segnalazione visiva e la manutenzione cellulare. Le cellule trapiantate hanno anche potenziato le vie coinvolte nella rimozione dei detriti cellulari e nell’adattamento metabolico, suggerendo che aiutano i fotorecettori a far fronte alle esigenze energetiche e ai prodotti tossici che si accumulano durante la malattia.
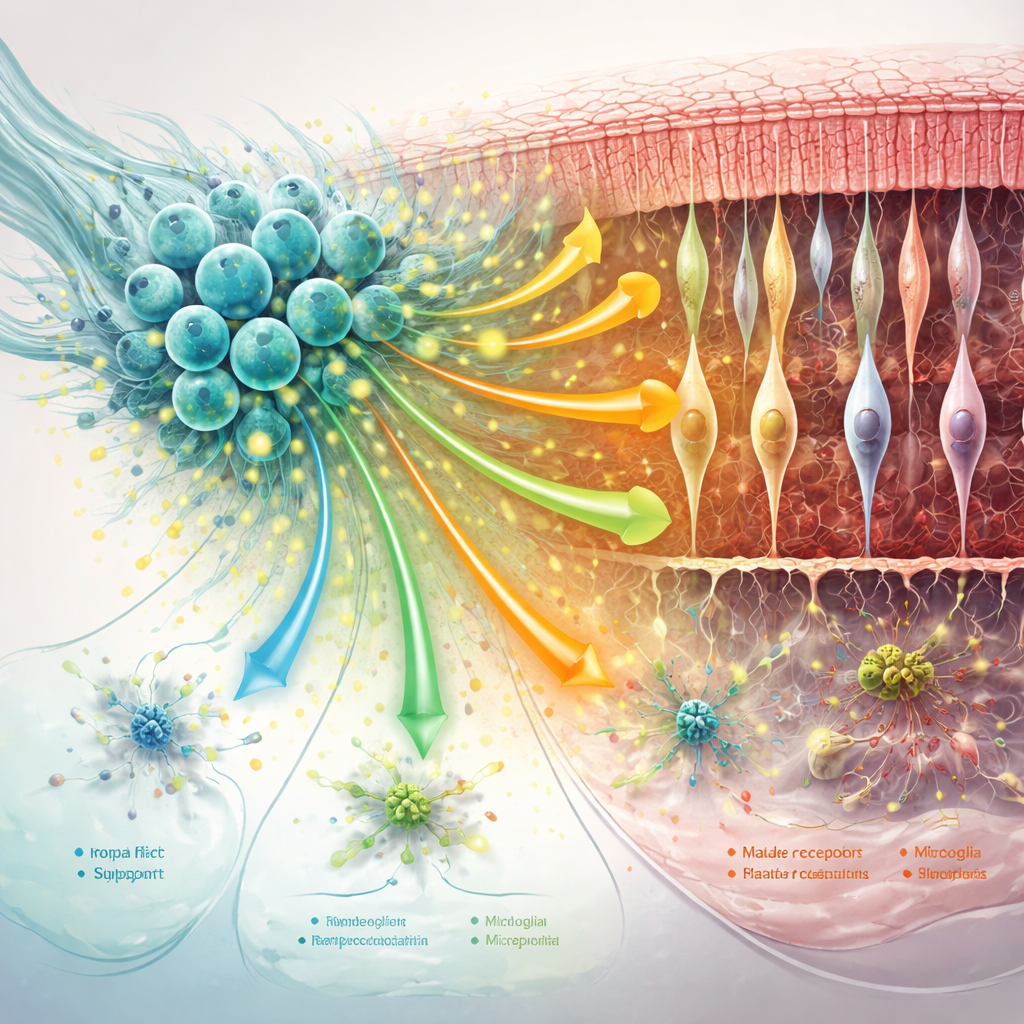
Calmare le cellule di supporto e rimodellare il vicinato retinico
La rete di supporto della retina—gli gliociti di Müller, le microglia e la matrice proteica circostante—gioca un ruolo importante sia nel peggiorare sia nel rallentare la degenerazione. Lo studio ha rilevato che il trattamento con hNPC ha attenuato marcatori chiave dei cambiamenti “reattivi” dannosi nelle cellule di Müller e ha spostato le microglia lontano da stati eccessivamente infiammatori, soprattutto nei primi tempi. Allo stesso tempo, i segnali di comunicazione che aiutano a stabilizzare le sinapsi, far aderire le cellule tra loro e mantenere l’impalcatura intorno ai fotorecettori sono stati rafforzati. Con l’avanzare della malattia, alcuni di questi benefici sono diminuiti: la comunicazione cellula‑cellula nel complesso si è indebolita, alcune vie protettive—compresa la segnalazione correlata a MANF—sono calate e le cellule di supporto hanno assunto profili più orientati allo stress e alla risposta immunitaria.
Cosa significa per le future terapie oculari
Per chi non è specialista, il messaggio principale è che le cellule progenitrici neurali umane trapiantate possono comportarsi come “primi soccorritori” in loco in una retina in degenerazione. Non ricostruiscono la retina da zero, ma rilasciano molecole protettive, modulano il metabolismo, attenuano l’infiammazione dannosa e aiutano a mantenere l’integrità strutturale locale, tutte azioni che rallentano la perdita della vista. Tuttavia, questo effetto protettivo diminuisce col tempo man mano che l’ambiente diventa più ostile e il dialogo tra cellule trapiantate e ospiti si indebolisce. Gli autori suggeriscono che potenziare fattori chiave come MANF e migliorare la salute della retina ospite—possibilmente tramite l’ingegneria genetica del trapianto o trattamenti combinati—potrebbe essere essenziale per trasformare una temporanea tregua in una preservazione della vista di lunga durata.
Citazione: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Parole chiave: retinite pigmentosa, terapia con cellule staminali, degenerazione retinica, neuroprotezione, sequenziamento dell’RNA a singola cellula