Clear Sky Science · it
TCL1A media i difetti di metilazione del DNA nella mola idatiforme ricorrente con varianti patogene di NLRP7
Perché è importante per la salute delle donne
Alcune gravidanze si interrompono molto presto, trasformandosi in una massa di tessuto placentare anomalo invece che in un feto in sviluppo. Questa condizione, chiamata mola idatiforme, può ripetersi in alcune donne e talvolta evolvere in cancro. Questo studio indaga una delle cause genetiche principali di queste rare ma gravi gravidanze e rivela come una singola salvaguardia difettosa nell’oocita possa compromettere le “etichette” chimiche che guidano lo sviluppo sano.
Un problema della gravidanza che ha radici nell’oocita
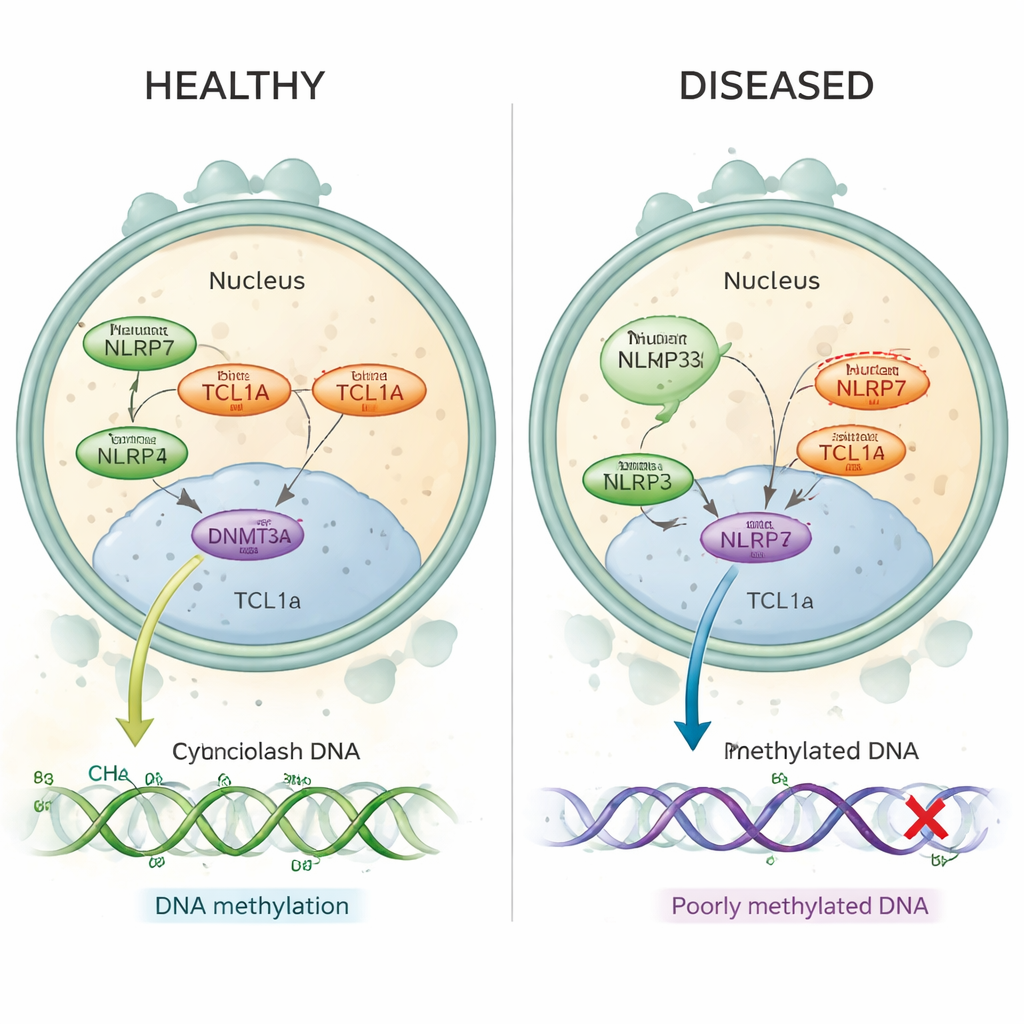
La mola idatiforme ricorrente è un disturbo in cui le donne sperimentano ripetute gravidanze molari, spesso senza gravidanze normali in mezzo. Molti di questi casi sono ora noti per essere causati da alterazioni dannose in un gene chiamato NLRP7, attivo nell’oocita prima e subito dopo la fecondazione. In queste donne, tratti chiave del DNA che dovrebbero portare gli “imprinting” materni mancano delle normali marche di metilazione—piccoli segni chimici che aiutano ad attivare o spegnere i geni al momento giusto. Fino a oggi, gli scienziati non avevano compreso come una proteina situata nel citoplasma dell’oocita, come NLRP7, potesse controllare la metilazione che avviene sul DNA racchiuso nel nucleo.
Trovare un partner mancante
Per risolvere questo enigma, i ricercatori hanno esaminato oociti umani scartati e embrioni molto precoci provenienti da cliniche di fertilità. Hanno isolato NLRP7 e i suoi partner noti da queste cellule e identificato altre proteine che vi si associano. Una in particolare ha attirato l’attenzione: TCL1A, già noto nei tumori del sangue come proteina in grado di entrare nel nucleo e interferire con enzimi metilanti del DNA chiamati DNMT3A e DNMT3B. TCL1A è insolitamente abbondante negli oociti umani, il che suggerisce che vi svolga un ruolo importante. Test dettagliati di interazione hanno mostrato che TCL1A si lega strettamente e specificamente a NLRP7, ma non a proteine strettamente correlate, e che questo complesso è integrato in una struttura più ampia specifica dell’oocita chiamata complesso materno subcorticale.
Osservare l’abbraccio molecolare
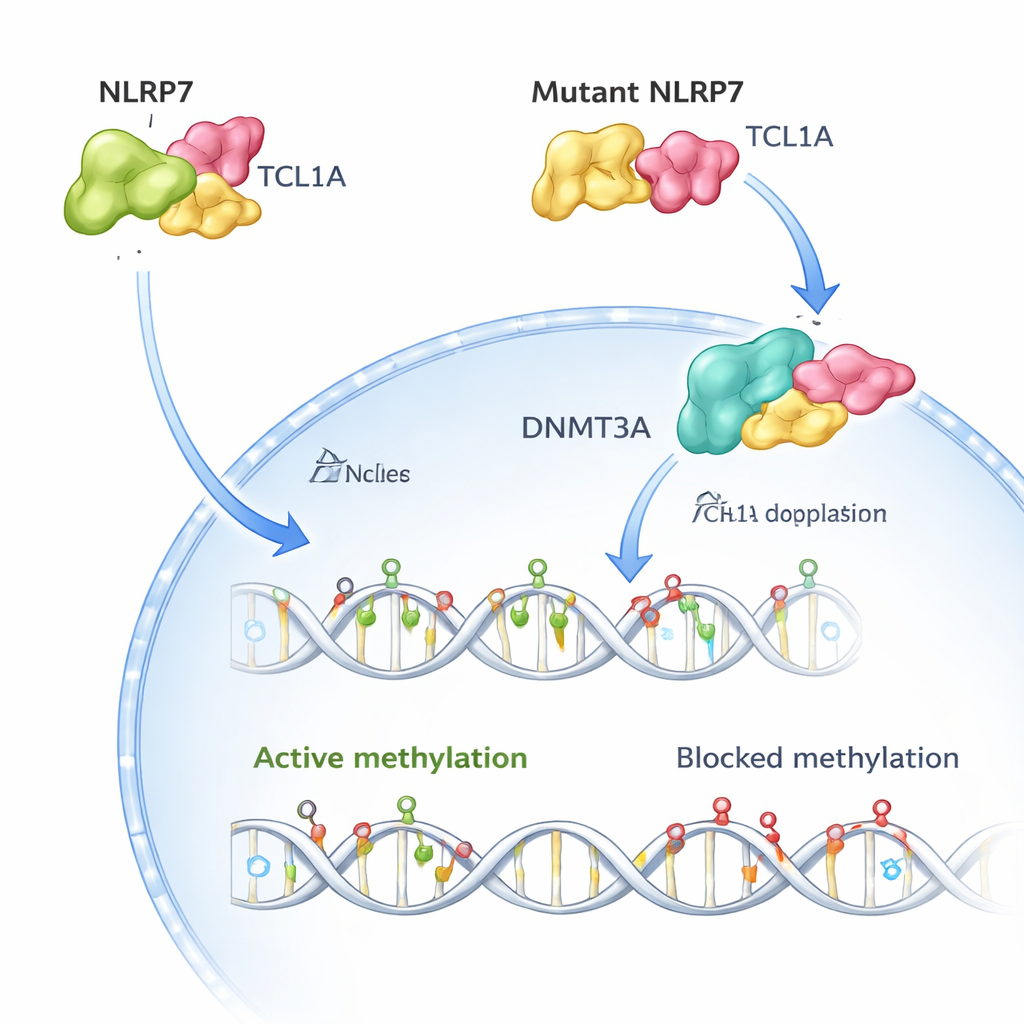
Il gruppo ha quindi usato la criomicroscopia elettronica per visualizzare la struttura tridimensionale del complesso NLRP7–TCL1A. Hanno scoperto che due molecole di NLRP7 si accoppiano e ciascuna afferra un dimero di TCL1A lungo una superficie curva costituita da motivi ripetuti. Questa disposizione spiega perché molte varianti che causano la malattia si concentrano lungo quella superficie: alterare punti chiave di contatto indebolisce o distrugge l’abbraccio con TCL1A. Quando i ricercatori hanno ricreato in cellule oltre 50 varianti note di pazienti, la maggior parte delle versioni associate a gravidanze molari ricorrenti o destabilizzava NLRP7 o riduceva drasticamente la sua capacità di legare TCL1A.
Come le proteine mal posizionate disturbano le marcature del DNA
Negli oociti umani sani, sia NLRP7 sia TCL1A si trovano principalmente nel citoplasma, con solo una piccola quantità di TCL1A che raggiunge il nucleo. Gli autori mostrano che NLRP7 agisce efficacemente come una guardia: quando può trattenere TCL1A, quest’ultima resta fuori dal nucleo. Quando NLRP7 è mutato e non riesce più a legarsi adeguatamente, TCL1A fuoriesce nel nucleo. Lì si attacca a DNMT3A, l’enzima principale che deposita nuove marche di metilazione negli oociti, e ne attenua l’attività. In modelli di cellule staminali che normalmente acquisiscono metilazione durante la maturazione, la sovraespressione di TCL1A ha provocato una drastica perdita di metilazione in tutto il genoma, mentre la co‑espressione di NLRP7 ha parzialmente corretto questo difetto. Insieme, questi risultati supportano un quadro semplice: NLRP7 normale mantiene bloccato nel citoplasma un “freno” della metilazione (TCL1A) così che DNMT3A possa correttamente marcare il DNA; NLRP7 difettoso permette a quel freno di entrare nel nucleo e bloccare il processo.
Dal meccanismo alla diagnosi
Oltre a spiegare come nascono le gravidanze molari ricorrenti, lo studio suggerisce un modo pratico per valutare se una nuova variante di NLRP7 scoperta in una paziente sia realmente dannosa. Gli autori confrontano tre approcci—test di laboratorio del legame NLRP7–TCL1A, previsioni basate su computer e strumenti standard di classificazione genetica—and mostrano che la perdita del legame con TCL1A si allinea strettamente con le varianti che causano la malattia. Scoprono inoltre una variante patogena precedentemente non riconosciuta, L766R, in famiglie con moli ricorrenti, confermando che essa sia in grado sia di indebolire la proteina sia di deviare TCL1A nel nucleo.
Cosa significa in termini semplici
Questo lavoro rivela una catena di eventi molecolari dietro un raro ma devastante disturbo della gravidanza. In sostanza, gli oociti delle donne colpite portano una proteina “guardia del corpo” rotta, NLRP7, che non riesce a tenere il suo partner TCL1A fuori dal nucleo. Una volta all’interno, TCL1A interferisce con l’enzima che scrive le etichette chimiche vitali sul DNA. Senza quelle etichette, la placenta precoce cresce in modo anomalo e un embrione non può formarsi. Tracciando questo percorso passo dopo passo, lo studio chiarisce perché certi cambiamenti genetici nelle madri possono sabotare ripetutamente le gravidanze e apre la strada a una consulenza genetica e a una diagnosi più precise per le donne con moli idatiformi ricorrenti.
Citazione: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Parole chiave: metilazione del DNA, mola idatiforme ricorrente, NLRP7, TCL1A, imprinting genomico