Clear Sky Science · it
GCN5 guida la progressione della MASLD attraverso la via di segnalazione LXRα/SREBP1c-mediata della lipogenesi de novo
Perché questa storia sul fegato è importante
La steatosi epatica associata a disfunzione metabolica (MASLD), precedentemente chiamata malattia del fegato grasso non alcolica, oggi colpisce circa una persona su quattro nel mondo. Spesso si sviluppa in modo silente, ma può progredire fino a indurre fibrosi, carcinoma epatico e gravi problemi metabolici. Questo studio individua una sorta di “manopola” molecolare che promuove l’accumulo dannoso di grasso nel fegato e mostra come diminuirne l’attività potrebbe proteggere l’organo e, potenzialmente, rendere più sicure strategie farmacologiche già studiate per il cuore.
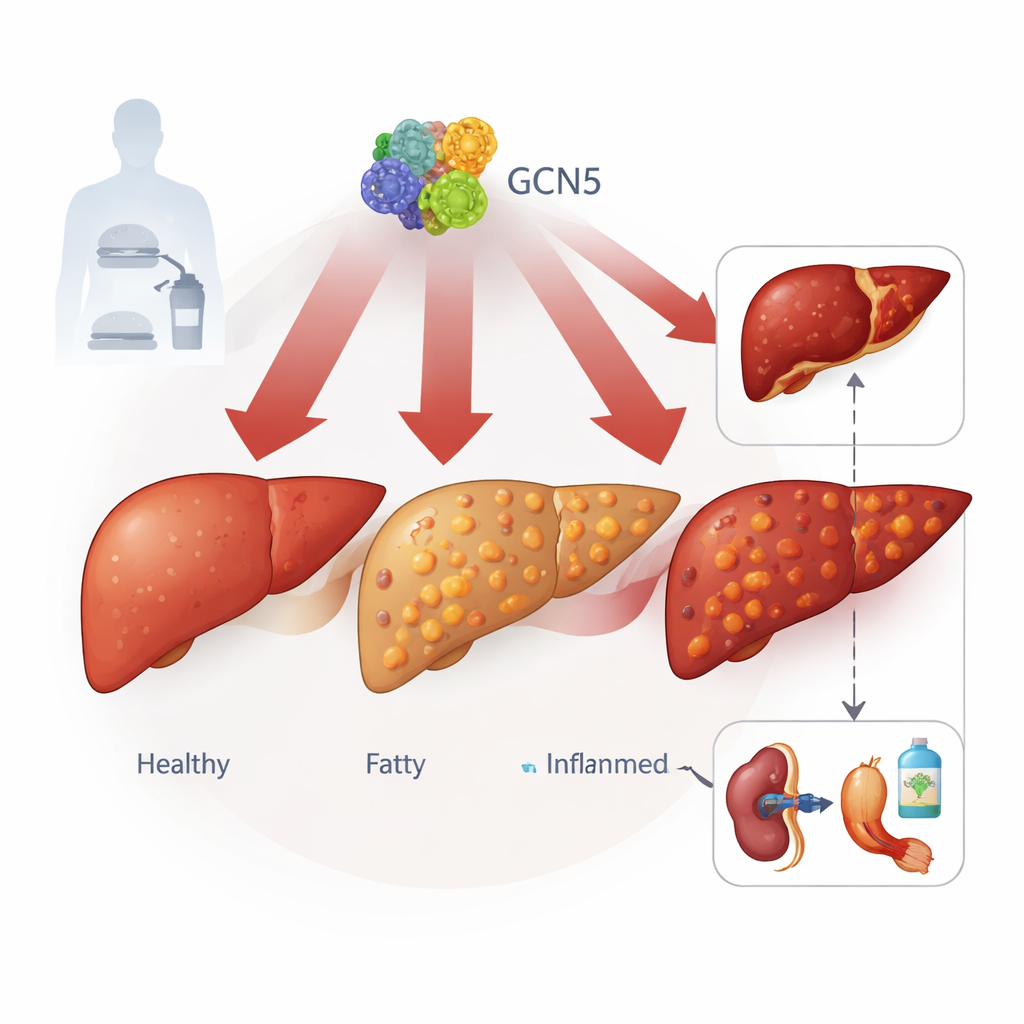
Un interruttore nascosto nelle cellule epatiche
Gli autori si concentrano su una proteina chiamata GCN5, nota soprattutto come regolatore del grado di compattamento del DNA. Studiando tessuto epatico proveniente da oltre 100 persone, dallo stato sano a forme gravi di MASLD, e vari modelli murini di fegato grasso indotto dalla dieta, hanno osservato che i livelli di GCN5 nelle cellule epatiche aumentano costantemente con il peggiorare della malattia. Una proteina strettamente correlata, PCAF, non mostrava lo stesso andamento, suggerendo che GCN5 abbia un ruolo specifico. L’elevata espressione di GCN5 correlava con maggiore steatosi epatica, livelli ematici di lipidi più alti e segni più marcati di danno epatico, collegando questo interruttore molecolare alla gravità clinica reale.
Regolare GCN5 verso l’alto o verso il basso negli animali
Per testare causa ed effetto, il team ha aumentato geneticamente o eliminato GCN5 specificamente nelle cellule epatiche dei topi. Quando GCN5 veniva sovraespresso, i topi sottoposti a una dieta ricca di grassi sviluppavano fegati più grandi e più grassi, livelli plasmatici di lipidi aumentati e maggior danno cellulare epatico, nonostante non consumassero più cibo né aumentassero di peso corporeo. Anche cellule epatiche coltivate in vitro mostravano un comportamento analogo: un eccesso di GCN5 portava a goccioline lipidiche più grandi e più numerose. Al contrario, i topi ingegnerizzati per essere privi di GCN5 solo nelle cellule del fegato risultavano fortemente protetti. In diversi modelli dietetici che imitano la MASLD umana e la sua forma infiammatoria più severa, questi animali accumulavano meno grasso epatico, mostravano livelli più bassi di lipidi e enzimi epatici nel sangue e sviluppavano meno infiammazione e fibrosi.
Come GCN5 spinge il fegato a produrre grasso
Approfondendo il metabolismo, i ricercatori hanno misurato numerosi acidi grassi e i loro precursori nel fegato. La perdita di GCN5 riduceva principalmente i lipidi sintetizzati dal fegato stesso, un processo noto come lipogenesi de novo, mentre lasciava relativamente invariati i grassi polinsaturi derivati dalla dieta. Esperimenti di espressione genica e di tracciamento isotopico hanno mostrato che GCN5 agisce a monte di un regolatore maestro della sintesi lipidica chiamato SREBP1c. Con GCN5 attivo, i geni che costruiscono e modificano gli acidi grassi venivano attivati e il tasso interno di produzione di lipidi del fegato aumentava. Rimuovere o bloccare GCN5 attenuava questo programma, riducendo il flusso di carbonio dallo zucchero verso i nuovi lipidi epatici.
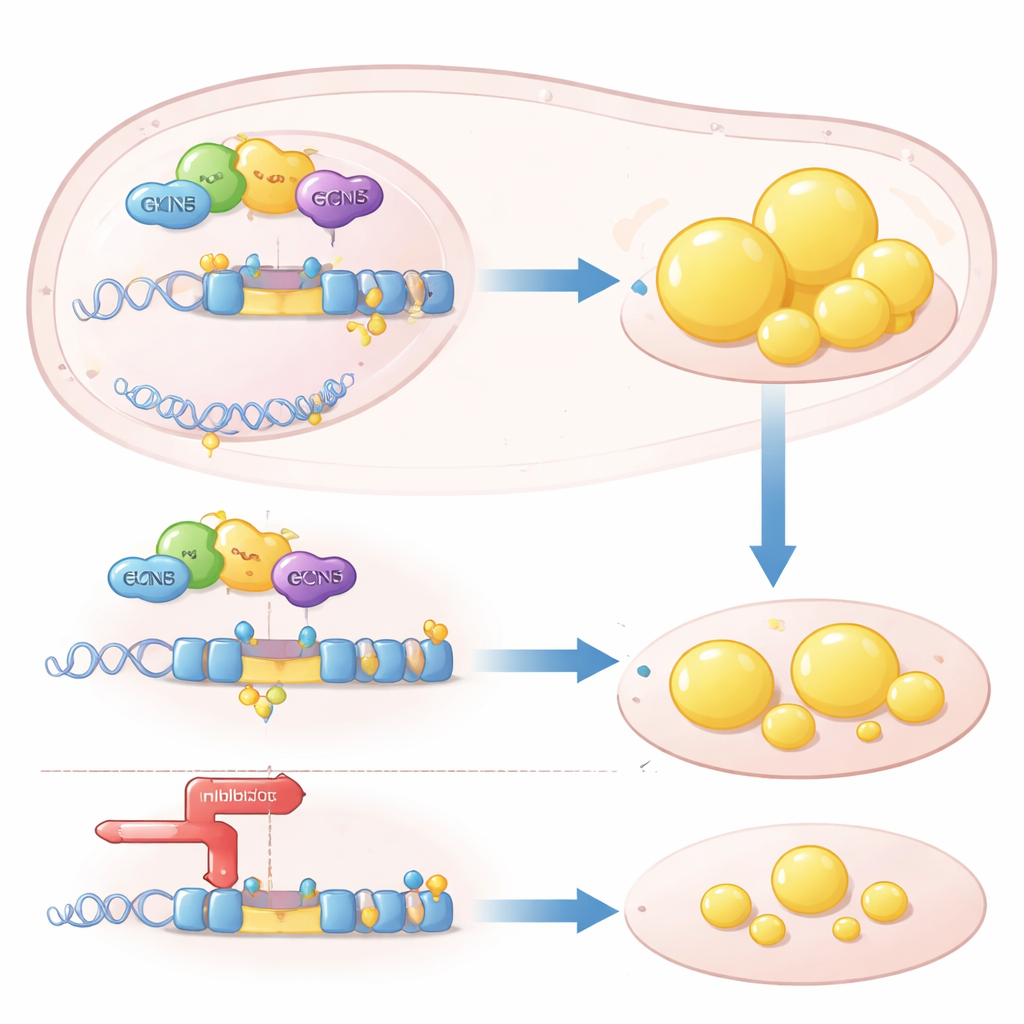
Una leva epigenetica su un gene chiave dei lipidi
Dal punto di vista meccanico, GCN5 agisce come una leva «epigenetica»: modifica chimicamente le proteine istoniche legate al DNA per rendere più accessibili alla trascrizione alcuni geni. Gli autori hanno mostrato che GCN5 viene reclutato nella regione di controllo del gene SREBP1c insieme a un recettore nucleare chiamato LXRα, che rileva molecole correlate al colesterolo. Una volta lì, GCN5 aggiunge marcature di acetilazione sull’istone H3, allentando la cromatina locale e potenziando la trascrizione di SREBP1c. Questo effetto era molto selettivo: GCN5 migliorava la capacità di LXRα di attivare SREBP1c ma non un altro bersaglio di LXR, ABCA1, che favorisce l’eliminazione del colesterolo dai tessuti. In assenza di GCN5, LXRα non riusciva più a interagire efficacemente con il promotore di SREBP1c e il programma sintomatico di sintesi lipidica si arrestava.
Un candidato farmacologico e una combinazione promettente
Il gruppo ha quindi testato CPTH2, un inibitore a piccola molecola di GCN5 che si concentra nel fegato. In modelli murini già sottoposti a diete grasse, CPTH2 ha ridotto le dimensioni del fegato, il contenuto lipidico e i marker di danno senza tossicità evidente o cambiamenti nell’assunzione di cibo. In cellule epatiche umane e murine in coltura, CPTH2 abbassava le goccioline lipidiche e i trigliceridi solo quando GCN5 era presente, confermando la specificità della sua azione. Importante, sia nelle cellule sia nei topi trattati con composti attivanti LXR (ideati per migliorare la rimozione del colesterolo e combattere l’aterosclerosi), CPTH2 bloccava selettivamente l’aumento indesiderato della sintesi lipidica guidata da SREBP1c preservando invece i geni che promuovono il trasporto inverso del colesterolo. In combinazione con un agonista LXR in topi nutriti con dieta ricca di grassi, CPTH2 riduceva ulteriormente i lipidi ematici dannosi e il colesterolo epatico e preveniva l’accumulo extra di grasso nel fegato.
Cosa significa questo per i pazienti
Lo studio colloca GCN5 come un driver centrale dell’accumulo di grasso epatico nella MASLD collegando segnali dietetici e ormonali all’interruttore di produzione lipidica SREBP1c. Poiché GCN5 sembra non essere necessario per il braccio benefico della segnalazione LXR che elimina il colesterolo, farmaci inibitori di GCN5 — come CPTH2 o successori più avanzati — potrebbero ridurre la steatosi e l’infiammazione epatica permettendo al contempo alle terapie cardioprotettive di funzionare. Per le persone a rischio sia di malattia epatica grassa sia di malattie cardiovascolari, mirare a questo interruttore epigenetico potrebbe un giorno offrire un modo per proteggere il fegato senza sacrificare i benefici del miglioramento del metabolismo del colesterolo.
Citazione: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Parole chiave: steatosi epatica, epigenetica, metabolismo dei lipidi, metabolismo epatico, recettori nucleari