Clear Sky Science · it
Controllo non‑chelante nelle allylazioni di chetoni α‑ossi usando allylatrani del gruppo 14
Costruire forme molecolari con maggiore precisione
Molti farmaci e prodotti naturali funzionano solo quando i loro atomi sono disposti in una precisa configurazione tridimensionale. I chimici pertanto dedicano grandi sforzi a imparare come "spingere" nuovi gruppi su una molecola da un lato o dall'altro. Questo articolo descrive un nuovo modo di introdurre gruppi allyl—brevi catene a tre atomi di carbonio—su una classe comune di molecole, consentendo l'accesso a strutture immagine‑speculari che finora erano molto difficili da ottenere.
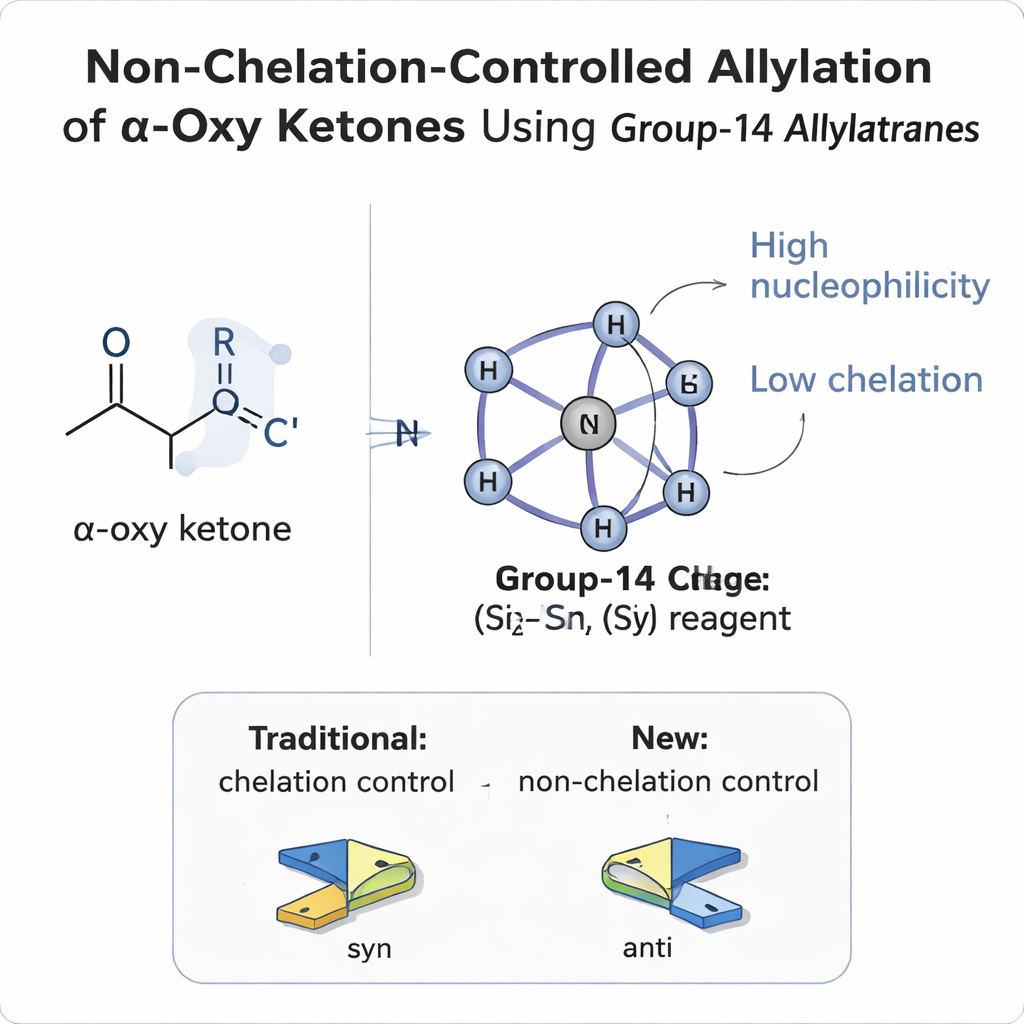
Perché controllare i lati di una molecola è così difficile
Quando un nuovo gruppo viene aggiunto a un doppio legame carbonio‑ossigeno planare (un carbonile), può attaccare da entrambe le facce, come una palla che colpisce una moneta dall'alto o dal basso. Se è presente già un sostituente al carbonio adiacente (la posizione α), il risultato sono due possibili prodotti tridimensionali, detti diastereomeri. Per decenni i chimici si sono affidati a modelli semplici—Felkin–Anh, Felkin–Anh polare, Cram e modelli di chelazione—per prevedere quale faccia preferirà il reagente. Nei composti carbonilici α‑ossi, dove il sostituente vicino contiene ossigeno (come un etere o un estere), l'ossigeno tende ad agire come una pinza che si lega ai reagenti metallici. Questa "chelazione" immobilizza la molecola in una conformazione e quasi sempre porta a prodotti cosiddetti syn, in cui i gruppi alcolici appena formati finiscono dallo stesso lato della catena carboniosa.
Il problema di lunga data dei vicini ossigeno
Sebbene la via della chelazione sia molto utile, è anche limitante: tende fortemente a favorire prodotti syn e rende molto difficile ottenere l'arrangiamento opposto, anti, in cui i due gruppi alcolici sono orientati su lati opposti. Per gli aldeidi α‑ossi—molecole in cui il carbonio carbonilico è legato ad almeno un idrogeno—alcuni trucchi ingegnosi che impiegano reagenti speciali a base di silicio e acidi di Lewis scelti con cura sono riusciti a fornire prodotti anti. Ma per i chetoni α‑ossi, che sono meno reattivi e più comuni in obiettivi complessi, la sfida è maggiore. I nucleofili più forti tendono a essere più acidi di Lewis, il che a sua volta incoraggia proprio la chelazione che il chimico vuole evitare. Quindi, bilanciare "abbastanza reattivo" con "non troppo propenso a legare l'ossigeno" è stato un problema centrale irrisolto.
Un reagente a gabbia che rompe la regola
Gli autori introducono una nuova famiglia di reagenti chiamati allylatrani, costruiti attorno a elementi del gruppo 14—silicio, germanio e stagno—tenuti in un telaio rigido a forma di gabbia. In queste molecole, un atomo di azoto interno raggiunge attraverso la gabbia per legarsi all'atomo centrale, creando un centro fortemente coordinato e quasi incapsulato. Questo design ha due effetti cruciali. Primo, aumenta la nucleofilicità del frammento allyl legato, rendendolo incline a formare un nuovo legame carbonio‑carbonio. Secondo, tempera l'acidità di Lewis dell'atomo centrale, rendendolo molto meno propenso a legarsi fortemente agli atomi di ossigeno del substrato. Calcoli quantochimici e dati di risonanza magnetica nucleare confermano che la carica è localizzata sul frammento allyl mentre la comunicazione elettronica con il centro di silicio è ridotta, spiegando come il reagente possa essere potente e al contempo riluttante alla chelazione.
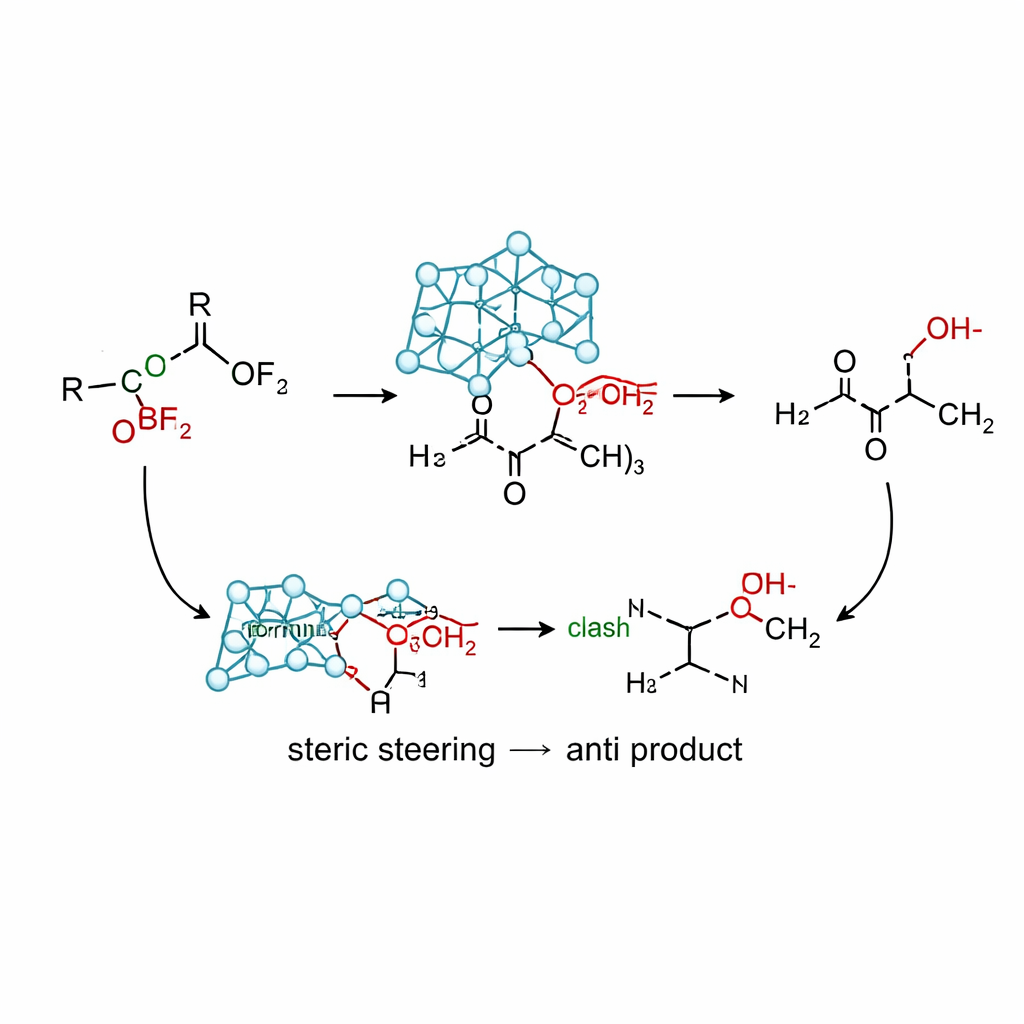
Come funziona la nuova reazione nella pratica
Utilizzando la versione a base di silicio di questo reagente, l'allylsilatrano, insieme a un acido di Lewis delicato (trifluoruro di boro), il gruppo ha sviluppato condizioni che forniscono elevati rendimenti di alcoli anti‑omoallylici da un'ampia gamma di chetoni α‑ossi. Esperimenti di confronto mostrano che molte fonti tradizionali di allyl—basate su stagno, indio, magnesio, litio e silani semplici—o favoriscono il prodotto syn, danno miscele o si decompongono. Al contrario, l'allylsilatrano fornisce sistematicamente rapporti anti/syn superiori a 95:5 su substrati con gruppi metossilici, isoprossilici, fenossilici, acetossilici, silyloxilici e aminossilici, così come vari anelli aromatici e chetoni ciclici. I calcoli suggeriscono una via non‑chelante in cui l'ingombrante impalcatura atrane indirizza l'approccio del gruppo allyl in una conformazione che ricorda il modello di Cram: il sostituente ossigeno si trova opposto al carbonile mentre la repulsione sterica tra la gabbia e gli anelli fenilici vicini favorisce la traiettoria che porta al prodotto anti.
Implicazioni per la sintesi di farmaci e prodotti naturali
Il metodo funziona anche per sistemi ciclici più rigidi, dove l'ingombro dell'allylsilatrano incoraggia l'attacco da posizioni meno ostacolate, e per derivati specializzati che trasferiscono gruppi allyl sostituiti con analoghi elevati livelli di selettività anti. Poiché i risultanti anti‑1,2‑dioli con un frammento homoallylic sono motivi comuni in molecole biologicamente attive, inclusi candidati per modulare enzimi, questa trasformazione offre ai chimici un modo affidabile per accedere a varianti strutturali che prima richiedevano soluzioni multistep o erano semplicemente impraticabili. È importante che gli stessi substrati possano essere diretti a dare prodotti syn o anti cambiando tra un sistema chelante a base di stagno e il nuovo sistema non‑chelante a base di silatrano, permettendo un controllo preciso sulla forma molecolare.
Che cosa significa in termini semplici
In sostanza, i ricercatori hanno costruito uno strumento intelligente per fornire il gruppo allyl che colpisce il carbonio bersaglio dal lato "sfavorito" senza rimanere intrappolato dagli ossigeni vicini. Ingegnerizzando con cura una gabbia attorno al silicio, hanno disaccoppiato forza e aderenza: il reagente è abbastanza forte da formare un nuovo legame ma non così appiccicoso da aggrapparsi agli atomi circostanti e compromettere la geometria desiderata. Per i non specialisti, questo significa che i chimici hanno ora un controllo molto migliore sulla scultura di strutture molecolari tridimensionali che sono alla base di molti farmaci e prodotti naturali, ampliando lo spazio di progettazione per future medicine e molecole complesse.
Citazione: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Parole chiave: allylazione stereoselettiva, chetoni alfa‑ossi, allylsilatrano, controllo non‑chelante, alcoli omoallylici