Clear Sky Science · it
La regione N-Myc MB0–MBI interagisce in modo specifico e dinamico con il N-lobo della chinasi Aurora A
Perché questo è importante per la terapia del cancro
Molti tumori pediatrici aggressivi dipendono da una proteina chiamata N-Myc per mantenere la crescita delle cellule tumorali. N-Myc è di per sé difficile da bloccare con farmaci perché si comporta più come un filo flessibile che come una serratura rigida in cui una chiave può inserirsi. Questo studio rivela, con dettaglio senza precedenti, come N-Myc si leghi a un’altra proteina, l’enzima Aurora chinasi A (AurA), per aumentare la sua attività e aiutare le cellule tumorali a sopravvivere. Mappando questa collaborazione, i ricercatori individuano un modo realistico per interromperla con piccole molecole.
Un disordinato flessibile trova un partner solido
N-Myc appartiene alla famiglia MYC, master switch che controllano crescita cellulare, metabolismo e divisione. Quando sovraespresso, questi switch diventano potenti driver tumorali, specialmente nei tumori del sistema nervoso come il neuroblastoma ad alto rischio nei bambini. A differenza di molti enzimi o recettori, N-Myc non si piega in una forma tridimensionale fissa da solo; è una proteina “intrinsecamente disordinata” che continuamente si muove e si rimodella. Questa flessibilità la rende adattabile ma anche notoriamente difficile da colpire con farmaci. AurA, al contrario, è un enzima ben strutturato che aiuta a organizzare la divisione cellulare. Studi precedenti hanno mostrato che AurA contribuisce a stabilizzare N-Myc nelle cellule tumorali e che le due proteine interagiscono fisicamente, ma la natura esatta e l’importanza dei punti di contatto non erano chiare.
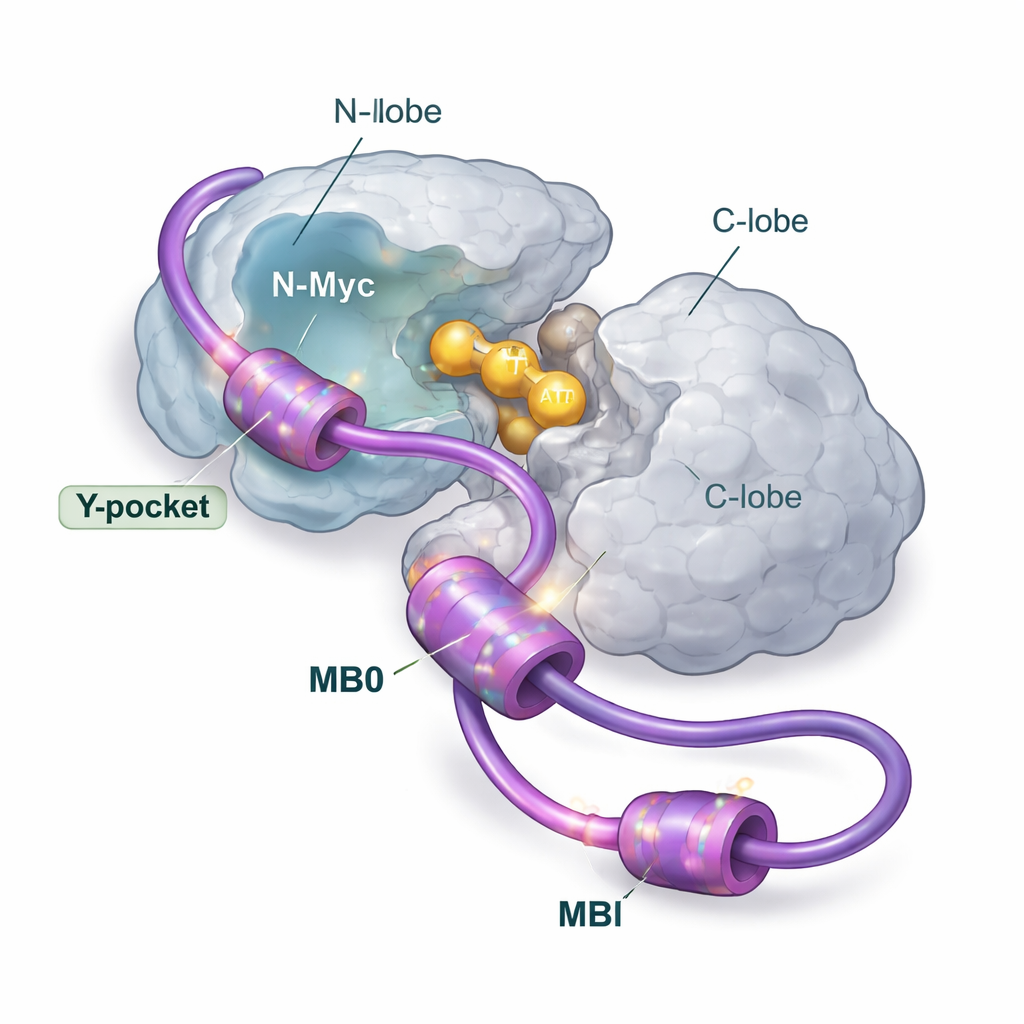
Molteplici punti di presa, un unico punto d’atterraggio principale
Usando un ampio kit di strumenti strutturali e biofisici, incluse risonanza magnetica nucleare, scattering di raggi X, spettrometria di massa, calorimetria e modellizzazione al calcolatore, gli autori hanno dissezionato come N-Myc e AurA si associano in soluzione. Si sono concentrati sull’estremità anteriore di N-Myc, che contiene due regioni conservate chiamate MB0 e MBI. Questi brevi segmenti sono ricchi di residui aromatici (come fenilalanina, tirosina e triptofano) che tendono ad aderire a tasche idrofobiche sulle proteine partner. Il gruppo mostra che N-Myc si lega ad AurA principalmente in rapporto 1:1, con MB0 e MBI che fungono da zone di contatto primarie. Un altro tratto di N-Myc che aveva attirato l’attenzione in precedenti strutture cristalline risulta avere un ruolo solo marginale quando è presente l’intera regione MB0–MBI.
Una stretta di mano dinamica che attiva l’enzima
Invece di assestarsi in una singola posa bloccata, N-Myc resta per lo più disordinato anche quando è legato ad AurA. I dati indicano un complesso “fumoso”: diversi segmenti di N-Myc si alternano nel contattare zone differenti del N-lobo di AurA, in particolare una scanalatura nota come Y-pocket e un anello vicino che collega i segnali al sito attivo. Malgrado questa scioltezza, l’effetto è chiaro: il legame di MB0 e MBI stabilizza il N-lobo di AurA e ne aumenta l’attività chinasica, cioè la sua capacità di trasferire gruppi fosfato ai bersagli. Quando i ricercatori hanno sostituito sistematicamente residui aromatici chiave in MB0 e MBI con alanina, il complesso N-Myc–AurA si è indebolito, l’enzima è stato meno stabilizzato e la sua attività è calata. Ciò dimostra che ancore aromatiche specifiche nella catena altrimenti floscia di N-Myc sono essenziali per attivare AurA.
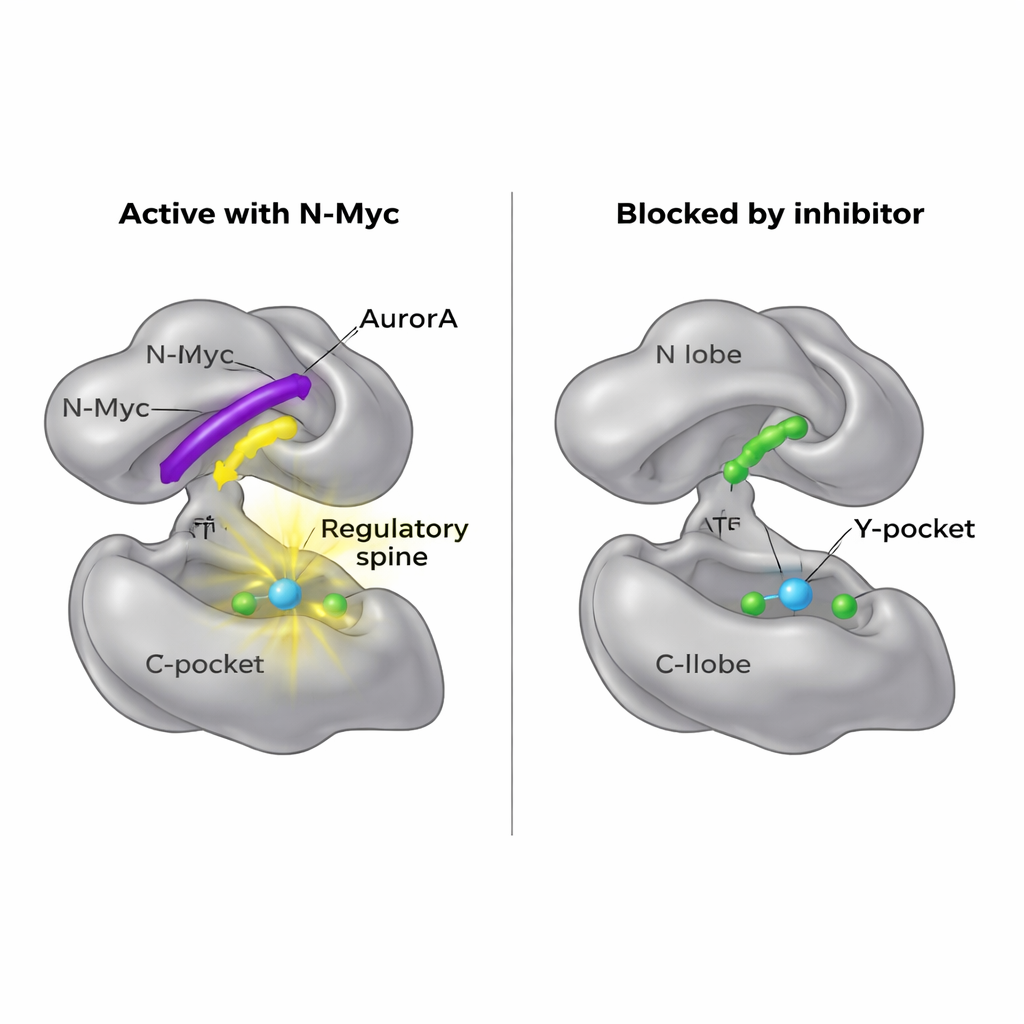
Sbloccare un nuovo punto d’ingresso per i farmaci
Poiché N-Myc è difficile da colpire direttamente, i ricercatori si sono chiesti se fosse possibile bloccare invece il suo sito di aggancio su AurA. Le loro mappe strutturali hanno rivelato che MB0 e MBI occupano la stessa regione generale del N-lobo utilizzata da un altro partner, TPX2, per attivare AurA. Una piccola molecola chiamata AurkinA è già nota per insinuarsi nella Y-pocket e spostare TPX2. Negli esperimenti di legame, AurkinA ha efficacemente concorrenzialo con N-Myc per il N-lobo di AurA, impedendo l’attacco sia dei frammenti N-Myc1–69 sia di N-Myc1–100. Questo risultato dimostra che la superficie del N-lobo, e in particolare la Y-pocket, è un punto caldo farmacologicamente aggredibile che controlla non solo regolatori classici come TPX2 ma anche oncoproteine disordinate come N-Myc.
Cosa significa per le terapie future
Questo lavoro riconfigura il rapporto N-Myc–AurA come un abbraccio dinamico con molteplici contatti centrato sul N-lobo di AurA, piuttosto che come un singolo sito di legame rigido. Per i non specialisti, il messaggio chiave è che anche una proteina tumorale senza forma definita come N-Myc può essere affrontata in modo indiretto colpendo una patch di aggancio solida sul suo enzima partner. Dimostrando che composti esistenti che si legano al N-lobo possono spingere via N-Myc da AurA, lo studio apre una via chiara verso farmaci che interrompono selettivamente questa interazione. Tali agenti potrebbero indebolire un supporto critico per N-Myc nei tumori pediatrici ad alto rischio e, con ulteriore sviluppo, offrire una nuova strategia terapeutica per tumori da lungo tempo considerati “non druggabili.”
Citazione: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Parole chiave: N-Myc, Aurora kinase A, proteine intrinsecamente disordinate, neuroblastoma, inibitori delle interazioni proteina–proteina