Clear Sky Science · it
Un atlante spazialmente risolto del glioblastoma umano rivela distinti modelli cellulari e molecolari dei nicchie anatomiche
Perché questa mappa del cancro cerebrale è importante
Il glioblastoma è uno dei tumori cerebrali più letali, in parte perché ogni tumore è un mosaico di diversi tipi cellulari e microambienti. Le scansioni standard e gli esami di laboratorio vedono il tumore per lo più come un’unica massa. Questo studio costruisce un “atlante” ad alta risoluzione che mostra dove si trovano i principali tipi cellulari all’interno dei glioblastomi umani, come queste cellule si raggruppano in quartieri distinti e in che modo alcuni di questi quartieri possono contribuire alla ricrescita tumorale e ridurre la sopravvivenza dei pazienti.
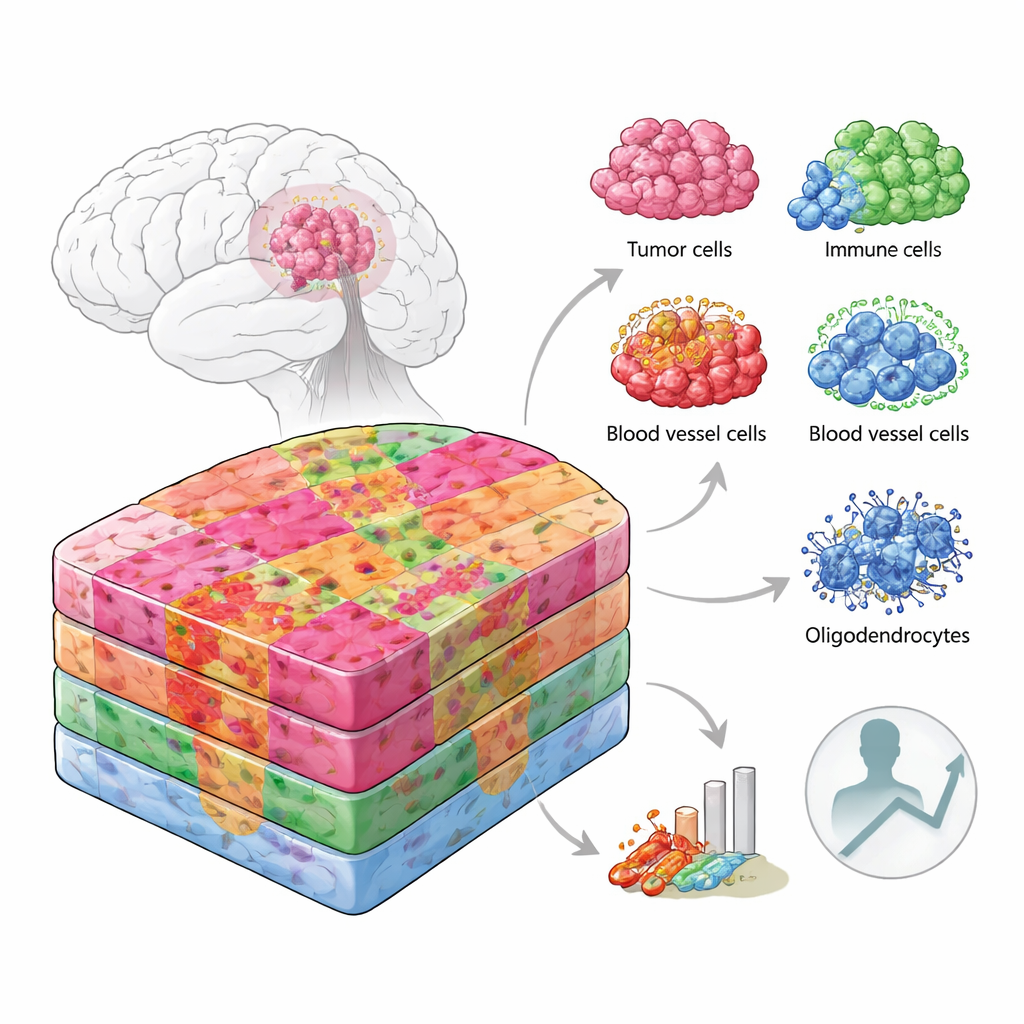
Guardare i tumori come mappe cittadine
Invece di trattare un’area tumorale come uniforme, i ricercatori l’hanno affrontata come una mappa urbana, in cui ogni quartiere ha la propria struttura e i propri abitanti. Hanno combinato diverse tecniche all’avanguardia che misurano l’attività genica in migliaia di piccolissimi punti distribuiti nel tessuto tumorale, e hanno integrato questi dati con informazioni a singola cellula e misure proteiche. È importante che lo abbiano fatto non solo su campioni congelati freschi prelevati in sala operatoria, ma anche su tessuti ospedalieri di routine conservati in paraffina, che sono quelli che la maggior parte dei laboratori di anatomia patologica effettivamente archiviano. In totale hanno analizzato più di 100.000 regioni marcate spazialmente e oltre 220.000 singole cellule provenienti da pazienti di età e background genetici diversi, coprendo sia il nucleo denso del tumore sia i suoi margini più diffusi.
Quartieri nascosti all’interno del glioblastoma
Sovrapponendo l’attività genica alle immagini microscopiche ad alto ingrandimento, il team ha diviso ogni tumore in “nicchie” anatomiche, come il fronte di invasione dove le cellule tumorali infiltrano il cervello sano, le zone centrali affollate, aree ricche di vasi sanguigni e regioni attorno a tessuto necrotico o povero di ossigeno. Ogni nicchia ospitava una propria miscela di tipi cellulari. Il margine del tumore nella sostanza grigia era ricco di neuroni e cellule di supporto tipiche, mentre il margine nella sostanza bianca conteneva molti oligodendrociti, le cellule che normalmente isolano le fibre nervose. Alcune nicchie vascolari erano piene di cellule specializzate dei vasi e cellule di supporto, mentre altre erano dominate da cellule immunitarie e tessuto cicatriziale. Le zone ipossiche vicino al tessuto necrotico contenevano per lo più cellule tumorali aggressive di tipo mesenchimale e macrofagi, con una diversità cellulare molto ridotta.
Un ruolo sorprendente per le cellule di supporto
Una delle scoperte più sorprendenti riguardava gli oligodendrociti, solitamente considerati silenziosi “isolanti” nel cervello. L’atlante ha rivelato quattro stati distinti di oligodendrociti, incluso un tipo finora sottovalutato che compariva quasi esclusivamente nei nuclei dei glioblastomi. Queste cellule avevano perso molti dei geni correlati alla mielina e avevano invece attivato geni legati all’infiammazione e allo stress, somigliando agli oligodendrociti associati a malattia osservati nella sclerosi multipla e in altri disturbi cerebrali. Spazialmente, questa popolazione di oligodendrociti con carattere immune si raggruppava in una “nicchia immune–gliale” insieme a microglia attivata, macrofagi, cellule vascolari anomale e cellule tumorali di tipo mesenchimale, ma significativamente non nelle regioni più prive di ossigeno.
Collegare i modelli microscopici all’esito dei pazienti
Gli autori hanno quindi verificato se i programmi genici che definiscono questi stati degli oligodendrociti ricomparivano in grandi raccolte di campioni tumorali associate ai dati clinici dei pazienti. In due coorti indipendenti di glioma, una firma di oligodendrociti convenzionali, produttori di mielina, era associata a una sopravvivenza migliore, anche dopo avere corretto per età e principali marcatori genetici di rischio. Al contrario, la firma di oligodendrociti attivati dal punto di vista immune era correlata a una sopravvivenza peggiore ed era più prominente nei tumori aggressivi e resistenti ai trattamenti, specialmente in quelli recidivati dopo terapia e privi di una comune alterazione di metilazione legata alla riparazione del DNA. Questo suggerisce che il riprogrammarsi degli oligodendrociti all’interno del tumore, e la loro posizione rispetto alle cellule tumorali e immunitarie, possa influenzare la risposta alla terapia e la probabilità di recidiva.
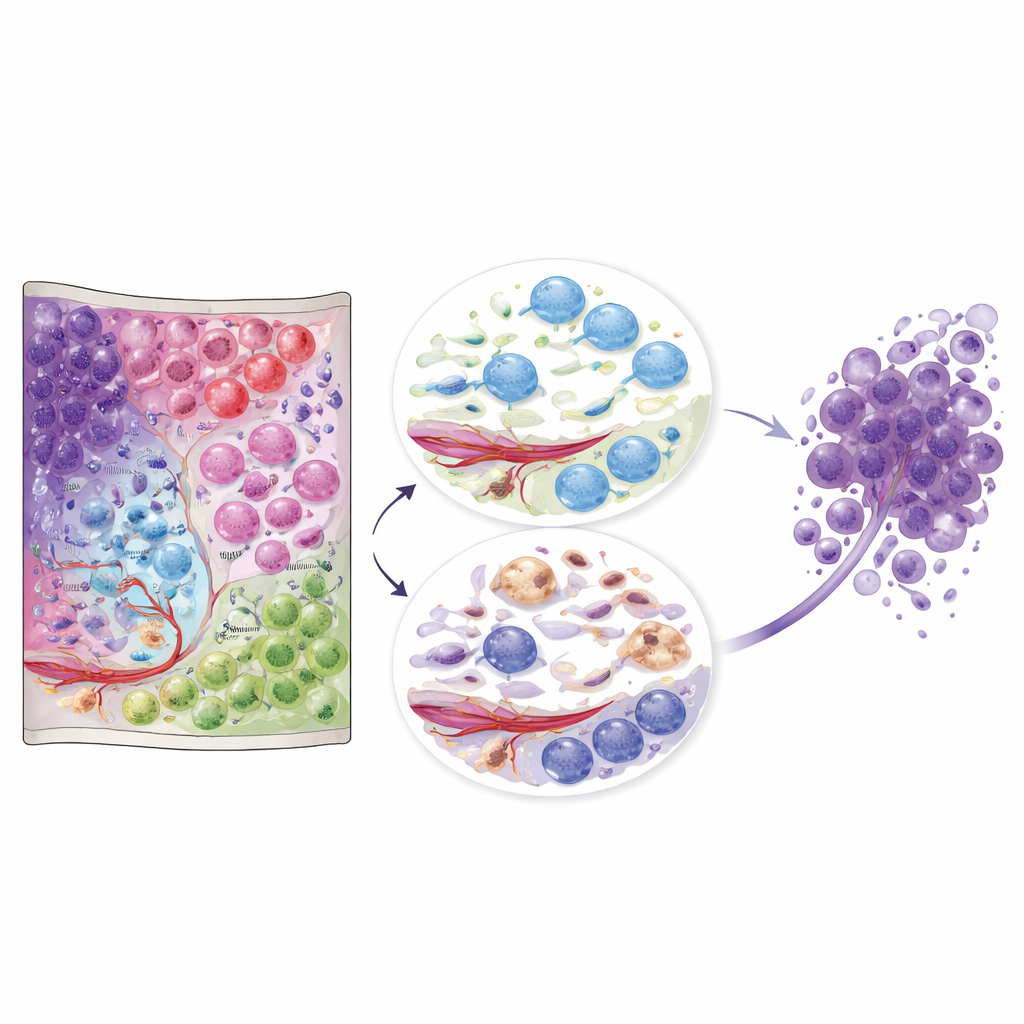
Cosa significa questo atlante per la cura futura
Nel complesso, questi dati trasformano il glioblastoma da una massa sfocata in un paesaggio dettagliato di comunità cellulari in interazione. Per i non specialisti, il messaggio chiave è che posizione e vicinato contano: gli stessi ampi tipi cellulari si comportano in modo molto diverso a seconda della nicchia che occupano. L’atlante pubblicamente disponibile offre un riferimento che altri ricercatori e clinici possono usare per collocare i propri campioni in questo contesto spaziale. A lungo termine, le terapie potrebbero essere progettate non solo per uccidere le cellule tumorali, ma per interrompere nicchie dannose — come le regioni immune‑cicatriziali o le sacche di oligodendrociti immune‑attivati — che sembrano favorire la sopravvivenza tumorale e la recidiva.
Citazione: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
Parole chiave: glioblastoma, trascrittomica spaziale, microambiente tumorale, oligodendrociti, atlante del cancro cerebrale