Clear Sky Science · it
Spatial perturb-seq: genomica funzionale a cellula singola nell’architettura tissutale intatta
Vedere i geni in azione nei circuiti cerebrali vivi
Molte malattie cerebrali, dall’Alzheimer al Parkinson, sono correlate a geni di rischio, ma sappiamo ancora poco su come questi geni influenzino singole cellule all’interno del cervello vivo. Questo studio introduce un metodo potente per osservare cosa succede quando geni specifici vengono spenti in singole cellule, mentre queste rimangono nei loro quartieri naturali all’interno del tessuto cerebrale. L’approccio, chiamato Spatial Perturb-Seq, aiuta a collegare il rischio genetico a comportamenti cellulari alterati e alla comunicazione cellula-cellula nel cervello intatto.
Un nuovo modo per testare molti geni contemporaneamente
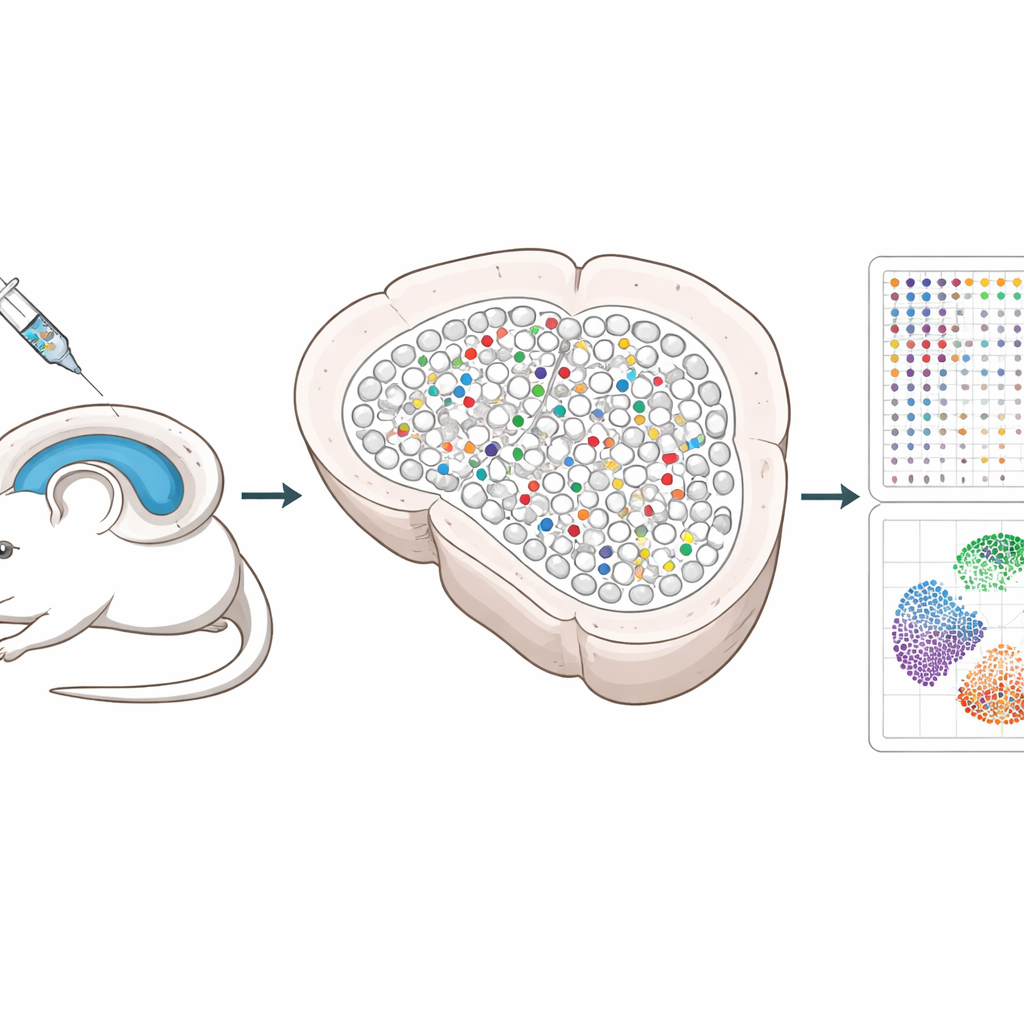
I ricercatori hanno messo a punto un sistema che utilizza strumenti di editing genico CRISPR veicolati da virus innocui all’ippocampo, una regione cerebrale importante per la memoria. Ogni virus porta tre guide che disattivano un gene scelto, insieme a un “codice a barre” di DNA unico e a un marcatore fluorescente in modo che le cellule modificate possano essere ritrovate in seguito. Mischiando questi virus e iniettandoli a bassa dose, viene modificata solo una piccola e sparsa frazione di cellule, mentre la maggior parte dei vicini resta intatta. Questo schema sparso permette agli scienziati di separare i cambiamenti che avvengono dentro le cellule modificate da quelli che avvengono nelle cellule sane vicine.
Mantenere intatta la mappa del cervello
I metodi tradizionali a cellula singola richiedono che i tessuti vengano disgregati, il che distrugge le posizioni precise delle cellule e può far perdere anche neuroni fragili. Spatial Perturb-Seq invece legge l’attività genica direttamente da sottili sezioni cerebrali, così la posizione di ogni cellula viene preservata. Utilizzando una tecnologia chiamata Stereo-seq, il gruppo ha catturato profili di espressione genica completi per più di 200.000 cellule, leggendo anche i codici a barre CRISPR e registrando le coordinate di ciascuna cellula nel tessuto. Hanno poi usato algoritmi avanzati basati su immagini per delineare ogni cellula e strumenti computazionali per identificare i tipi cellulari e i quartieri locali, concentrandosi in particolare sui neuroni ippocampali e i loro contatti stretti.
Come le cellule modificate influenzano i loro vicini
Con la mappa tissutale a disposizione, gli scienziati hanno confrontato i neuroni modificati con neuroni non modificati e, separatamente, con i vicini non modificati che circondavano ogni cellula modificata. Questo ha permesso di distinguere gli effetti “cell-autonomi” (all’interno della cellula modificata) dagli effetti “non cell-autonomi” (nell’ambiente microambientale circostante). L’abbattimento di 18 diversi geni, molti legati al rischio di malattie neurodegenerative, ha prodotto schemi distinti di cambiamenti genici all’interno dei neuroni modificati. Alcune modifiche, come quelle che prendono di mira il gene Cfap410, hanno anche innescato forti cambiamenti nell’attività genica delle cellule vicine, riflettendo segnali locali e meccanismi di supporto alterati.
Indizi sui percorsi delle malattie neurodegenerative
Alcuni geni hanno offerto spunti particolarmente interessanti. Disabilitare Lrrk2, un importante gene di rischio per il morbo di Parkinson, ha causato grandi cambiamenti nei neuroni modificati, inclusa la riduzione dei livelli di Bc1, una molecola di RNA importante per la regolazione della produzione proteica alle sinapsi. Allo stesso tempo, le cellule vicine hanno mostrato un’espressione alterata di geni coinvolti nella struttura sinaptica, nel traffico proteico e nella gestione del calcio, suggerendo che i problemi legati a Lrrk2 si propagano nei circuiti locali. L’abbattimento di un altro gene, Srf, ha disturbato una rete di geni legati alla crescita e alla plasticità neuronale e ha indebolito specifiche vie di segnalazione ligando-recettore tra i neuroni, indicando una comunicazione cellula-cellula compromessa. Valutando sistematicamente queste coppie di segnali, il team è stato in grado di individuare quali rotte di comunicazione risultavano più colpite per ciascun gene.
Strumenti flessibili per mappare gli effetti genetici
Per dimostrare che Spatial Perturb-Seq non è vincolato a una singola piattaforma, i ricercatori lo hanno anche adattato a un sistema basato sull’imaging chiamato Xenium. Lì, pannelli di sonde preprogettati e sonde codice a barre personalizzate leggono geni selezionati e codici a barre direttamente nel tessuto. Pur essendo questo approccio mirato in grado di coprire meno geni rispetto al trascrittoma completo di Stereo-seq, i pattern di cambiamento genico per modifiche chiave come Lrrk2 e Srf erano in buon accordo tra i due metodi e con un ampio atlante cerebrale esterno. Questa verifica incrociata sostiene la robustezza degli effetti osservati su geni e quartieri cellulari.
Cosa significa per la ricerca sulla salute del cervello
In termini concreti, Spatial Perturb-Seq consente agli scienziati di spegnere molti geni diversi in singole cellule cerebrali e poi osservare come quelle cellule e i loro vicini immediati reagiscono, il tutto mantenendo intatto il diagramma delle connessioni del tessuto. Questo rende possibile tracciare come i fattori di rischio genetico perturbino non solo singole cellule ma anche le conversazioni tra di esse, che sono cruciali per il funzionamento cerebrale sano. Col tempo, man mano che il sequenziamento diventerà più economico e verranno condotti esperimenti su scala maggiore, questo approccio potrebbe aiutare a rivelare quali geni e circuiti locali sono più importanti nelle fasi iniziali di disturbi come Alzheimer, Parkinson e SLA, guidando strategie di trattamento più mirate.
Citazione: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Parole chiave: genomica spaziale, screen CRISPR, sequenziamento a cellula singola, neurodegenerazione, comunicazione cellula-cellula