Clear Sky Science · it
FLEXTAG: un sistema piccolo e autorinnovabile per etichettare le proteine per immagini super-risolute multicolore resistenti allo sbiadimento
Vedere l’invisibile all’interno delle cellule
Gran parte della biologia moderna si basa sul fotografare le molecole che mantengono vive le nostre cellule. Ma anche i migliori microscopi ottici devono affrontare un problema semplice: i marcatori fluorescenti usati per evidenziare le proteine si spengono rapidamente, ed è difficile etichettare molti bersagli diversi contemporaneamente senza alterare il funzionamento cellulare. Questo studio introduce FLEXTAG, una nuova famiglia di marker piccoli e ricaricabili che rimangono fluorescenti molto più a lungo, supportano più colori e funzionano con i microscopi più potenti che gli scienziati usano per vedere l’architettura interna delle cellule.
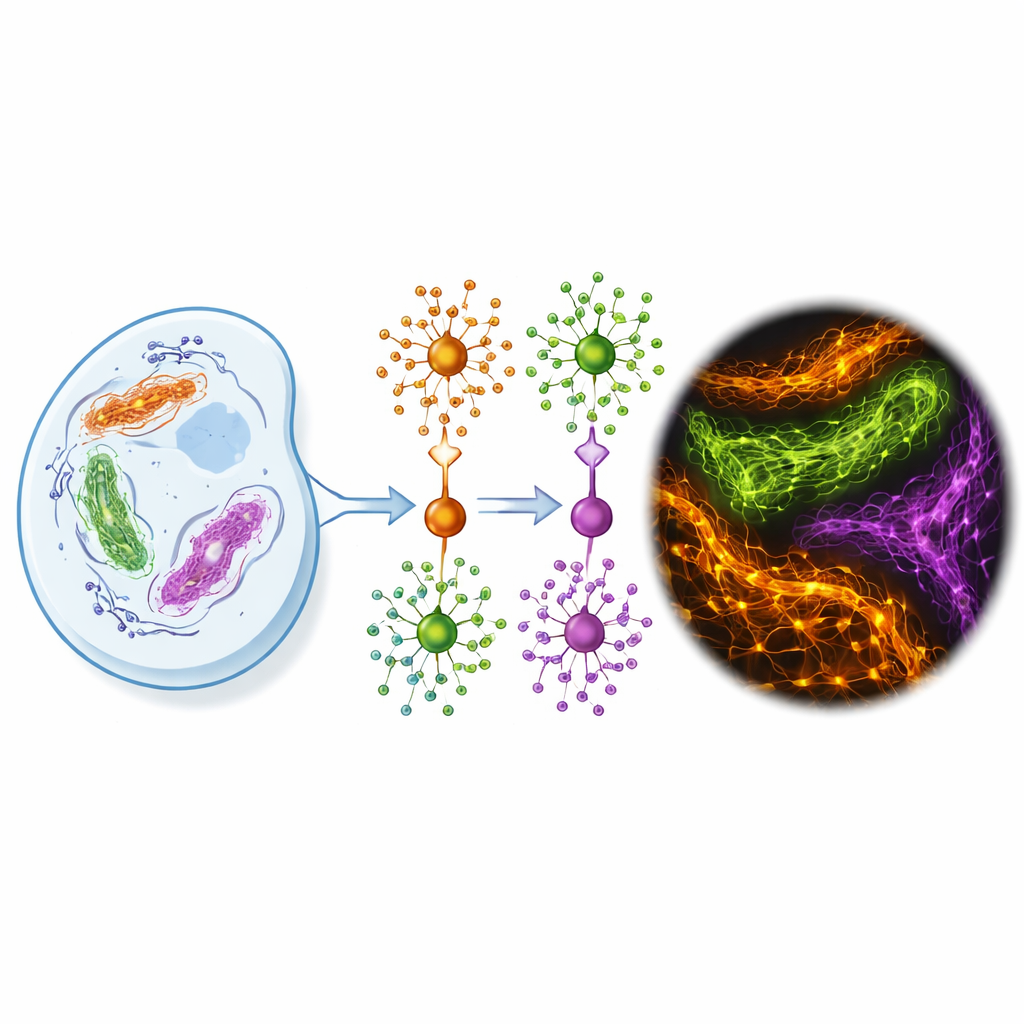
Perché è così difficile ottenere immagini cellulari più nitide
I microscopi a fluorescenza convenzionali possono rivelare strutture dell’ordine di un quarto di micrometro, che resta comunque molto più grande della maggior parte delle singole proteine. I metodi a super-risoluzione estraggono dettagli più fini, arrivando a pochi miliardesimi di metro, ma solo se i marcatori fluorescenti si comportano perfettamente. I marcatori proteici più usati oggi sono o anticorpi ingombranti, o proteine fluorescenti poco luminose, o tag chimici i cui coloranti si consumano rapidamente sotto la luce intensa richiesta da queste tecniche. Fissare le cellule con agenti chimici per l’imaging dettagliato può inoltre legare le proteine in modi che impediscono ai coloranti di raggiungere i loro bersagli, e molecole di colorante libere possono aderire in modo non specifico, offuscando l’immagine con un bagliore di fondo.
Un nuovo tipo di tag proteico ricaricabile
Gli autori hanno progettato FLEXTAG (acronimo di Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy) per affrontare direttamente questi limiti. FLEXTAG non è un singolo tag ma un trio coordinato—FLEXTAG1, FLEXTAG2 e FLEXTAG3—ognuno un piccolo protein engineering (12–18 kilodalton, circa la metà delle dimensioni di tag classici come GFP e molto più piccolo di HaloTag). Ogni FLEXTAG si lega a un ligando di piccole dimensioni corrispondente che porta un colorante organico brillante. Fondamentale è che questo legame è reversibile: le molecole ligando–colorante si alternano continuamente. Quando un fluoroforo viene danneggiato dalla luce, uno nuovo dalla soluzione circostante prende il suo posto, così il segnale si “autorinnova” invece di decadere costantemente.
Costruire tre tag compatti e affidabili
Per creare FLEXTAG1–3, il team ha riadattato tre noti scaffold proteici della biologia cellulare e del design farmacologico, quindi ha usato modellazione strutturale e saggi basati su imaging per rimodellare il loro comportamento. FLEXTAG1 deriva da una proteina bromodominio che riconosce una piccola molecola modificata; gli autori hanno introdotto mutazioni per interrompere la tendenza all’associazione e alla formazione di aggregati, preservando al contempo un forte legame con il ligando. FLEXTAG2 proviene dalla diidrofolato reduttasi batterica. Aggiungendo un ponte disolfuro strategico e regolando connettori flessibili, hanno stabilizzato la proteina e aumentato notevolmente la frazione di tag carichi di colorante in ogni momento, mantenendo però la reversibilità del legame. FLEXTAG3 si basa su una proteina umana FKBP usata in biologia chimica; in questo caso il gruppo ha bilanciato l’affinità e la cinetica di legame in modo che i coloranti si stacchino abbastanza rapidamente da essere sostituiti, ma ancora abbastanza saldamente da fornire immagini luminose ed evitare eccessive aggregazioni.
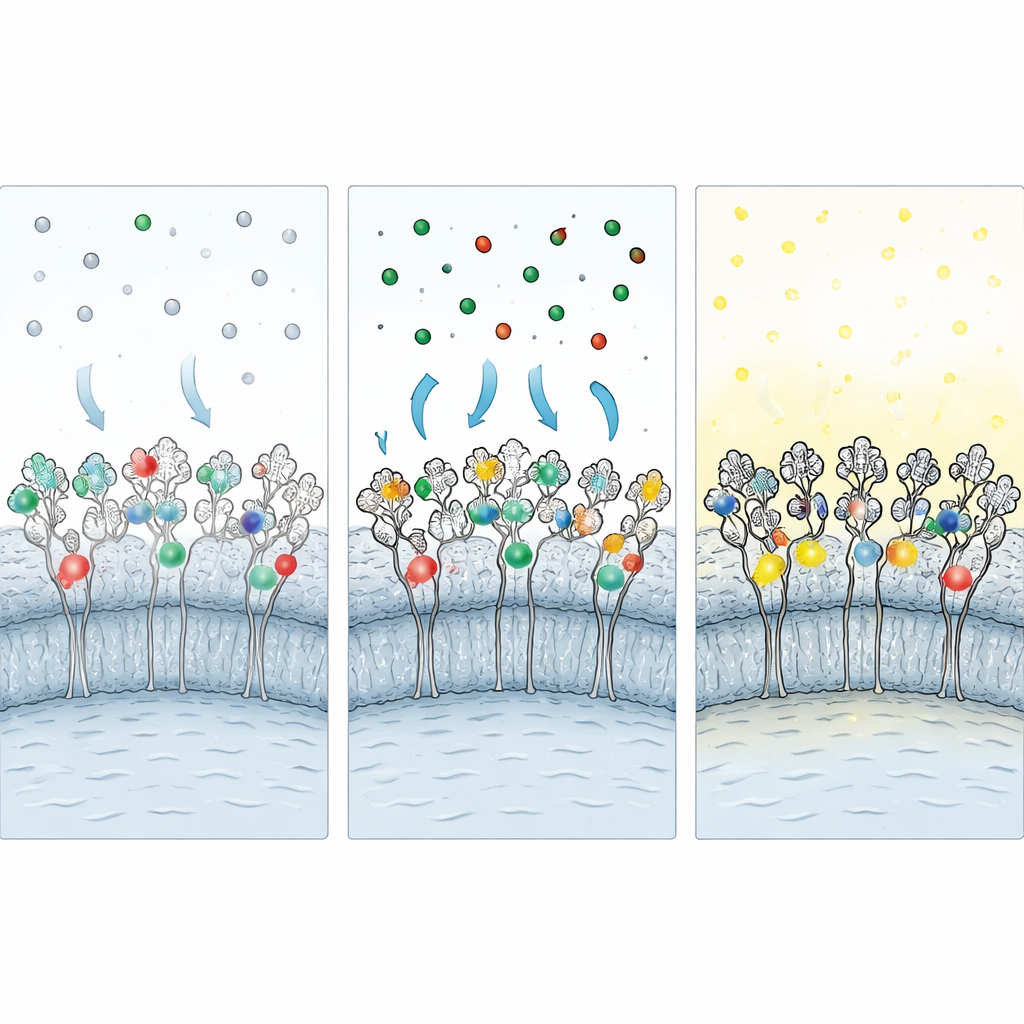
Proteggere i tag durante la fissazione e ridurre il fondo
Poiché molti esperimenti importanti richiedono l’imaging di cellule fissate, i ricercatori hanno sviluppato una strategia di “fissazione protettiva”. Prima di aggiungere fissativi aldeidici, saturano le cellule vive con versioni non etichettate di ciascun ligando, bloccando la tasca di legame del tag. Durante la fissazione, questi ligandi protettivi schermano gli amminoacidi vulnerabili dall’incrossamento chimico. Dopo la fissazione, i ligandi protettivi vengono lavati via e sostituiti con quelli fluorescenti, ripristinando l’accesso al tag. Passaggi aggiuntivi—riduzione chimica per neutralizzare gruppi reattivi residui e un cocktail di blocco contenente albumina, tensioattivo e un sale caotropico—riducono ulteriormente il legame non specifico dei coloranti liberi. Insieme, queste misure conservano circa il 60–70% dell’etichettatura vista nelle cellule vive migliorando nettamente il rapporto segnale/rumore.
Filmati più nitidi e duraturi su molte tecniche
Con il framework FLEXTAG operativo, gli autori lo hanno testato nelle principali famiglie di microscopia a super-risoluzione. Nei metodi a illuminazione strutturata come SIM e STED, i FLEXTAG hanno consentito imaging multicolore di mitocondri, microtubuli, reticolo endoplasmatico e actina con molto meno sbiadimento rispetto ai tag covalenti standard; in dozzine di cicli di imaging, il segnale dei tag convenzionali scendeva della metà o più, mentre i segnali FLEXTAG restavano quasi costanti. Nei metodi a singola molecola come PAINT e STORM, il rapido scambio on–off dei ligandi FLEXTAG ha prodotto flussi ricchi e stabili di localizzazioni che potevano essere trasformati in mappe tridimensionali e multicolore di strutture subcellulari, anche in cellule vive per molti minuti. FLEXTAG2 ha mostrato cinetiche particolarmente favorevoli per PAINT, mentre FLEXTAG3 ha eccelso in filmati STORM di lunga durata. Poiché i tag sono ortogonali tra loro e compatibili con una vasta palette di coloranti, gli scienziati possono etichettare più proteine contemporaneamente e poi scegliere la modalità di imaging più adatta alla loro domanda senza cambiare i costrutti di base.
Cosa significa per l’osservazione all’interno delle cellule
FLEXTAG offre una sorta di connettore universale e ricaricabile tra proteine e coloranti brillanti. Le sue dimensioni ridotte diminuiscono il rischio che il tag distorca la localizzazione o la funzione di una proteina, e i suoi coloranti autorinnovabili aiutano a superare il problema di lunga data del fotobleaching nei microscopi ad alta potenza. Abbinando questi tag a fissazione protettiva e chimica per sopprimere il fondo, i ricercatori possono ottenere viste più pulite, durature e più colorate dell’organizzazione e del movimento delle proteine all’interno delle cellule. In termini pratici, ciò si traduce in mappe migliori dell’architettura cellulare, tracciamenti più affidabili delle interazioni molecolari nel tempo e in una cassetta degli attrezzi versatile che dovrebbe avvantaggiare sia la biologia cellulare di base sia gli studi traslazionali che si basano sull’osservazione di cambiamenti legati a malattie alla scala nanometrica.
Citazione: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Parole chiave: microscopia a super-risoluzione, marcatura con proteine fluorescenti, imaging di cellule vive, resistenza al fotobleaching, architettura cellulare