Clear Sky Science · it
Upcycling efficiente del metanolo in etilene glicole e glicolaldeide tramite sintesi divergente di accoppiamento C−C
Trasformare un combustibile semplice in blocchi di costruzione utili
Il metanolo, un alcol semplice che può essere prodotto a partire da anidride carbonica, gas naturale, carbone o biomassa, è già un combustibile e una materia chimica di rilievo. Questo studio mostra come fasci di luce e nanomateriali progettati con cura possano trasformare il metanolo in molecole più complesse e di maggior valore—rilasciando nello stesso tempo idrogeno gassoso come vettore energetico pulito. Il lavoro rivela un nuovo modo di indirizzare un unico materiale di partenza verso due prodotti utili diversi semplicemente cambiando come singoli atomi metallici sono disposti sulla superficie di un catalizzatore estremamente piccolo. 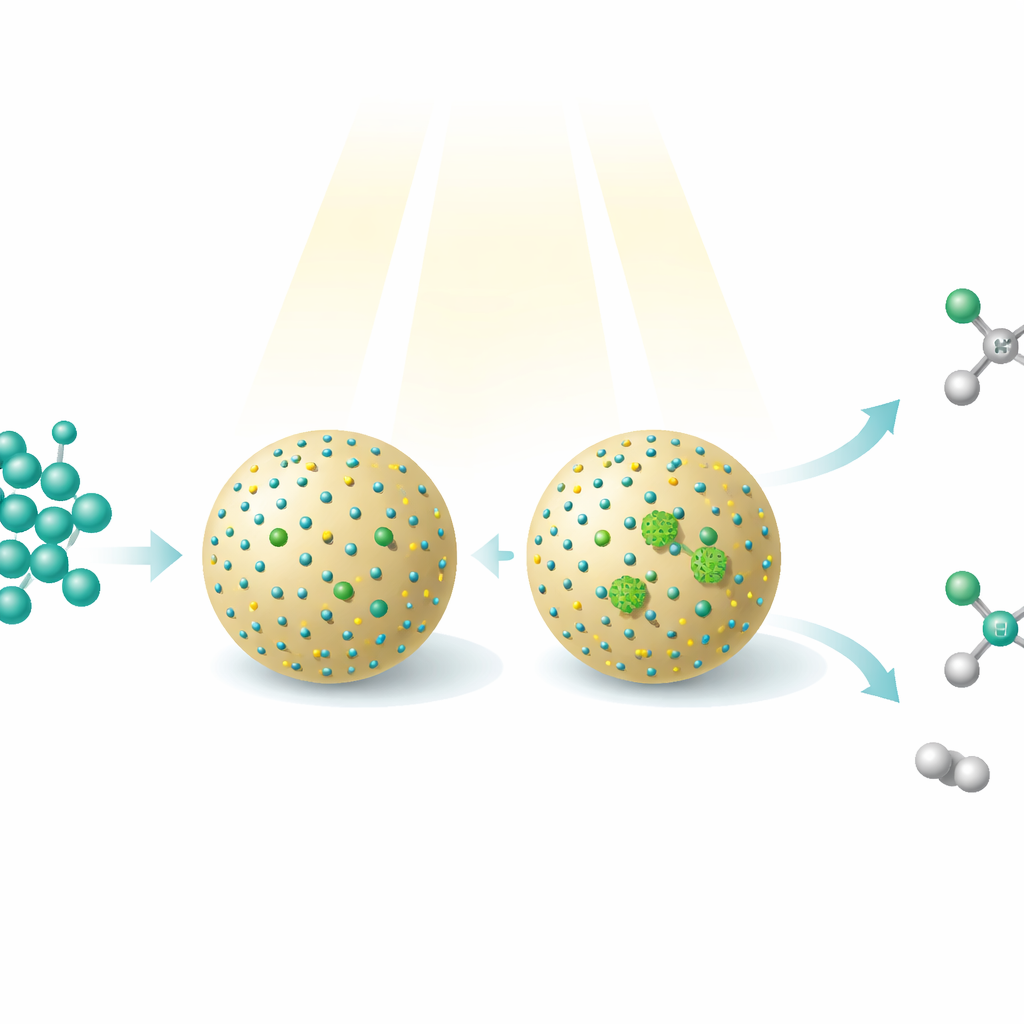
Perché conviene migliorare il metanolo
Mentre il mondo cerca alternative al petrolio, il metanolo è emerso come un liquido attraente che può immagazzinare energia e carbonio. Tuttavia, la maggior parte dei processi industriali che trasformano il metanolo in molecole più grandi sono strumenti rozzi: richiedono alte temperature, dipendono da vie fossili e spesso generano molti sottoprodotti indesiderati. I chimici vorrebbero accoppiare le molecole di metanolo con grande precisione per poter produrre selettivamente solo i composti desiderati. Eseguire questo sotto condizioni miti usando la luce invece del calore renderebbe più semplice integrare la produzione chimica con energie rinnovabili.
Nanosfere attivate dalla luce fanno il lavoro
I ricercatori hanno costruito un fotocatalizzatore—letteralmente un catalizzatore azionato dalla luce—decorando piccolissimi punti quantici di solfuro di cadmio su particelle sferiche di silice. Questi punti quantici assorbono la luce e generano elettroni ed “holes” energetici che possono strappare atomi di idrogeno dal metanolo, formando frammenti altamente reattivi. Successivamente sono stati depositati atomi di nichel sui punti quantici in due modi distinti. In un materiale il nichel esisteva principalmente come atomi singoli isolati; nell’altro il nichel formava piccolissimi aggregati di alcuni atomi. Sebbene la composizione complessiva sia cambiata di poco, questa sottile differenza nell’organizzazione del nichel ha alterato drasticamente quali reazioni avvenivano sulla superficie.
Due progetti di nichel, due prodotti puliti
Quando il catalizzatore con atomi singoli di nichel è stato esposto alla luce in metanolo, ha favorito l’accoppiamento di due frammenti identici derivati dal metanolo, portando principalmente alla formazione di etilene glicole—un diolo a due carboni ampiamente usato negli antigelo e nelle materie plastiche. Questa via ha raggiunto circa il 90% di selettività, il che significa che quasi tutto il metanolo convertito è finito in questo singolo prodotto, mentre l’idrogeno gassoso è stato prodotto in quantità corrispondenti dagli atomi di idrogeno rimossi. Al contrario, il catalizzatore con aggregati di nichel ha incanalato gli stessi frammenti di metanolo lungo un percorso diverso. Qui, una porzione di metanolo è stata ulteriormente ossidata fino a un intermedio simile al formaldeide, di breve durata, che poi si è combinato con un altro frammento per formare glicolaldeide, un altro composto a due carboni con molte applicazioni nelle chimiche fini e potenzialmente nei processi bio-based. Questa via ha fornito glicolaldeide con il 96% di selettività, di nuovo insieme a idrogeno. Il supporto in silice ha aiutato i punti quantici a catturare la luce in modo più efficiente e ha reso le particelle più robuste su molti cicli d’uso. 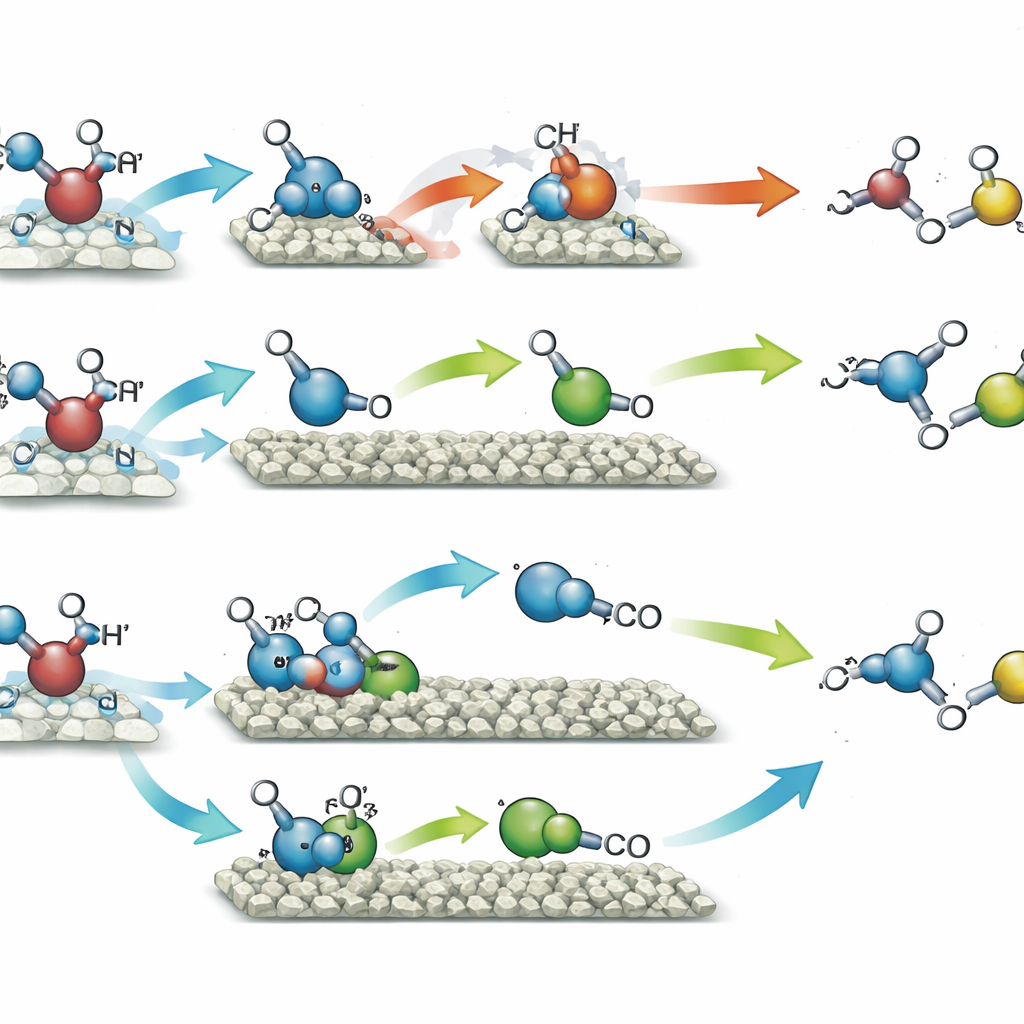
Uno sguardo sotto il cofano della reazione
Per capire perché i due allineamenti del nichel si comportassero così diversamente, il gruppo ha combinato una serie di misure avanzate con simulazioni al calcolatore. Esperimenti di risonanza paramagnetica elettronica hanno mostrato che entrambi i catalizzatori generavano radicali a base di metanolo sotto la luce, ma il catalizzatore con aggregati promuoveva anche la rottura del legame ossigeno–idrogeno, portando a frammenti di reazione più diversificati e all’intermedio formaldeidico. Test temporali hanno confermato che questo intermedio aumentava e poi diminuiva in concentrazione mentre veniva consumato per formare la glicolaldeide. Calcoli quantochimici hanno mappato i costi energetici di ogni piccolo passaggio. Sugli atomi singoli di nichel, l’accoppiamento diretto di due radicali identici per formare etilene glicole era la via più agevole. Sugli aggregati di nichel, lo stesso accoppiamento tratteneva troppo fortemente il prodotto, rendendone difficile il distacco, mentre la via che formava prima l’intermedio asimmetrico e poi la glicolaldeide diventava energeticamente favorita.
Una nuova leva per una chimica più pulita
In termini pratici, questo lavoro mostra che il “dove” ogni atomo di nichel è posizionato su una superficie a scala nanometrica può decidere il “in cosa” il metanolo si trasforma quando illuminato dalla luce. Alternando tra atomi singoli e piccoli aggregati di nichel, i ricercatori possono invertire il prodotto principale da etilene glicole a glicolaldeide, entrambi ottenuti in modo efficiente e pulito insieme a combustibile a idrogeno. Questa strategia di progettare catalizzatori atomo per atomo offre una via promettente per valorizzare materie prime semplici e rinnovabili come il metanolo in una gamma di prodotti chimici utili senza dipendere dal petrolio, da condizioni severe o da reazioni collaterali sprecone.
Citazione: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Parole chiave: upcycling del metanolo, fotocatalisi, atomi singoli di nichel, etilene glicole, glicolaldeide