Clear Sky Science · it
L’inclusione degli esoni consente una stima accurata dell’attività dei fattori di splicing
Leggere i segni nascosti di editing della cellula
Ogni cellula del nostro corpo modifica costantemente i suoi messaggi di RNA prima di tradurli in proteine. Questa modifica, chiamata splicing, contribuisce a decidere se una cellula rimane sana o diventa cancerosa. Lo studio alla base di questo articolo mostra che, osservando con attenzione quali frammenti di RNA vengono mantenuti o saltati — le cosiddette firme di inclusione degli esoni — gli scienziati possono inferire con precisione l’attività degli “editor” molecolari che controllano lo splicing, anche in malattie complesse come il cancro.
Come le cellule tagliano e incollano i loro messaggi
I geni non vengono letti in un unico tratto continuo. Le cellule rimuovono segmenti non codificanti e ricollegano tra loro i pezzi codificanti, noti come esoni, per costruire i messaggi finali di RNA. Proteine specializzate chiamate fattori di splicing guidano questo processo di taglia‑e‑incolla, decidendo quali esoni includere. Il loro comportamento è influenzato da molti livelli di regolazione: quanto del loro RNA e della loro proteina viene prodotto, come vengono chimicamente modificati, dove si localizzano nella cellula e come interagiscono con altre proteine. Poiché così tante leve possono modificare il comportamento dei fattori di splicing, misurare semplicemente un tipo di dato — per esempio l’espressione genica — spesso non rivela quello che questi fattori stanno realmente facendo.
Trasformare i pattern di esoni in letture di attività
Ispirati da lavori precedenti sui fattori di trascrizione, gli autori propongono una strategia diversa: invece di cercare di misurare i fattori di splicing direttamente, leggerne l’attività dagli effetti che producono. Quando un fattore di splicing cambia, l’inclusione dei suoi esoni bersaglio si sposta secondo schemi riconoscibili. Il team ha compilato centinaia di esperimenti in cui singoli fattori di splicing sono stati silenziati, eliminati o sovra‑espressi, e ha usato questi dati per costruire “reti empiriche” che collegano ciascun fattore agli esoni che influenzano chiaramente. Hanno quindi adattato un quadro computazionale chiamato VIPER per leggere una nuova firma di inclusione degli esoni e attribuire un punteggio su quanto ciascun fattore di splicing debba essere attivo per spiegare il pattern osservato.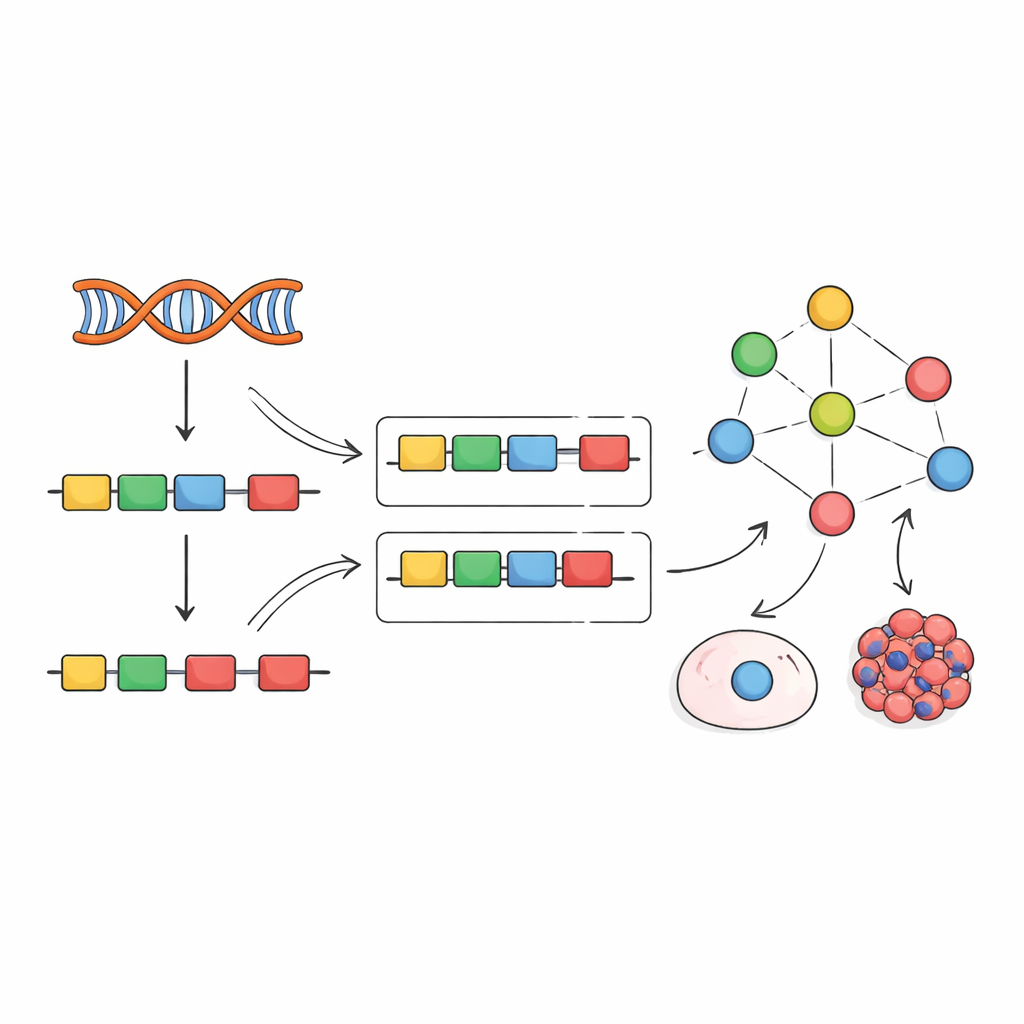
Testare il metodo in perturbazioni reali
Per verificare l’efficacia dell’approccio, i ricercatori hanno valutato diverse modalità di costruzione delle reti e di calcolo dei punteggi di attività. Le reti empiriche derivate direttamente da esperimenti di perturbazione, combinate con l’analisi di arricchimento di VIPER, hanno superato chiaramente le alternative basate solo sull’inferenza statistica. Il metodo ha identificato correttamente il fattore di splicing perturbato sperimentalmente nella maggior parte dei test, anche attraverso diversi tipi cellulari e studi. Ha inoltre catturato meccanismi regolatori più sottili. Per esempio, un farmaco antitumorale chiamato Indisulam provoca la degradazione della proteina del fattore di splicing RBM39 mentre i suoi livelli di RNA aumentano in quello che sembra un tentativo di compensazione. Un’analisi tradizionale dell’espressione suggerirebbe erroneamente che RBM39 sia più attivo, ma il punteggio di attività basato sugli esoni ha rivelato correttamente una forte perdita di funzione, in linea con l’azione nota del farmaco.
Scoprire programmi di splicing nascosti nel cancro
Armati di questo strumento, gli autori si sono rivolti al The Cancer Genome Atlas, analizzando dati a livello di esone provenienti da diversi tipi tumorali e dai tessuti sani corrispondenti. Hanno scoperto due ampi e ricorrenti programmi di splicing. Un programma è composto da fattori di splicing che tendono ad essere più attivi nei tumori ed è associato a una sopravvivenza peggiore dei pazienti — un programma con caratteristiche oncogeniche. L’altro presenta fattori sistematicamente meno attivi nei tumori e collegati a esiti migliori, somigliando a programmi di soppressione tumorale. Questi programmi riguardano geni coinvolti in tratti fondamentali del cancro come la rapida divisione cellulare e la capacità dei tumori di eludere il sistema immunitario. Per esempio, alcuni esoni regolati dal programma simile a un soppressore tumorale sembrano influenzare la risposta dei pazienti alle terapie con checkpoint immunitari, indicando nuovi marcatori o punti di intervento.
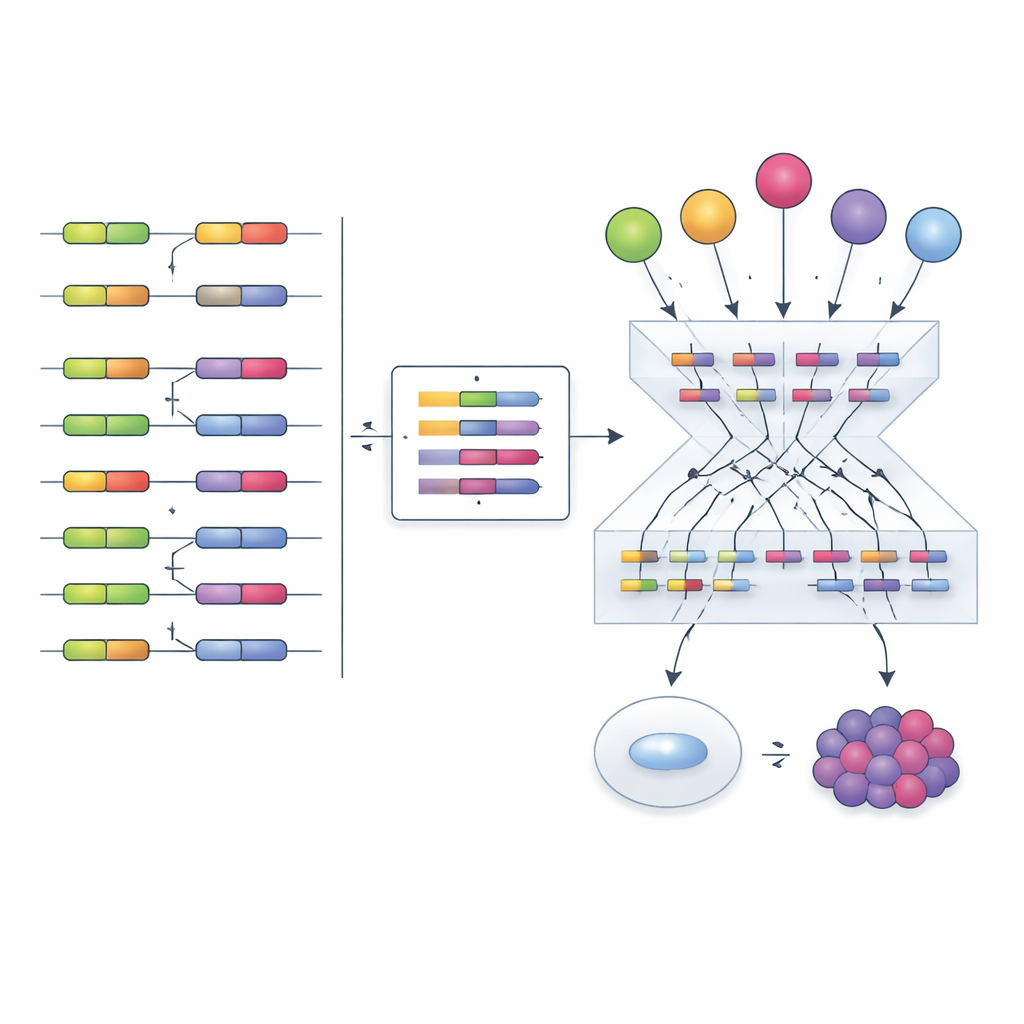
Seguire i cambiamenti di splicing lungo la progressione verso il cancro
Il team ha anche esaminato un modello passo‑passo di cellule umane che progrediscono da uno stato normale a uno immortalizzato, tumorigeno e infine metastatico. Hanno riscontrato che il programma con caratteristiche oncogeniche diventa più attivo man mano che le cellule acquisiscono mutazioni che guidano il cancro, mentre il programma simile a un soppressore si affievolisce. Integrando più livelli di dati — livelli di RNA, abbondanza proteica, modificazioni chimiche e cambiamenti di splicing all’interno degli stessi fattori di splicing — hanno identificato un insieme mirato di eventi molecolari candidati che potrebbero guidare questi cambi di programma, offrendo una lista prioritaria per future verifiche sperimentali.
Perché è importante per i pazienti e la ricerca futura
In sostanza, lo studio mostra che il comportamento complesso dei fattori di splicing può essere distillato in un unico punteggio di attività interpretabile, derivato da come gli esoni vengono inclusi o saltati. Questo rende possibile studiare la regolazione dello splicing in vaste coorti di pazienti e in esperimenti diversi usando solo dati di sequenziamento RNA standard, senza richiedere costosi profili multi‑omici. Per il lettore non specialista, il messaggio chiave è che i pattern di come i geni vengono tagliati e incollati contengono informazioni ricche sui sistemi di controllo nascosti della cellula, e che decodificare questi pattern può rivelare nuovi driver tumorali, migliorare la prognosi e orientare la ricerca verso terapie più precise.
Citazione: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Parole chiave: Splicing dell'RNA, fattori di splicing, genomica del cancro, trascrittomica, inferenza dell'attività proteica